Cho hỗn hợp (N, Al) lấy dư vào 91,6 g dung dịch H2SO4 21,4% thu được V lít khí H2 ở đktc. Tính V ?

Những câu hỏi liên quan
Cho 12,8 gam hỗn hợp X gồm Fe và FeO vào dung dịch H2SO4 loãng dư thấy có 2,24 lít H2 thoát ra.a-Tính số mol Fe và FeO.Biết khí đo ở đktc .(1đ)b-Cho toàn bộ lượng hỗn hợp X trên tác dụng với H2SO4 đặc nóng dư thu được V lít khí SO2 ở đktc .Tính V
\(n_{Fe}=a\left(mol\right),n_{FeO}=b\left(mol\right)\)
\(m_X=56a+72b=12.8\left(g\right)\)
\(n_{H_2}=n_{Fe}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(\Rightarrow a=0.1\)
\(b=\dfrac{12.8-56\cdot0.1}{72}=0.1\left(mol\right)\)
\(BTe:\)
\(3n_{Fe}+n_{FeO}=2n_{SO_2}\)
\(\Rightarrow n_{SO_2}=\dfrac{3\cdot0.1+0.1}{2}=0.2\left(mol\right)\)
\(V_{SO_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(\)
Đúng 0
Bình luận (0)
Cho một lượng hỗn hợp Al, Fe tác dụng với dung dịch H 2 S O 4 loãng, dư thấy thu được 8,96 lít khí ở đktc. Mặt khác, cho lượng hỗn hợp như trên tác dụng với dung dịch NaOH dư thì thu được 6,72 lít khí H 2 ở đktc. Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Cho m(g) hỗn hợp đồng và sắt vào dung dịch H2SO4 loãng dư thu được 0,1 (mol) khí H2 (đktc). Cũng cho m(g) hỗn hợp trên vào dung dịch H2SO4 đặc nóng thì thu được 4,48 lít SO2 (đktc). Tính m?
PTHH: \(Fe+H_2SO_{4\left(l\right)}\rightarrow FeSO_4+H_2\uparrow\)
\(2Fe+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
\(Cu+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}CuSO_4+SO_2\uparrow+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe}=n_{H_2}=0,1\left(mol\right)\\n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,1\left(mol\right)\\n_{Cu}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Cu}+m_{Fe}=0,1\cdot56+0,05\cdot64=8,8\left(g\right)\)
Đúng 2
Bình luận (0)
Giả sử: \(\left\{{}\begin{matrix}n_{Cu}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
_ Khi pư với H2SO4 loãng.
Theo ĐLBT mol e, có: 2y = 0,1.2 ⇒ y = 0,1 (mol) (1)
_ Khi pư với H2SO4 đặc nóng.
Ta có: \(n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo ĐLBT mol e, có: 2x + 3y = 0,2.2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,05\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
⇒ m = mCu + mFe = 0,05.64 + 0,1.56 = 8,8 (g)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Đề bài cho 0,1 g H2 hay 0,1 mol H2 bạn nhỉ?
Đúng 0
Bình luận (1)
Cho 33,2 g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch HCl thu được V lít khí ở đktc và chất rắn không tan Y. Cho Y hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2 (đktc). Phần trăm khối lượng của Cu trong hỗn hợp X là A. 57,83%. B. 33,33%. C. 19,28%. D. 38,55%.
Đọc tiếp
Cho 33,2 g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch HCl thu được V lít khí ở đktc và chất rắn không tan Y. Cho Y hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2 (đktc). Phần trăm khối lượng của Cu trong hỗn hợp X là
A. 57,83%.
B. 33,33%.
C. 19,28%.
D. 38,55%.
Cho m gam hỗn hợp G gồm: Na, Al, Fe vào nước dư thu được 4,48 lít khí (ở đktc). Mặt khác cho m gam G ở trên vào dung dịch NaOH dư thu được 7,84 lít khí (ở đktc) và dung dịch X, chất rắn Y. Hòa tan hoàn toàn Y vào
H
2
S
O
4
đặc, nóng thu được 5,04 lít khí (ở đktc). Giá trị của m là A. 23,9. B. 47,8. C. 16,1. D. 32,2
Đọc tiếp
Cho m gam hỗn hợp G gồm: Na, Al, Fe vào nước dư thu được 4,48 lít khí (ở đktc). Mặt khác cho m gam G ở trên vào dung dịch NaOH dư thu được 7,84 lít khí (ở đktc) và dung dịch X, chất rắn Y. Hòa tan hoàn toàn Y vào H 2 S O 4 đặc, nóng thu được 5,04 lít khí (ở đktc). Giá trị của m là
A. 23,9.
B. 47,8.
C. 16,1.
D. 32,2
Chọn C
Gọi số mol Na, Al và Fe có trong m gam G lần lượt là x, y và z (mol)
Do khi cho G vào nước thu được số mol khí ít hơn khi cho G vào NaOH dư nên khi cho G vào nước dư chỉ có Na phản ứng hết.

Đúng 0
Bình luận (0)
Cho 7,8 g hỗn hợp X gồm Mg, Al tác dụng vừa đủ với 800ml dung dịch gồm HCl 0,5M và H2SO4 0,25M thu được V lít khí H2 (đktc). Tính V và khối lượng hỗn hợp X
\(n_{H^+}=0,5.0,8+0,25.0,8.2=0,8\left(mol\right)\\ \Rightarrow n_{H_2}=\dfrac{n_{H^+}}{2}=\dfrac{0,8}{2}=0,4\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,4.22,4=8,96\left(l\right)\)
Không phải KL hhX cho rồi à ta?
Đúng 5
Bình luận (0)
Cho 13,4 gam hỗn hợp Al, CuO vào dung dịch H2SO4 10% dư thu được 6,72 lít khí H2(đktc)
a, Tính % mAl, mCuO
b, Cho 13,4 gam hỗn hợp trên tác dụng với dung dịch H2SO4 đặc nóng dư thu được dung dịch B. Tính VSO2 sản phâm khử duy nhất.
c, Tính C% các chất trong B
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH:
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
0,2 0,3
\(\rightarrow m_{Al}=0,2.27=5,4\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{5,4}{13,4}=40,3\%\\\%m_{CuO}=100\%-40,3\%=59,7\%\end{matrix}\right.\\ n_{CuO}=\dfrac{13,4-5,4}{80}=0,1\left(mol\right)\)
PTHH:
2Al + 6H2SO4 ---> Al2(SO4)3 + 3SO2 + 6H2O
0,2 0,6 0,1 0,3
CuO + H2SO4 ---> CuSO4 + H2O
0,1 0,1 0,1
\(V_{SO_2}=0,3.22,4=6,72\left(l\right)\)
Mặc định C% H2SO4 là 98% nhé
\(m_{ddH_2SO_4}=\dfrac{98.\left(0,1+0,6\right)}{98\%}=70\left(g\right)\\ m_{dd\left(sau.pư\right)}=70-64.0,3+13,4=64,2\left(g\right)\)
\(\rightarrow\left\{{}\begin{matrix}C\%_{Al_2\left(SO_4\right)_3}=\dfrac{0,1.342}{64,2}=53,27\%\\C\%_{CuSO_4}=\dfrac{0,1.160}{64,2}=24,92\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
a)\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2 0,3
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(m_{Al}=0,2\cdot27=5,4g\)
\(\%m_{Al}=\dfrac{5,4}{13,4}\cdot1005=40,3\%\Rightarrow\%m_{CuO}=59,7\%\)
Câu b có thiếu dữ kiện đề bài không nhỉ
Đúng 3
Bình luận (0)
Hòa tan 50,54 gam hỗn hợp X gồm (Fe, Al) trong dung dịch
H
2
S
O
4
loãng dư thu được V lít khí
H
2
(đktc) và dung dịch A, cô cạn dung dịch A thu được 178,22 gam hỗn hợp muối. Giá trị của V là A. 30,240 B. 29,568 C. 29,792 D. 27,328
Đọc tiếp
Hòa tan 50,54 gam hỗn hợp X gồm (Fe, Al) trong dung dịch H 2 S O 4 loãng dư thu được V lít khí H 2 (đktc) và dung dịch A, cô cạn dung dịch A thu được 178,22 gam hỗn hợp muối. Giá trị của V là
A. 30,240
B. 29,568
C. 29,792
D. 27,328
Chọn C
Gọi số mol của Fe và Al lần lượt là x và y mol

Muối trong dung dịch A gồm x mol F e S O 4 và 0,5y mol A l 2 ( S O 4 ) 3

Đúng 0
Bình luận (0)
Nung nóng hỗn hợp X gồm Al và Fe2O3 (không có không khí) đến khi phản ứng hoàn toàn thu được hỗn hợp rắn Y. Cho Y vào dung dịch NaOH dư thì có 3,36 lít khí H2 (ở đktc) thoát ra và thu được 16,8 gam phần không tan Z. Mặt khác nếu hòa tan hết hỗn hợp Y bằng dung dịch chứa hỗn hợp HCl 1M và H2SO4 0,5M thì cần V lít. Giá trị của V là A. 1,0. B. 0,9. C. 1,5. D. 1,2.
Đọc tiếp
Nung nóng hỗn hợp X gồm Al và Fe2O3 (không có không khí) đến khi phản ứng hoàn toàn thu được hỗn hợp rắn Y. Cho Y vào dung dịch NaOH dư thì có 3,36 lít khí H2 (ở đktc) thoát ra và thu được 16,8 gam phần không tan Z. Mặt khác nếu hòa tan hết hỗn hợp Y bằng dung dịch chứa hỗn hợp HCl 1M và H2SO4 0,5M thì cần V lít. Giá trị của V là
A. 1,0.
B. 0,9.
C. 1,5.
D. 1,2.
Giải thích:
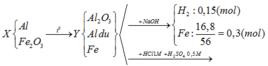
BT e: nAl dư = 2/3 nH2 = 2/3. 0,15 = 0,1 (mol)
BTNT: Fe => nFe2O3 = ½ nFe = 0,15 (mol)
Phản ứng xảy ra hoàn toàn, Al dư sau phản ứng ( vì Y + NaOH có khí H2 bay ra), do đó Fe2O3 phản ứng hết
Fe2O3 + 2Al Al2O3 + 2Fe
0,15 → 0,3
=> nAl ban đầu = 0,3 + 0,1 = 0,4 (mol)
nHCl = V (mol) ; nH2SO4 = 0,5V (mol)
Bảo toàn điện tích khi cho Y tác dụng với hh axit
=> 2nFe2+ + 3nAl3+ = nCl- + 2nSO42-
=> 2.0,3 + 3. 0,4 = V + 2. 0,5V
=> V = 0,9 (lít)
Đáp án B
Đúng 0
Bình luận (0)


















