gọi caxi là Ca
gọi sắt là Fe
vậy
Ca+Fe = gì
gốc muối là gì? nhóm muối là gì?tại sao ta lại ghi sắt(II) sunfua mà ko phải fe và số II có ý nghĩa gì?
+) Gốc muối còn gọi là gốc axit (VD: SO42-, NO3-, PO43-....)
+) Nhóm muối chia làm 2 loại: Muối axit và muối trung hòa
+) Sắt (II) Sunfua là cách đọc tên của FeS trong đó II là hóa trị của Sắt trong hợp chất, và được "quy ước" viết bằng số La Mã
*Có gì không hiểu thì bạn cứ hỏi :3
Cho sắt tác dụng với oxygen tạo ra oxit sắt theo sơ đồ
Fe + O² -> Fe³O⁴
a)Tính hiệu suất của phản ứng khi đốt cháy 11kg Fe .biết lượng oxit sắt sau phản ứng là 200kg
b)Biết kg oxit sắt thu được sau phản ứng là 23,2kg;hiệu suất đạt 85%,hãy tính kg sắt đã tham gia phản ứng giúp vs ạ
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
a, \(n_{Fe}=\dfrac{11}{56}\left(kmol\right)\)
Theo PT: \(n_{Fe_3O_4\left(LT\right)}=\dfrac{1}{3}n_{Fe}=\dfrac{11}{168}\left(kmol\right)\)
\(\Rightarrow m_{Fe_3O_4\left(LT\right)}=\dfrac{11}{168}.232=\dfrac{319}{21}\left(kg\right)\) > mFe3O4 (TT) = 200 (kg)
→ vô lý
Bạn xem lại đề phần a nhé.
b, \(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(kmol\right)\)
Theo PT: \(n_{Fe\left(LT\right)}=3n_{Fe_3O_4}=0,3\left(kmol\right)\)
\(\Rightarrow m_{Fe\left(LT\right)}=0,3.56=16,8\left(kg\right)\)
Mà: H = 85%
\(\Rightarrow m_{Fe\left(TT\right)}=\dfrac{16,8}{85\%}=\dfrac{336}{17}\left(kg\right)\)
H2SO4,FE(NO3)2 được gọi là gì thuộc phân loại nào?
\(H_2SO_4\) là axit (axit sunfuric)
\(FE\left(NO_3\right)_2\) là muối trung hòa ( sắt (||) nitrat)
H2SO4H2SO4 là axit (axit sunfuric)
FE(NO3)2FE(NO3)2 là muối trung hòa ( sắt (||) nitrat)
Thực hiện các thí nghiệm sau: Cho Fe vào dung dịch HCl ; Đốt dây sắt trong khí clo; cho Fe dư vào dd HNO 3 loãng; cho Fe vào dung dịch AgNO 3 dư; cho Fe vào dd KHSO 4 . Số thí nghiệm tạo ra muối sắt(II) là:
A. 2.
B. 3.
C. 4.
D. 5.
Đáp án B
Có 3 thí nghiệm tạo ra muối sắt(II) là :
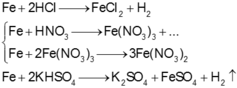
Thực hiện các thí nghiệm sau: Cho Fe vào dung dịch HCl; Đốt dây sắt trong khí clo; cho Fe dư vào dd HNO3 loãng; cho Fe vào dung dịch AgNO3 dư; cho Fe vào dd KHSO4. Số thí nghiệm tạo ra muối sắt(II) là:
A. 2.
B. 3.
C. 4.
D. 5.
Đáp án B.
3.
Cho Fe vào dung dịch HCl;
cho Fe dư vào dd HNO3 loãng;
cho Fe vào dd KHSO4.
Thực hiện các thí nghiệm sau: Cho Fe vào dung dịch HCl; Đốt dây sắt trong khí clo; Cho Fe dư vào dd HNO3 loãng ; Cho Fe vào dung dịch AgNO3 dư ; Cho Fe vào dd KHSO4. Số thí nghiệm tạo ra muối sắt (II) là:
A. 2
B. 3
C. 4
D. 5
Đáp án : B
Cho Fe vào dung dịch HCl; Cho Fe dư vào dd HNO3 loãng ; Cho Fe vào dd KHSO4.
Thực hiện các thí nghiệm sau: Cho Fe vào dung dịch HCl; Đốt dây sắt trong khí clo; cho Fe dư vào dung dịch HNO3 loãng; cho Fe vào dung dịch AgNO3 dư; cho Fe vào dung dịch KHSO4. Số thí nghiệm tạo ra muối sắt(II) là
A. 2.
B. 3.
C. 4.
D. 5.
Đáp án B
Các thí nghiệm là: Cho Fe vào dung dịch HCl; cho Fe dư vào dung dịch HNO3 loãng; cho Fe vào dung dịch KHSO4
Có các cặp kim loại sau tiếp xúc với nhau Al-Fe; Zn-Fe; Sn-Fe; Cu-Fe để lâu trong không khí ẩm. Cặp mà sắt bị ăn mòn là
A. Cặp Sn-Fe và Cu-Fe
B. Chỉ có cặp Sn-Fe
C. Chỉ có cặp Al-Fe
D. Chỉ có cặp Zn-Fe
Đáp án A
Trong cấu tạo 1 cặp điện cực của pin điện, kim loại có tính khử mạnh hơn sẽ bị oxi hóa trước
Fe bị ăn mòn khi Fe có tính khử mạnh hơn kim loại còn lại
=> Sn-Fe, Cu-Fe
Một loại quặng sắt chứa 80% Fe2O3 và 10% SiO2. Hàm lượng các nguyên tử Fe và Si trong quặng này là
A. 56% Fe và 4,7% Si.
B. 54% Fe và 3,7% Si.
C. 53% Fe và 2,7% Si.
D. 52% Fe và 4,7% Si.
Giả sử có 100 gam quặng sắt thì khối lượng Fe2O3 là 80 gam và khối lượng SiO2 là 10 gam
=> \(n_{Fe}=2n_{Fe_2O_3}=2.\dfrac{80}{160}=1\left(mol\right)\\ n_{Si}=n_{SiO_2}=\dfrac{10}{60}=\dfrac{1}{6}\left(mol\right)\)
Ta có :
\(\%Fe=\dfrac{m_{Fe}}{m_{quặng}}.100=\dfrac{1.56}{100}=56\%\\ \%Si=\dfrac{m_{Si}}{m_{quặng}}=\dfrac{\dfrac{1}{6}.28}{100}=4,7\%\)
=> Chọn A