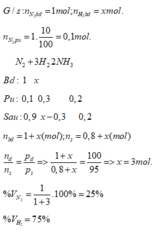Cho phản ứng 2HCl=H2+2Cl. Cho Kp của phản ứng ở 727°C và 1727°C lần lượt là 4.9×10^(-11) và 4.237×10^(-6). Tính Entanpi của phản ứng. Coi entanpi của pư là số đối với nhiệt độ

Những câu hỏi liên quan
Biến thiên entanpi của phản ứng (kí hiệu là Delta H) có thể hiểu đơn giản là nhiệt tỏa ra hoặc thu vào khi phản ứng hóa học xảy ra. Nếu phản ứng tỏa nhiệt thì Delta H có dấu âm và ngược lại, nếu phản ứng thu nhiệt thì Delta H có dấu dương. Khi một phản ứng hóa học xảy ra, các liên kết trong chất phản ứng bị cắt đứt và các liên kết mới được hình thành, tạo nên chất sản phẩm. Để tính Delta H của phản ứng, người ta dựa vào năng lượng các liên kết left(E_{lk}right). E_{lk} là năng lượng cần cung cấp...
Đọc tiếp
Biến thiên entanpi của phản ứng (kí hiệu là \(\Delta H\)) có thể hiểu đơn giản là nhiệt tỏa ra hoặc thu vào khi phản ứng hóa học xảy ra. Nếu phản ứng tỏa nhiệt thì \(\Delta H\) có dấu âm và ngược lại, nếu phản ứng thu nhiệt thì \(\Delta H\) có dấu dương. Khi một phản ứng hóa học xảy ra, các liên kết trong chất phản ứng bị cắt đứt và các liên kết mới được hình thành, tạo nên chất sản phẩm. Để tính \(\Delta H\) của phản ứng, người ta dựa vào năng lượng các liên kết \(\left(E_{lk}\right)\). \(E_{lk}\) là năng lượng cần cung cấp để cắt đứt một liên kết thành các nguyên tử ở thể khí. Năng lượng tỏa ra khi hình thành liên kết đó từ các nguyên tử ở thể khí cũng có giá trị bằng giá trị của \(E_{lk}\) nhưng có dấu ngược lại.
\(E_{lk}\) của một số liên kết được cho trong bảng sau:
| Liên kết | C\(\equiv\)C\(\) | C-C | C-H | H-H |
| \(E_{lk}\left(kJ/mol\right)\) | 839,0 | 343,3 | 418,4 | 432,0 |
Xét phản ứng: \(C_2H_2+2H_2\rightarrow C_2H_6\left(1\right)\)
Dựa vào bảng số liệu trên hãy:
a. Tính năng lượng cần cung cấp để phá vỡ liên kết của các chất tham gia trong phản ứng (1) (Lưu ý hệ số của các chất trong phương trình phản ứng).
b. Tính năng lượng tỏa ra khi hình thành các liên kết trong chất sản phẩm của phản ứng (1)
c. Từ các kết quả trên, xác định \(\Delta H\) của phản ứng (1) và cho biết phản ứng (1) tỏa nhiệt hay thu nhiệt.
\(a.E_r=839,0+2\cdot418,4+2\cdot432,0=2539,8kJ\\ b.E_p=343,3+6\cdot418,4=2853,7kJ\\ c.\Delta_rH^{^{ }0}=2539,8-3197=-313,9kJ\cdot mol^{-1}\\ \Delta H< 0:pư.thu.nhiệt\)
Đúng 1
Bình luận (1)
\(a.E_{reactants}=839,0+2\cdot432,0=1703kJ\\ b.E_{products}=343,3+6\cdot432,0=2935,3kJ\\ c.\Delta_rH^{^o}_{298}=E_r-E_p=1703-2935,3=1232,3kJ\cdot mol^{^{ }-1}.\)
\(\Delta H< 0\) => Phản ứng (1) thu nhiệt
Đúng 0
Bình luận (3)
1, cho biết phản ứng sau:N2(g) + H2O(g)CO2 . Nồng độ các chất lúc cân bằng ở nhiệt độ 430 độ c là [h2] [I2] 0,107M ; [HI] 0,786M. tính hằng số cân bằng Kc tại 430 độ c
2, Iodine bị phân hủy bởi nhiệt theo phản ứng sau :I2(g)2I(g).Ở 727 độ c hằng số cân bằng của phản ứng KC 3,80×10-⁵ .Cho 0,05 mol I2 vào một bình kín dung tích 2,5 lít ở 727°c tính nồng độ của i2 và I ở trạng thái cân bằng
Đọc tiếp
1, cho biết phản ứng sau:N2(g) + H2O(g)<===>CO2 . Nồng độ các chất lúc cân bằng ở nhiệt độ 430 độ c là [h2] =[I2] = 0,107M ; [HI]= 0,786M. tính hằng số cân bằng Kc tại 430 độ c
2, Iodine bị phân hủy bởi nhiệt theo phản ứng sau :I2(g)<==>2I(g).Ở 727 độ c hằng số cân bằng của phản ứng KC = 3,80×10-⁵ .Cho 0,05 mol I2 vào một bình kín dung tích 2,5 lít ở 727°c tính nồng độ của i2 và I ở trạng thái cân bằng
Cho hỗn hợp N2 và H2 vào bình phản ứng có nhiệt độ không đổi. Sau một thời gian phản ứng, áp suất khí trong bình giảm 5% so với áp suất ban đầu. Biết tỉ lệ số mol của nitơ đã phản ứng là 10%. Thành phần phần trăm về số mol của N2 và H2 trong hỗn hợp đầu là: A. 15% và 85% B. 82,35% và 77,5% C. 25% và 75% D. 22,5% và 77,5%
Đọc tiếp
Cho hỗn hợp N2 và H2 vào bình phản ứng có nhiệt độ không đổi. Sau một thời gian phản ứng, áp suất khí trong bình giảm 5% so với áp suất ban đầu. Biết tỉ lệ số mol của nitơ đã phản ứng là 10%. Thành phần phần trăm về số mol của N2 và H2 trong hỗn hợp đầu là:
A. 15% và 85%
B. 82,35% và 77,5%
C. 25% và 75%
D. 22,5% và 77,5%
Đáp án C
Giả sử có 1 mol hỗn hợp đầu. Gọi x và y (mol) lần lượt là số mol của N₂ và H₂ trong 1 mol hỗn hợp đầu
Gọi n₁, P₁ và n₂, P₂ lần lượt là số mol hỗn hợp khí + áp suất trong bình ban đầu và lúc sau
⇒ n₁ = x + y = 1 (1)
Khi nhiệt độ không đổi
⇒ n₁ / n₂ = P₁ / P₂
Áp suất khí trong bình giảm 5% so với áp suất ban đầu ⇒ P₁ / P₂ = 20 / 19
⇒ n₁ / n₂ = 20 / 19 (2)
Số mol của nito đã phản ứng là 10% ⇒ N₂ pứ 0,1x mol
N₂ + 3H₂ → 2NH₃
Trước: x y 0
Pứ 0,1x 0,3x 0,2x
Sau: n N₂ = 0,9x ; n H₂ = y - 0,3x ; n NH₃ = 0,2x
⇒ n₂ = 0,9x + y - 0,3x + 0,2x
⇒ n₂ = 0,8x + y (3)
Từ (1) (2) & (3) ta có:
(x + y) / (0,8x + y) = 20 / 19
⇒ 3x - y = 0 (4)
Giải hệ (1) & (4) cho ta: x = 0,25 mol và y = 0,75 mol
Thành phần phần trăm về số mol của N₂ và H₂ trong hỗn hợp đầu là:
%N₂ = 25% và %H₂ = 75%
Đúng 0
Bình luận (0)
Cho hỗn hợp N2 và H2 vào bình phản ứng có nhiệt độ không đổi. Sau một thời gian phản ứng, áp suất khí trong bình giảm 5% so với áp suất ban đầu. Biết tỉ lệ số mol của nitơ đã phản ứng là 10%. Thành phần phần trăm về số mol của N2 và H2 trong hỗn hợp đầu là: A. 15% và 85% B. 82,35% và 77,5% C. 25% và 75% D. 22,5% và 77,5%.
Đọc tiếp
Cho hỗn hợp N2 và H2 vào bình phản ứng có nhiệt độ không đổi. Sau một thời gian phản ứng, áp suất khí trong bình giảm 5% so với áp suất ban đầu. Biết tỉ lệ số mol của nitơ đã phản ứng là 10%. Thành phần phần trăm về số mol của N2 và H2 trong hỗn hợp đầu là:
A. 15% và 85%
B. 82,35% và 77,5%
C. 25% và 75%
D. 22,5% và 77,5%.
Hóa lý
Nghiên cứu phản ứng C + 2H2 = CH4. Người ta xác định được hằng số cân bằng như sau:
Ở 700 độ C, Kp = 0,915
Ở 750 độ C, Kp = 0,1175
Tính hiệu ứng nhiệt của phản ứng trong khoảng nhiệt độ trên và so sánh với giá trị chính xác hơn thu được bằng thực nghiệm là -89,663 kJ/mol.
Áp dụng công thức:
ln(KT2/KT1) = -\(\triangle\)H/R[1/T2 - 1/T1]
Như vậy: deltaH = RT1T2.ln(KT2/KT1)/(T2-T1)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cho các số liệu động học của một số phản ứng sau ở 298K và 1atm.
2NH3 + 3N2O ---> 4N2 + 3H2O; delta H1 = -1011 kJ
N2O + 3H2 ---> N2H4 + H2O; delta H2 = -317 kJ
2NH3 + 1/2 O2 ---> N2H4 + H2O; delta H3 = -143 kJ
H2 + 1/2 O2 ---> H2O; delta H4 = -286 kJ
Tính entanpi (nhiệt tạo thành) của N2H4 và N2O.
Iodine bị phân hủy bởi nhiệt theo phản ứng sau: I2 (g) 2I (g) Ở 727oC hằng số cân bằng của phản ứng KC = 3,80.10-5 . Cho 0,05 mol I2 vào một bình kín dung tích 2,5 lít ở o 727 C. Tính nồng độ của I2 và I ở trạng thái cân bằng
CM(I2)=0.02M
gọi nồng độ iot chuyển hóa là x
I2(k) <=> 2I(k)
pư: x 2x
cb: 0.02-x 2x
Ta có: (2x)^2/ 0.02-x = 3,80*10^-5
=> x=4,311*10^-4
=> [I2] = 0.02-4,311*10^-4=0,019M
=>[I] = 9,5*10^-3(M)
Đúng 0
Bình luận (0)
Cho các chất sau: 1. Ở thể rắn trong điều kiện thường. 2. Tan trong nước. 3. phản ứng với Cu(OH)2 ở nhiệt độ thường. 4. phản ứng với dung dịch AgNO3/NH3. 5. phản ứng với H2. 6. phản ứng với nước brom. 7. phản ứng vói màu với dung dịch iot. 8. phản ứng thủy phân. Trong các tính chất này, người ta thấy glucozơ có X tính chất, fructozơ có y tính chất và saccarozơ có Z tính chất. Giá trị của X, Y và Z theo thứ tự là A. X 5, Y 4, Z 4 B. X 6, Y 6, Z 4 C. X 6, Y 5, Z 4 D. X 6, Y 6, Z 5
Đọc tiếp
Cho các chất sau:
1. Ở thể rắn trong điều kiện thường.
2. Tan trong nước.
3. phản ứng với Cu(OH)2 ở nhiệt độ thường.
4. phản ứng với dung dịch AgNO3/NH3.
5. phản ứng với H2.
6. phản ứng với nước brom.
7. phản ứng vói màu với dung dịch iot.
8. phản ứng thủy phân.
Trong các tính chất này, người ta thấy glucozơ có X tính chất, fructozơ có y tính chất và saccarozơ có Z tính chất. Giá trị của X, Y và Z theo thứ tự là
A. X = 5, Y = 4, Z = 4
B. X = 6, Y = 6, Z = 4
C. X = 6, Y = 5, Z = 4
D. X = 6, Y = 6, Z = 5
Cho 10 lít hỗn hợp khí CH4 và C2H2 tác dụng với 10 lít H2 (Ni, to). Sau khi phản ứng xảy ra hoàn toàn thu được 16 lít hỗn hợp khí (các khí đều đo ở cùng điều kiện nhiệt độ áp suất). Thể tích của CH4 và C2H2 trước phản ứng là A. 2 lít và 8 lít. B. 3 lít và 7 lít. C. 8 lít và 2 lít. D. 2,5 lít và 7,5 lít
Đọc tiếp
Cho 10 lít hỗn hợp khí CH4 và C2H2 tác dụng với 10 lít H2 (Ni, to). Sau khi phản ứng xảy ra hoàn toàn thu được 16 lít hỗn hợp khí (các khí đều đo ở cùng điều kiện nhiệt độ áp suất). Thể tích của CH4 và C2H2 trước phản ứng là
A. 2 lít và 8 lít.
B. 3 lít và 7 lít.
C. 8 lít và 2 lít.
D. 2,5 lít và 7,5 lít
Đáp án : C
Ta có Cùng điều kiện -> Quy số lít về số mol.n(hh ban đầu) = 20 mol; n(hh sau) = 16 lít
=> H2 phản ứng mất 4 lít => C2H2 có 2 lít và CH4 có 8 lít
Đúng 0
Bình luận (0)