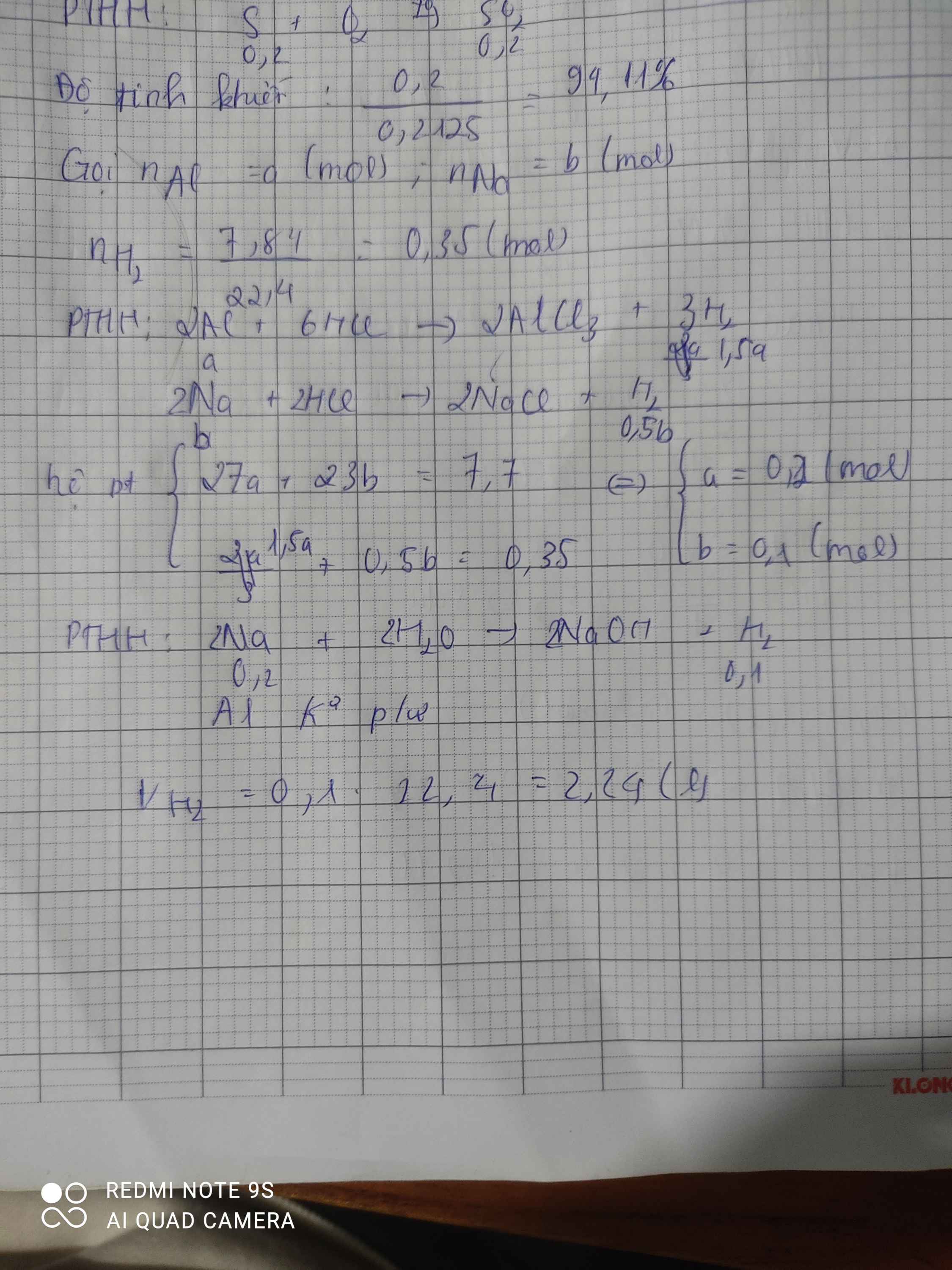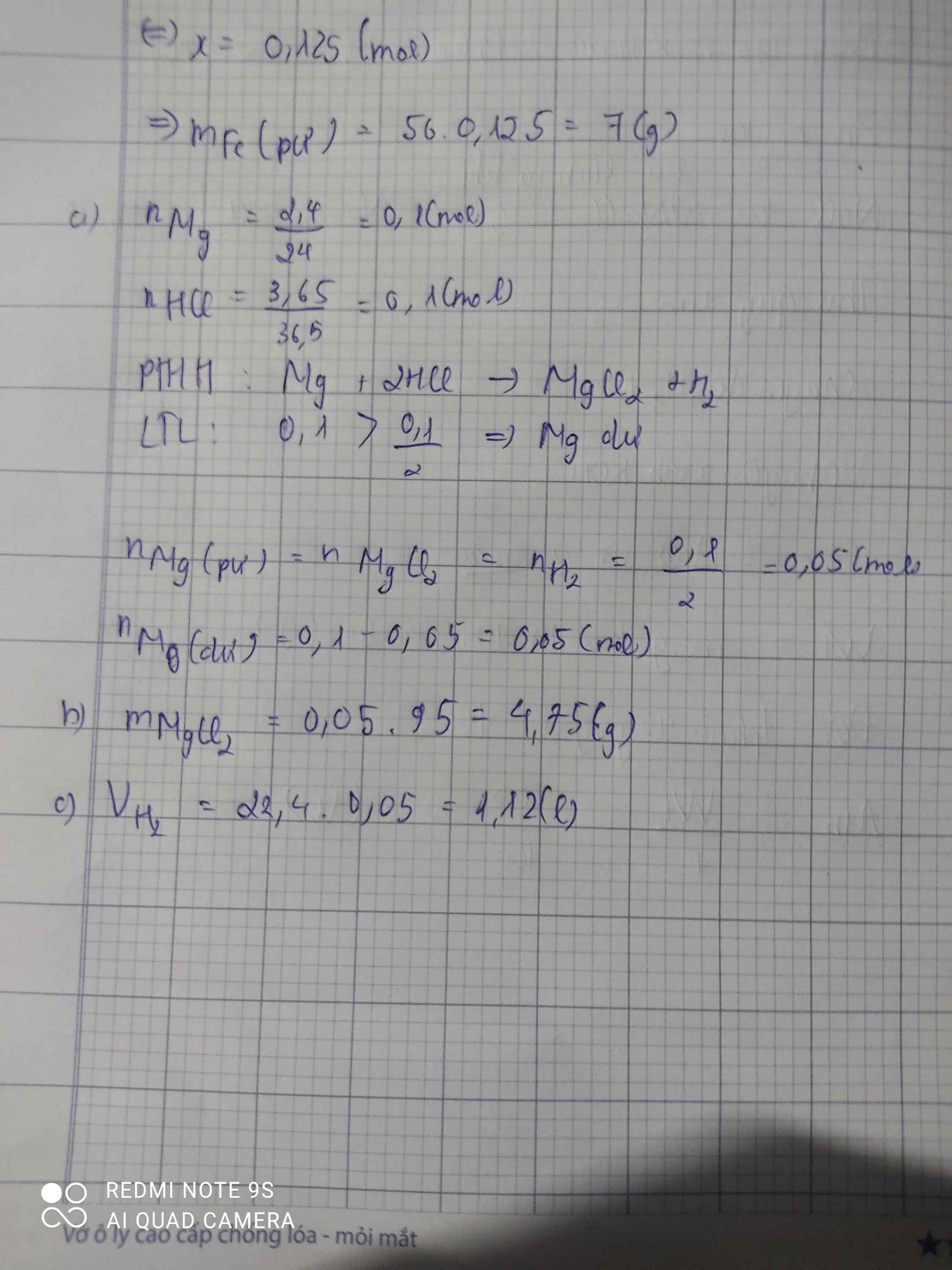Tính thể tích khí H2 ở đktc . khi cho 0.5 mol Al vào dd axit HCl dư

Những câu hỏi liên quan
: Cho m (g) Mg, Al vào 250 ml dd X chứa hỗn hợp HCl 1M và H2SO4 0,5M thu được 5,32 lít khí H2 ( ở đktc) và dd Y ( Coi thể tích dd không thay đổi).
a. Trong dd Y axit dư hay hết?
b. Tính giá trị m?
c. Cô cạn dd Y thu được a(g) muối. Tính a?
Bài 10. Cho 10,8 gam hỗn hợp gồm Mg và Al vào dung dịch axit clohiđric (HCl) dư. Tính thể tích khí H2 sinh ra ở đktc. Biết rằng các phản ứng xảy ra hoàn toàn.
Hòa tan hoàn toàn 7,7g hỗn hợp gồm hai kim loại Al và Na bằng dung dịch HCl dư thấy thoát ra 7,84 lít khí H2 (ở đktc). Tính thể tích khí H2 thu được khi cho hỗn hợp trên vào lượng nước dư
Cho một đinh sắt nặng 28 gam vào dd axit clohiđric HCl (dư) thu được sắt(II) clorua FeCl2 và khí hiđro.
a/ Viết PTHH.
b/ Tính khối lượng muối sắt(II) clorua thu được.
c/ Tính thể tích khí H2 thoát ra ở đktc .Một quả bóng có thể tích tối đa là 10 lít, hỏi quả bóng có chứa được hết lượng H2 thoát ra không?
a. PTHH : Fe + HCl -> FeCl2 + H2
b) \(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\)
\(n_{FeCl_2}=\dfrac{0,5}{2}=0,25\left(mol\right)\\ m_{FeCl_2}=0,25.127=31,75\left(g\right)\)
c) \(n_{H_2}=\dfrac{0,5}{1}=0,5\left(mol\right)\\ V_{H_2}=0,5.22,4=11,2\left(l\right)\)
Mà thể tích tối đa là 10 l -> quả bóng k chứa được hết lượng H2 thoát ra ngoài
Đúng 4
Bình luận (0)
Fe+2HCl->FeCl2+H2
0,5------------0,5-----0,5
=>n Fe=28\56=0,5 mol
=>m FeCl2=0,5.127=63,5g
=>VH2=0,5.22,4=11,2l
bóng 10l ko chứa hết đc nhé thừa 1,2l
Đúng 4
Bình luận (0)
Bài 8: Cho 6 gam Magie vào bình chứa dd Axit clohiđric HCl thu được Magieclorua và khí hiđro
a/ Tính khối lượng MgCl2 thu được
b/ Tính thể tích Hidrô thu được ở đktc ?
c/ Lấy lượng H2 trên dẫn vào ống nghiệm có chứa 0,3 mol PbO đã nung nóng tới nhiệt độ thích hợp.Tính khối lượng chất rắn thu được sau phản ứng?
a,b, \(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\)
PTHH: Mg + 2HCl ---> MgCl2 + H2
0,25 0,25 0,25
\(\rightarrow\left\{{}\begin{matrix}m_{MgCl_2}=0,25.95=23.75\left(g\right)\\V_{H_2}=0,25.22,4=5,6\left(l\right)\end{matrix}\right.\)
c, PTHH: PbO + H2 --to--> Pb + H2O
LTL: \(0,3>0,25\rightarrow\) PbO dư
\(n_{PbO\left(pư\right)}=n_{Pb}=n_{H_2}=0,25\left(mol\right)\\ \rightarrow m_{chất.rắn}=\left(0,3-0,25\right).233+217.0,25=65,9\left(g\right)\)
Đúng 2
Bình luận (2)
nMg = 6 : 24 = 0,25 (mol)
pthh : Mg + 2HCl -> MgCl2 + H2
0,25 0,25 0,25
=> mMgCl2 = 0,25 . 95 = 23,75 (g)
=> VH2 = 0,25 . 22,4 = 5,6 (L)
pthh : PbO + H2 -t--> Pb + H2O
LTL : \(\dfrac{0,3}{1}\) > \(\dfrac{0,25}{1}\)
=> PbO dư
theo pthh : nPb = nH2 = 0,25 (mol)
=> mPb = 0,25 . 201 = 50,25 (G)
Đúng 0
Bình luận (1)
giải giúp mình với mọi người ơi !
cho 2,4 g Magie vào 3,65 g axit clohiđric ( HCl ) thu được magie clorua ( MgCl2 ) và khí hiđro.
a) Magie hay axit dư? Dư bao nhiêu mol?
b) tính khối lượng MgCl ?
c) tính thể tích H2 (ĐKTC)
\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right);n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\\ a,Mg+2HCl\rightarrow MgCl_2+H_2\\ Vì:\dfrac{0,1}{2}< \dfrac{0,1}{1}\\ \Rightarrow Mgdư\\ \Rightarrow n_{Mg\left(p.ứ\right)}=n_{MgCl_2}=n_{H_2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ n_{Mg\left(dư\right)}=0,1-0,05=0,05\left(mol\right)\\ \Rightarrow m_{Mg\left(dư\right)}=0,05.24=1,2\left(g\right)\\ b,m_{MgCl_2}=95.0,05=4,75\left(g\right)\\ c,V_{H_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\)
Đúng 2
Bình luận (1)
a. \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
\(n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\)
PTHH : Mg + 2HCl -> MgCl2 + H2
0,05 0,1 0,05 0,05
Xét tỉ lệ : \(\dfrac{0,1}{1}>\dfrac{0,1}{2}\) => HCl đủ , Mg dư
\(n_{Mg\left(dư\right)}=0,1-0,05=0,05\left(mol\right)\)
b. \(m_{MgCl_2}=0,05.95=4,75\left(g\right)\)
c. \(V_{H_2}=0,05.22,4=1,12\left(l\right)\)
Đúng 0
Bình luận (0)
Cho 4.8 gam kim loại magie vào 200ml dd axit clohiric (hcl) sau phản ứng thu được magie clorua(MgCl2) và khí hidro a) tính thể tích khí video thu được ở đktc b) tính nồng độ mol dd HCL? c) nếu trung hòa dd HCL trên bằng dd KOH 5.6% (D= 1.045g/ml).Tính thể tích dd KOH cần dùng
Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
a, \(n_{H_2}=n_{Mg}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, \(n_{HCl}=2n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,4}{0,2}=2\left(M\right)\)
c, PT: \(HCl+KOH\rightarrow KCl+H_2O\)
Theo PT: \(n_{KOH}=n_{HCl}=0,4\left(mol\right)\)
\(\Rightarrow m_{ddKOH}=\dfrac{0,4.56}{5,6\%}=400\left(g\right)\)
\(\Rightarrow V_{ddKOH}=\dfrac{400}{1,045}\approx382,78\left(ml\right)\)
Đúng 2
Bình luận (0)
Cho một đinh sắt nặng 28 gam vào dd axit clohiđric HCl (dư) thu được sắt(II) clorua FeCl2 và khí hiđro.
a/ Viết PTHH.
b/ Tính khối lượng muối sắt(II) clorua thu được.
c/ Tính thể tích khí H2 thoát ra ở đktc. Một quả bóng Người ta đốt cháy 4,8 gam kim loại magie trong không khí (chứa oxi), sau phản ứng thu được chất rắn màu trắng là magie oxit MgO.
\(n_{Fe}=\dfrac{28}{56}=0,5mol\)
a, PTHH : \(Fe + 2HCl-> FECl_2+ H_2↑\)
0,5 0,5 0,5 (mol)
b/. Theo phương trình, ta có:
\(n_{FeCl_2}=n_{Fe}=0,5 mol\)
\(m_{FeCl_2}=0,5.127=63,5g\)
c, Thông cảm không biết làm
Đúng 2
Bình luận (6)
\(a,PTHH\left(1\right):Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(b,n_{Fe}=\dfrac{m}{M}=\dfrac{28}{56}=0,5\left(mol\right)\\ Theo.PTHH\left(1\right):n_{FeCl_2}=n_{Fe}=0,5\left(mol\right)\\ m_{FeCl_2}=n.M=0,5.91,5=45,75\left(g\right)\)
\(c,PTHH\left(2\right):2Mg+O_2\underrightarrow{t^o}2MgO\\ n_{Mg}=\dfrac{m}{M}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ Theo.PTHH\left(2\right):n_{O_2}=2.n_{Mg}=0,2.2=0,4\left(mol\right)\\ V_{O_2\left(đktc\right)}=n.22,4=0,4.22,4=8,96\left(l\right)\)
(c lỗi đề à có oxi chứ ko có hidro nên mik thay bằng oxi nha)
Đúng 1
Bình luận (1)
5. Cho 5,6 g sắt vào 100 ml dung dịch HCl . Hãy: Tính thể tích khí H2 tạo ra ở đktc? Tính khối lượng muối thu được. Tính nồng độ MOL dd HCl đã dùng. Tính nồng độ MOL các chất sau phản ứng?
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,2\left(mol\right)\\n_{FeCl_2}=0,1\left(mol\right)=n_{H_2}\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,1\cdot22,4=2,24\left(l\right)\\m_{FeCl_2}=0,1\cdot127=12,7\left(g\right)\\C_{M_{FeCl_2}}=\dfrac{0,1}{0,1}=1\left(M\right)\\C_{M_{HCl}}=\dfrac{0,2}{0,1}=2\left(M\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)