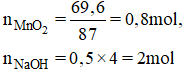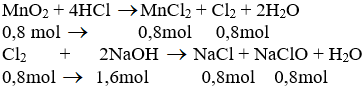Trộn 120ml dung dịch KOH 1m với 80ml dung dịch chứa hỗn hợp HNO3 0,5M và HCL 0,5M thu được dung dịch (A).Tính nồng độ mol của các chất trong dung dịch (A).( Giả thiết thể tích dung dịch thay đổi không đáng kể)

Những câu hỏi liên quan
trộn lẫn 100ml dung dịch KOH 1M với 100ml dung dịch HCl 0,5M thì thu được dung dịch D.
a,Tính nồng độ mol của các ion có trong dung dịch D.
b,Tính thể tích của dung dịch H2SO4 1M đủ để trung hoà hoàn toàn dung dịch D.
c,Tính pH của dung dịch D
trộn lẫn 100ml dung dịch KOH 1M với 100ml dung dịch HCl 0,5M thì thu được dung dịch D.
a,Tính nồng độ mol của các ion có trong dung dịch D.
b,Tính thể tích của dung dịch H2SO4 1M đủ để trung hoà hoàn toàn dung dịch D.
c,Tính pH của dung dịch D
[K+]=[Cl-]=0,25M
[KOH dư]=0,25M
b) 2KCl + H2SO4 ----------->K2SO4 + 2HCl
0,05(mol)---->0,025(mol)
=>vH2SO4=\(\frac{0,025}{1}\)=0,025(lít)
c)pH=-log(0,25)=0,602
(câu c mình không chắc chắn lắm nha bạn!!!)
Đúng 0
Bình luận (1)
trộn 30ml dung dịch có chứa CaCl2 0,5M với 70ml dung dịch có chứa AgNO3 1M thu được m gam kết tủa và 100ml dung dịch A . TÍNH m và nồng độ mol các chất có trong dung dịch A
30ml = 0,03l
70ml = 0,07l
\(n_{CaCl2}=0,5.0,03=0,015\left(mol\right)\)
\(n_{AgNO3}=1.0,07=0,07\left(mol\right)\)
Pt : \(CaCl_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgCl|\)
1 2 1 2
0,015 0,07 0,015 0,03
Lập tỉ số so sánh : \(\dfrac{0,015}{1}< \dfrac{0,07}{2}\)
⇒ CaCl2 phản ứng hết , AgNO3 dư
⇒ Tính toán dựa vào số mol của CaCl2
\(n_{AgCl}=\dfrac{0,015.2}{1}=0,03\left(mol\right)\)
⇒ \(m_{AgCl}=0,03.143,5=4,305\left(g\right)\)
\(n_{Ca\left(NO3\right)2}=\dfrac{0,03.1}{2}=0,015\left(mol\right)\)
\(n_{AgNO3\left(dư\right)}=0,07-\left(0,015.2\right)=0,04\left(mol\right)\)
Sau phản ứng :
\(V_{dd}=0,03+0,07=0,1\left(l\right)\)
\(C_{M_{Ca\left(NO3\right)2}}=\dfrac{0,015}{0,1}=0,15\left(M\right)\)
\(C_{M_{AgNO3\left(dư\right)}}=\dfrac{0,04}{0,1}=0,4\left(M\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (1)
Bài 1: Trộn 300ml dung dịch NaOH 1,5M với 400ml dung dịch NaOH 2,5M. Tính nồng độ mol của dung dịch thu được?
Bài 5: Cần lấy bao nhiêu lit dd HCl 0,2M để khi trộn với dd HCl 0,8M thì thu được 2lit dd HCl 0,5M? Giả sử không có sự thay đổi thể tích khi trộn.
B4:
nNaOH = 0,3 . 1,5 + 0,4 . 2,5 = 1,45 (mol)
VddNaOH = 0,3 + 0,4 = 0,7 (l)
CMddNaOH = 1,45/0,7 = 2,07M
B5:
nHCl (sau khi pha) = 0,5 . 2 = 1 (mol)
Gọi VHCl (0,2) = x (l); VHCl (0,8) = y (l)
x + y = 2 (1)
nHCl (0,2) = 0,2x (mol)
nHCl (0,8) = 0,8y (mol)
=> 0,2x + 0,8y = 1 (2)
(1)(2) => x = y = 1 (l)
Đúng 1
Bình luận (0)
Trộn 100ml dung dịch Ba(OH)2 0,5M với 100 ml dung dịch KOH 0,5M thu được dung dịch A. Tính nồng độ mol/l của ion OH- trong dung dịch?
A. 0,65
B. 0,75
C. 0,5
D.1,5
Đáp án B
[OH-]= (0,5.2.0,1+0,1.0,5)/0,2= 0,75M
Đúng 0
Bình luận (0)
trộn lẫn 80ml dung dịch KOH 0,45M với 35ml dung dịch H2SO4 0,8M thì thu được dung dịch D
a) tính nồng độ mol của các chất có trong dung dịch D
b) tính thể tích dung dịch BaCl2 1,2M cần để tác dụng hết với các chất trong dung dịch D
Xem thêm câu trả lời
Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc dư thu được một lượng khí X. Dẫn khí X vào 500ml dung dịch NaOH 4M thu được dung dịch A. Tính nồng độ mol của các chất trong dung dịch A. Giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
a) Phương trình hóa học của phản ứng:
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 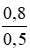
CM (NaOH)dư = 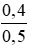
tích cho mình nha![]()
Đúng 2
Bình luận (0)
Trộn lẫn 100ml dung dịch KOH 1m với 100ml dung dịch HCL 0,5 M thì thu được dung dịch D a) tính nồng độ mol của các ion có trong dung dịch D b) tính thể tích dung dịch H2SO4 1m đủ để trung hòa hoàn toàn dung dịch D
\(n_{KOH}=0.1\cdot1=0.1\left(mol\right)\)
\(n_{HCl}=0.1\cdot0.5=0.05\left(mol\right)\)
\(KOH+HCl\rightarrow KCl+H_2O\)
\(0.05.......0.05.......0.05\)
Dung dịch D : 0.05 (mol) KOH , 0.05 (mol) KCl
\(\left[K^+\right]=\dfrac{0.05+0.05}{0.1+0.1}=0.5\left(M\right)\)
\(\left[Cl^-\right]=\dfrac{0.05}{0.2}=0.25\left(M\right)\)
\(\left[OH^-\right]=\dfrac{0.05}{0.2}=0.25\left(M\right)\)
\(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
\(0.05.........0.025\)
\(V_{dd_{H_2SO_4}}=\dfrac{0.025}{1}=0.025\left(l\right)\)
Đúng 2
Bình luận (0)
Trộn 300ml dung dịch H2S04 0,5M với 200ml dung dich KOH 1M thu được dung dịch A
a) tính nồng độ mol/l của các ion trong dung dịch A
b) Tính thể tích dung dịch NaOH 0,5M cần dùng để trung hòa dung dịch A
a, Ta có: \(n_{H_2SO_4}=0,3.0,5=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{H^+}=2n_{H_2SO_4}=0,3\left(mol\right)\\n_{SO_4^{2-}}=n_{H_2SO_4}=0,15\left(mol\right)\end{matrix}\right.\)
\(n_{K^+}=n_{OH^-}=n_{KOH}=0,2.1=0,2\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
0,3 ___ 0,2 __________ (mol)
\(\Rightarrow n_{H^+\left(dư\right)}=0,1\left(mol\right)\)
⇒ Dung dịch A gồm: H+; SO42- và K+
\(\Rightarrow\left\{{}\begin{matrix}\left[H^+\right]=\frac{0,1}{0,5}=0,2M\\\left[SO_4^{2-}\right]=\frac{0,15}{0,5}=0,3M\\\left[K^+\right]=\frac{0,2}{0,5}=0,4M\end{matrix}\right.\)
b, \(H^++OH^-\rightarrow H_2O\)
__0,1 → 0,1 ___________ (mol)
\(\Rightarrow n_{NaOH}=n_{OH^-}=0,1\left(mol\right)\)
\(\Rightarrow V_{NaOH}=\frac{0,1}{0,5}=0,2\left(l\right)\)
Bạn tham khảo nhé!