Điều chế trong hóa học là gì vậy?

Những câu hỏi liên quan
Việt phương trình hóa học điều chế hidro, điều chế oxi trong phong thí nghiệm?
điều chế hidro
Fe+2HCl->FeCl2+H2
2Al+3H2SO4->Al2(SO4)3+3H2
Điều chế O2
2KMnO4-to>K2MnO4+MnO2+O2
2KClO3-to>2KCl+3O2
Đúng 1
Bình luận (0)
Thực hiện phản ứng điều chế tơ axetat từ xenlulozơ (tỷ lệ mắt xích xenlulozơ triaxetat và xenlulozơ điaxetat trong hỗn hợp là 1 : 1). Biết rằng cứ 162 gam xenlulozơ người ta điều chế được 213,6 gam tơ axetat. Vậy hiệu suất chuyển hóa là A. 70% B. 85% C. 75% D. 80%
Đọc tiếp
Thực hiện phản ứng điều chế tơ axetat từ xenlulozơ (tỷ lệ mắt xích xenlulozơ triaxetat và xenlulozơ điaxetat trong hỗn hợp là 1 : 1). Biết rằng cứ 162 gam xenlulozơ người ta điều chế được 213,6 gam tơ axetat. Vậy hiệu suất chuyển hóa là
A. 70%
B. 85%
C. 75%
D. 80%
Hình vẽ sau mô tả thí nghiệm điều chế Z Phương pháp hóa học điều chế Z là: A. Ca(OH)2(dung dịch) + 2NH4Cl (rắn) ® 2NH3 + CaCl2+ 2H2O. B. 2HCl (dung dịch) + Zn ® ZnCl2 + H2. C. H2SO4 (đặc) + Na2SO4 (rắn) ® SO2 + Na2SO4 + H2O. D. 4HCl (đặc) + MnO2 ® Cl2 + MnCl2 + 2H2O
Đọc tiếp
Hình vẽ sau mô tả thí nghiệm điều chế Z
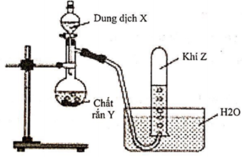
Phương pháp hóa học điều chế Z là:
A. Ca(OH)2(dung dịch) + 2NH4Cl (rắn) ® 2NH3 + CaCl2+ 2H2O.
B. 2HCl (dung dịch) + Zn ® ZnCl2 + H2.
C. H2SO4 (đặc) + Na2SO4 (rắn) ® SO2 + Na2SO4 + H2O.
D. 4HCl (đặc) + MnO2 ® Cl2 + MnCl2 + 2H2O
Hình vẽ mô tả thí nghiệm điều chế khí Z: Phương trình hóa học điều chế khi Z là A. 2HCl(dung dịch) + Zn → H2↑ + ZnCl2. B. H2SO4(đặc) + Na2SO3 (rắn) → SO2↑ + Na2SO4 + H2O. C. Ca(OH)2(dung dịch) + 2NH4Cl(rắn) → 2NH3↑ + CaCl2 + 2H2O. D. 4HCl(đặc) + MnO2 → Cl2↑ + MnCl2 + 2H2O.
Đọc tiếp
Hình vẽ mô tả thí nghiệm điều chế khí Z:

Phương trình hóa học điều chế khi Z là
A. 2HCl(dung dịch) + Zn → H2↑ + ZnCl2.
B. H2SO4(đặc) + Na2SO3 (rắn) → SO2↑ + Na2SO4 + H2O.
C. Ca(OH)2(dung dịch) + 2NH4Cl(rắn) → 2NH3↑ + CaCl2 + 2H2O.
D. 4HCl(đặc) + MnO2 → Cl2↑ + MnCl2 + 2H2O.
Đáp án A
Khi Z là khi H2 vì khí này nhẹ hơn nước và không tan trong nước
→ Có thể thu khí H2 bằng phương pháp đẩy nước
→ Phương trình phản ứng thỏa mãn điều kiện là:
Zn + 2HCl(dung dich) → ZnCl2 + H2↑
Đúng 0
Bình luận (0)
Hình vẽ mô tả thí nghiệm điều chế khí Z: Phương trình hóa học điều chế khi Z là A. 2HCl(dung dịch) + Zn → H2↑ + ZnCl2. B. H2SO4(đặc) + Na2SO3 (rắn) → SO2↑ + Na2SO4 + H2O. C. Ca(OH)2(dung dịch) + 2NH4Cl(rắn) → 2NH3↑ + CaCl2 + 2H2O. D. 4HCl(đặc) + MnO2 → Cl2↑ + MnCl2 + 2H2O.
Đọc tiếp
Hình vẽ mô tả thí nghiệm điều chế khí Z:

Phương trình hóa học điều chế khi Z là
A. 2HCl(dung dịch) + Zn → H2↑ + ZnCl2.
B. H2SO4(đặc) + Na2SO3 (rắn) → SO2↑ + Na2SO4 + H2O.
C. Ca(OH)2(dung dịch) + 2NH4Cl(rắn) → 2NH3↑ + CaCl2 + 2H2O.
D. 4HCl(đặc) + MnO2 → Cl2↑ + MnCl2 + 2H2O.
Đáp án A
Khi Z là khi H2 vì khí này nhẹ hơn nước và không tan trong nước
→ Có thể thu khí H2 bằng phương pháp đẩy nước
→ Phương trình phản ứng thỏa mãn điều kiện là:
Zn + 2HCl(dung dich) → ZnCl2 + H2↑
Đúng 0
Bình luận (0)
Hình vẽ mô tả thí nghiệm điều chế khí Z: Phương trình hóa học điều chế khí Z là A. 2HCl (dung dịch) + Zn
→
H2
↑
+ ZnCl2 B. H2SO4 (đặc) + Na2SO4 (rắn)
→
SO2
↑
+ Na2SO4 + H2O C. Ca(OH)2 (dung dịch) + 2NH4Cl(rắn)
→
2NH3
↑
+ CaCl2 + 2H2O D. 4HCl (đặc) + MnO2
→
Cl2
↑
+ MnCl2 + 2H2O
Đọc tiếp
Hình vẽ mô tả thí nghiệm điều chế khí Z:
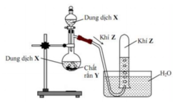
Phương trình hóa học điều chế khí Z là
A. 2HCl (dung dịch) + Zn → H2 ↑ + ZnCl2
B. H2SO4 (đặc) + Na2SO4 (rắn) → SO2 ↑ + Na2SO4 + H2O
C. Ca(OH)2 (dung dịch) + 2NH4Cl(rắn) → 2NH3 ↑ + CaCl2 + 2H2O
D. 4HCl (đặc) + MnO2 → Cl2 ↑ + MnCl2 + 2H2O
Hình vẽ mô tả thí nghiệm điều chế khí Z: Phương trình hóa học điều chế khí Z là A. 2HCl (dung dịch) + Zn
→
H2 + ZnCl2 B. H2SO4 (đặc) + Na2SO4 (rắn)
→
SO2 + Na2SO4 + H2O C. Ca(OH)2 (dung dịch) + 2NH4Cl(rắn)
→
2NH3 + CaCl2 + 2H2O D. 4HCl (đặc) + MnO2
→
Cl2 + MnCl2 + 2H2O
Đọc tiếp
Hình vẽ mô tả thí nghiệm điều chế khí Z:
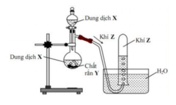
Phương trình hóa học điều chế khí Z là
A. 2HCl (dung dịch) + Zn → H2 + ZnCl2
B. H2SO4 (đặc) + Na2SO4 (rắn) → SO2 + Na2SO4 + H2O
C. Ca(OH)2 (dung dịch) + 2NH4Cl(rắn) → 2NH3 + CaCl2 + 2H2O
D. 4HCl (đặc) + MnO2 → Cl2 + MnCl2 + 2H2O
Khí Z là khí H2 vì khí này nhẹ hơn nước và không tan trong nước
Có thể thu khí H2 bằng phương pháp đẩy nước
Phương trình phản ứng thỏa mãn điều kiện là:
Zn + 2HCl(dung dịch) → ZnCl2 + H2
Đáp án A
Đúng 0
Bình luận (0)
Hình vẽ sau mô tả thí nghiệm điều chế khí Z: Phương trình hóa học điều chế khí Z là
Đọc tiếp
Hình vẽ sau mô tả thí nghiệm điều chế khí Z:
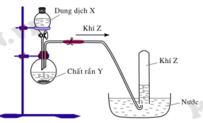
Phương trình hóa học điều chế khí Z là

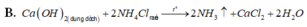
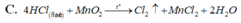
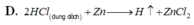
Đáp án D
Khí Z thu bằng cách dời chỗ H2O, nên khí Z không tan trong nước ⇒ Z là H2 (các khí SO2, NH3 và Cl2 tan nhiều trong nước)
Đúng 0
Bình luận (0)
Hình vẽ sau mô tả thí nghiệm điều chế khí Z: Phương trình hóa học điều chế khí Z là A.
H
2
S
O
4
đ
ặ
c
+
N
a
2
S
O
4
r...
Đọc tiếp
Hình vẽ sau mô tả thí nghiệm điều chế khí Z:
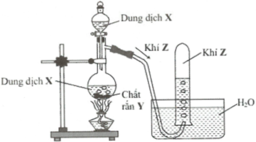
Phương trình hóa học điều chế khí Z là
A. H 2 S O 4 đ ặ c + N a 2 S O 4 r ắ n → S O 2 ↑ + N a 2 S O 4 + H 2 O
B. C a O H 2 d u n g d ị c h + 2 N H 4 C l r ắ n → t 2 N H 3 ↑ + C a C l 2 + 2 H 2 O
C. 4 H C l đ ặ c + M n O 2 → t C l ↑ + M n C l 2 + 2 H 2 O
D. 2 H C l d u n g d ị c h + Z n → Z n C l 2 + H 2
Hình vẽ sau mô tả thí nghiệm điều chế khí Z: Phương trình hóa học điều chế khí Z là
Đọc tiếp
Hình vẽ sau mô tả thí nghiệm điều chế khí Z:
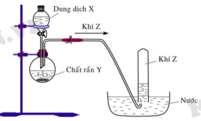
Phương trình hóa học điều chế khí Z là
![]()
![]()
![]()
![]()
Đáp án D
Khí Z thu bằng cách dời chỗ H2O, nên khí Z không tan trong nước ⇒ Z là H2 (các khí SO2, NH3 và Cl2 tan nhiều trong nước)
Đúng 0
Bình luận (0)








