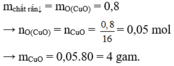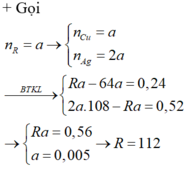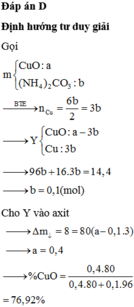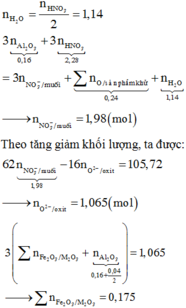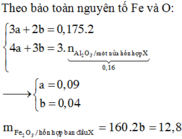Nung 27,2 gam hỗn hợp sắt (III) hidroxit và magie hidroxit đến khi phản ứng hoàn toàn thấy khối lượng chất rắn thu được giảm 7,2 gam so với khối lượng hidroxit ban đầu. Tính khối lượng chất rắn tạo thành và phần trăm khối lượng mỗi hidroxit.

Những câu hỏi liên quan
Cho luồng khí CO (dư) đi qua 9,1 gam hỗn hợp gồm CuO và A l 2 O 3 nung nóng đến khi phản ứng hoàn toàn thấy khối lượng chất rắn giảm 0,8 gam. Khối lượng CuO có trong hỗn hợp ban đầu là
A. 0,8 gam.
B. 8,3 gam.
C. 2,0 gam.
D. 4,0 gam.
Nung 24,2 gam hỗn hợp X gồm sắt II hidroxit và sắt III hidroxit thu được 18,6 gam hỗn hợp Y gồm sắt II oxit và sắt III oxit . Phản ứng xảy ra theo sơ đồ: Bazơ không tan ot oxit + nước Em hãy tính khối lượng mỗi chất trong X và khối lượng mỗi chất trong Y
Cho m gam bột kim loại R hóa trị 2 vào dung dịch CuSO4 dư. Sau phản ứng hoàn toàn, khối lượng chất rắn thu được giảm 0,24 gam so với khối lượng chất rắn ban đầu. Cũng cho m gam bột kim loại trên vào dung dịch AgNO3 dư, đến khi phản ứng hoàn toàn, khối lượng chất rắn thu được tăng 0,52 gam so với khối lượng chất rắn ban đầu. Kim loại R là A. Sn B. Cd C. Zn D. Pb
Đọc tiếp
Cho m gam bột kim loại R hóa trị 2 vào dung dịch CuSO4 dư. Sau phản ứng hoàn toàn, khối lượng chất rắn thu được giảm 0,24 gam so với khối lượng chất rắn ban đầu. Cũng cho m gam bột kim loại trên vào dung dịch AgNO3 dư, đến khi phản ứng hoàn toàn, khối lượng chất rắn thu được tăng 0,52 gam so với khối lượng chất rắn ban đầu. Kim loại R là
A. Sn
B. Cd
C. Zn
D. Pb
Đem nung 6,66g hh X (2 hidroxit của nhôm và kẽm) sau khi phản ứng xảy ra xong thấy khối lượng chất rắn đem nung giảm đi 1,98g. Tính thành phần % khối lượng hh hidroxit?
- PTHH: 2Al(OH)3\(\underrightarrow{t^0}\)Al2O3+3H2O
Zn(OH)2\(\underrightarrow{t^0}\)ZnO+H2O
- Khối lượng chất rắn giảm chính là khối lượng nước tạo thành
\(\rightarrow\)\(n_{H_2O}=\dfrac{m}{M}=\dfrac{1,98}{18}=0,11mol\)
- Gọi số mol Al(OH)3 là x và Zn(OH)2 là y ta có hệ phương trình:
\(\left\{{}\begin{matrix}78x+99y=6,66\\\dfrac{3x}{2}+y=0,11\end{matrix}\right.\)
- Giải ra x=0,06 và y=0,02
- Thành phần phần trăm khối lượng mỗi hidroxit là:
\(\%m_{Al\left(OH\right)_3}=\dfrac{0,06.78.100}{6,66}\simeq70,27\%\)
\(\%m_{Zn\left(OH\right)_2}=100\%-70,27\%=29,73\%\)
Đúng 0
Bình luận (0)
Cho hỗn hợp X gồm CuO và (NH4)2CO3 vào bình kín không có không khí rồi nung đến khi phản ứng hoàn toàn thu được chất rắn Y có khối lượng giảm so với khối lượng X là 14,4 gam. Mặt khác cho Y vào dung dịch H2SO4 loãng dư thu được chất rắn T có khối lượng giảm so với khối lượng của Y là 8 gam. Phần trăm khối lượng của CuO trong X? A. 52,82% B. 28,65% C. 43,13% D. 76,92%
Đọc tiếp
Cho hỗn hợp X gồm CuO và (NH4)2CO3 vào bình kín không có không khí rồi nung đến khi phản ứng hoàn toàn thu được chất rắn Y có khối lượng giảm so với khối lượng X là 14,4 gam. Mặt khác cho Y vào dung dịch H2SO4 loãng dư thu được chất rắn T có khối lượng giảm so với khối lượng của Y là 8 gam. Phần trăm khối lượng của CuO trong X?
A. 52,82%
B. 28,65%
C. 43,13%
D. 76,92%
Cho hỗn hợp X gồm CuO và (NH4)2CO3 vào bình kín không có không khí rồi nung đến khi phản ứng hoàn toàn thu được chất rắn Y có khối lượng giảm so với khối lượng X là 14,4 gam. Mặt khác cho Y vào dung dịch H2SO4 loãng dư thu được chất rắn T có khối lượng giảm so với khối lượng của Y là 8 gam. Phần trăm khối lượng của CuO trong X? A. 52,82% B. 28,65% C. 43,13% D. 76,92%
Đọc tiếp
Cho hỗn hợp X gồm CuO và (NH4)2CO3 vào bình kín không có không khí rồi nung đến khi phản ứng hoàn toàn thu được chất rắn Y có khối lượng giảm so với khối lượng X là 14,4 gam. Mặt khác cho Y vào dung dịch H2SO4 loãng dư thu được chất rắn T có khối lượng giảm so với khối lượng của Y là 8 gam. Phần trăm khối lượng của CuO trong X?
A. 52,82%
B. 28,65%
C. 43,13%
D. 76,92%

| CHÚ Ý |
| + Nhiệt phân (NH4)2CO3 sẽ cho ra NH3. Khí NH3 có thể khử CuO về Cu + Chất rắn Y không tan hoàn toàn trong axit H2SO4 loãng nên có phải chứa hỗn hợp CuO và Cu. |
Đúng 0
Bình luận (0)
Trộn 160 gam dung dịch natri hidroxit 20% với dung dịch đồng (II) nitrat 4% thu được dung dịch X và kết tủa Y. Lọc kết tủa Y , nung kết tủa Y đến khi khối lượng không đổi thu được chất rắn A. a)Tính khối lượng chất rắn A thu được . b)Tính khối lượng dung dịch đồng (II) nitrat 4% phản ứng. c)Tính nồng độ % của dung dịch X.
Đun nóng hỗn hợp Fe3O4, Fe2O3 và 19,44 gam Al trong khí trơ đến khi phản ứng xảy ra hoàn toàn thu được chất rắn X. Chia X làm hai phần bằng nhau. Phần 1 cho vào dung dịch NaOH dư thoát ra 0,06 mol H2. Phần 2 tác dụng vừa đủ với 420 gam dung dịch HNO3 34,2% thu được dung dịch Y chỉ chứa các muối kim loại và 5,376 lít (đktc) hỗn hợp khí Z gồm N2O và NO. Cô cạn dung dịch Y, sau đó lấy chất rắn nung trong chân không tới khối lượng không đổi thấy khối lượng chất rắn giảm 105,72 gam. Khối lượng Fe2O3...
Đọc tiếp
Đun nóng hỗn hợp Fe3O4, Fe2O3 và 19,44 gam Al trong khí trơ đến khi phản ứng xảy ra hoàn toàn thu được chất rắn X. Chia X làm hai phần bằng nhau. Phần 1 cho vào dung dịch NaOH dư thoát ra 0,06 mol H2. Phần 2 tác dụng vừa đủ với 420 gam dung dịch HNO3 34,2% thu được dung dịch Y chỉ chứa các muối kim loại và 5,376 lít (đktc) hỗn hợp khí Z gồm N2O và NO. Cô cạn dung dịch Y, sau đó lấy chất rắn nung trong chân không tới khối lượng không đổi thấy khối lượng chất rắn giảm 105,72 gam. Khối lượng Fe2O3 trong hỗn hợp ban đầu là:
A. 12,8 gam
B. 14,4 gam
C. 11,2 gam
D. 16,0 gam
Cho a gam hỗn hợp A ( gồm Natri hidroxit và Magie hidroxit) vào nước khuấy đều thì thu được đung dịch B và chất rắn C. Lọc chất rắn C đem nung hoàn toàn thu được 6 gam chất rắn D. Trung hòa dung dịch B cần 50 ml dung dịch Axit clohidric 0,4M. Tính a ?
Ta có: \(\left\{{}\begin{matrix}n_{MgO}=\dfrac{6}{40}=0,15\left(mol\right)\\n_{HCl}=0,05\cdot0,4=0,02\left(mol\right)\end{matrix}\right.\)
Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_{Mg\left(OH\right)_2}=n_{MgO}=0,15\left(mol\right)\\n_{NaOH}=n_{NaCl}=n_{HCl}=0,02\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow a=m_{NaOH}+m_{Mg\left(OH\right)_2}=0,02\cdot40+0,15\cdot58=9,5\left(g\right)\)
Đúng 0
Bình luận (0)