cho kim loại đồng kết hợp với axit HCI tạo thành sản phẩm j (mik ko bt là HCI hay HCL nữa ai thấy sai thì sữa dùm mik )

Những câu hỏi liên quan
cho 5,6g kim loại sắt tác dụng hết với dung dịch axit clohidric HCI theo phương trình: Fe + HCI ---> FeCI2 + H2. a) Lập phương trình hoá học của phản ứng trên. b) Tính khối lượng sắt ( II) clorua FeCI2 tạo thành. c) Tính thể tích khí H2 sinh ( ở đktc )
Giúp mình với 🥺🥺🥺
Fe+2HCl->FeCl2+H2
0,1--0,2-----0,1-----0,1
nFe=0,1 mol
=>mFeCl2=0,1.127=12,7g
=>VH2=0,1.22,4=2,24l
Đúng 0
Bình luận (0)
kim loại tác dụng với dung dịch axit hci giải phóng khí hiđro là
là kim loại đứng trước H trong dãy hd hóa học
Đúng 0
Bình luận (0)
Cho 15 gam hợp kim nhôm - magie vào dung dịch HCI thu được 15,68 lít khí H2 ( đktc ) và 2,5 g một chất ko tan . Xác định thành phần % của hợp kim biết Cu không tác dụng với axit HCI
2Al +6 HCl => 2AlCl3 + 3H2
Mg + 2HCl => MgCl2 + H2
Cu không tác dụng HCl => chất rắn không tan là Cu, mCu = 2.5 (g)
nH2 = V/22.4 = 15.68/22.4 = 0.7 (mol)
Đề là: 15g Nhôm và Magie
=> mAl + mMg = 15
Gọi x,y (mol) lần lượt là số mol của Al và Mg
Theo đề bài và phương trình ta có:
27x + 24y = 15, 1.5x + y = 0.7
==> x = 0.2, y = 0.4
mAl = n.M = 0.2 x 27 = 5.4 (g)
mMg = n.M = 0.4 x 24 = 9.6 (g)
mhh Cu,Al,Mg = 17.5 (g)
-----> Tìm % từng kim loại
Đúng 0
Bình luận (0)
Vì Cu không tác dụng với HCl
nên: mCu= 2.5g
Đặt: nAl= x (mol), nMg= y (mol)
2Al + 6HCl --> 2AlCl3 + 3H2
Mg + 2HCl --> MgCl2 + H2
mhh= 27x + 24y= 15 (1)
nH2= 1.5x + y= 15.68/22.4=0.7 (mol) (2)
Giải (1) và (2):
x=0.2
y=0.4
Khối lượng hỗn hợp:
mAl + mMg + mCu= 5.4 + 9.6 +2.5= 17.5 g
%Al= 5.4/17.5*100%= 30.85%
%Mg= 9.6/17.5*100%= 54.85%
%Cu= 100-30.85-54.85=14.3 %
Chúc bạn học tốt <3
Đúng 0
Bình luận (4)
Khi nhân 1 số với 23, Nam đã viết các tích riêng thẳng hàng với nhau thì được kết quả sai là 460. Tìm kết quả đúng.
Mình đang cần gấp ạ
mik ko cần bt đúng hay sai chỉ cần bạn cho mik đáp án mik sẽ tik ạ
vì bạn ấy đã đặt các tích riêng thẳng cột vs nhau nên thực chất bạn ấy đã nhân số đó vs :
2+3=5
thừa số thứ nhất là :
460:5=92
tích đúng là :
92x23=2116
Đúng 3
Bình luận (0)
Xem thêm câu trả lời
Khử hoàn toàn 4,06 gam một oxit kim loại bằng CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ sản phẩm khí sinh ra vào dung dịch Ca(OH)2 dư thấy tạo thành 7 gam kết tủa. Nếu lấy lượng kim loại sinh ra hoà tan hết vào dung dịch HCl thì thu được 1,176 lít H2 (đktc). Công thức của oxit kim loại là A. CuO. B. Al2O3. C. Fe3O4. D. ZnO.
Đọc tiếp
Khử hoàn toàn 4,06 gam một oxit kim loại bằng CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ sản phẩm khí sinh ra vào dung dịch Ca(OH)2 dư thấy tạo thành 7 gam kết tủa. Nếu lấy lượng kim loại sinh ra hoà tan hết vào dung dịch HCl thì thu được 1,176 lít H2 (đktc). Công thức của oxit kim loại là
A. CuO.
B. Al2O3.
C. Fe3O4.
D. ZnO.
Đáp án C
nCO2 = nCaCO3 = 0,07 mol
O + CO → CO2
0,07 ← 0,07
mKL = moxit – mO
= 4,06 – 0,07.16 = 2,94 (g)
Gọi hóa trị của KL khi tác dụng với HCl là n
M → 0,5n H2
0,105/n← 0,0525 (mol)
![]()
![]()
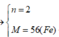
![]()
![]()
Đúng 0
Bình luận (0)
cho 34,25 gam một kim loại loại r thuộc nhóm IIa tác dụng với 200ml dung dịch HCI Thì Thu đc 5.6 lít khí hidro (ở dktc)
A xác định tên R
B tính hiệu độ âm điện, xác định loại liên kết của sảm phẩm muối thu được
a) \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: R + 2HCl --> RCl2 + H2
_____0,25<----------------0,25
=> \(\dfrac{34,25}{0,25}=137\left(Ba\right)\)
b) Muối thu được là BaCl2
Hiệu độ âm điện = 3,16 - 0,89 = 2,27
=> Liên kết ion
Đúng 0
Bình luận (0)
Cho 22,4 gam kim loại sắt tác dụng với 300ml dung dịch axit clohidric (HCI) thu được muối sắt (||)clorua(FeCL²) và khí khí hidro thoát ra A tinh thể tích khí hidro sinh ra (dktc) B tính khối lượng của muối sắc (||) clorua (FeCL²) tạo thành Có tính nồng độ mol của dung dịch axit clorua (HCI) đã phản ứng
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
A. \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
Theo PTHH: \(n_{H_2}=n_{Fe}=0,4\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,4.22,4=8,96\left(l\right)\)
B. Theo PTHH: \(n_{FeCl_2}=n_{Fe}=0,4\left(mol\right)\)
\(m_{FeCl_2}=0,4.127=50,8\left(g\right)\)
C. Nồng độ mol:
\(C_M=\dfrac{0,4}{0,3}=1,3\left(M\right)\)
Đúng 3
Bình luận (0)
Bai 18: Cho 9,2 gam hỗn hợp gồm Cu. Fe tác dụng hoàn toàn với dung dịch HCI (lấy dư). Sau khi phản ứng kết thúc thu được 6,35 gam muối khan.
a) Viết phương trình hóa học.
b) Tính thành phần % khối lượng mỗi kim loại trong hỗn hợp.
a) Fe + 2HCl --> FeCl2 + H2
Cu + HCl -×->
b) nFeCl2 = 6,35/127 = 0,05(mol)
nFe = nFeCl2 = 0,05mol
%Fe = (0,05.56)/9,2 × 100 = 30%
%Cu = 100 - 30 = 70%
Đúng 2
Bình luận (1)
Cho 4.2 g hỗn hợp 2 kim loại Mg và Zn phản ứng hoàn toàn với dung dịch HCI được 2.24 lít H› ở đktc. Khôi lượng muối tạo ra trong dung dịch là ( Biết Mg =24 7n =đ63)
Mg + 2HCl \(\rightarrow\) MgCl2 + H2 ( 1 )
Zn + 2HCl \(\rightarrow\) ZnCl2 + H2 ( 2 )
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(n_{HCl}=0,1.2=0,2mol\)
\(Theo.ĐLBTKL,ta.có:m_{hh}+m_{HCl}=m_{muối}+m_{H_2}\)
\(\Rightarrow m_{muối}=4,2+0,2.36,5-0,1.2=11,3g\)
Đúng 4
Bình luận (0)

























