Nung m gam hỗn hợp 2 KL Zn và Fe trong bột lưu huỳnh dư. Chất rắn thu đc hòa tan hoàn toàn trong 200ml dd H2SO4 loãng thì thu đc 75,66g muối sunfat và 10,752l khí ở đktc
a/ Tính khối lượng m của hỗn hợp 2 KL
b. Tính CM dd H2SO4 cần dùng

Những câu hỏi liên quan
1, Hòa tan hoàn toàn 37,6 gam hỗn hợp Fe và Fe2O3 trong dd H2SO4 loãng, dư thu đc dd X và 2.24 lít khí H2 (ở đktc)a.Viết pt pư xảy rab. Tính % Kl mỗi chất trong hỗn hợp ban đầu2, Hòa tan 14,2 gam hỗn hợp Al,Mg và Cu trong dd H2SO4 loãng dư thu đc đ X, 6,4 gam một chất rắn không tan và 8,96 lít khí H2 (ở đktc)a, viết pt pư b, tính phần trăm kl mỗi chất trong hỗn hợp ban đầu3, cho một dd có chứa 50ml HNO3 1M td vs 342 gam dd Ba(OH)2 5%a, viết pt pư và tính KL muối thu đcb, nếu sau pư cho mẩu quì...
Đọc tiếp
1, Hòa tan hoàn toàn 37,6 gam hỗn hợp Fe và Fe2O3 trong dd H2SO4 loãng, dư thu đc dd X và 2.24 lít khí H2 (ở đktc)
a.Viết pt pư xảy ra
b. Tính % Kl mỗi chất trong hỗn hợp ban đầu
2, Hòa tan 14,2 gam hỗn hợp Al,Mg và Cu trong dd H2SO4 loãng dư thu đc đ X, 6,4 gam một chất rắn không tan và 8,96 lít khí H2 (ở đktc)
a, viết pt pư
b, tính phần trăm kl mỗi chất trong hỗn hợp ban đầu
3, cho một dd có chứa 50ml HNO3 1M td vs 342 gam dd Ba(OH)2 5%
a, viết pt pư và tính KL muối thu đc
b, nếu sau pư cho mẩu quì tím thì giấy quì có màu gì
#giúp mk vs ạ![]()
Bài 1:
PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)=n_{Fe}\)
\(\Rightarrow\%m_{Fe}=\dfrac{0,1\cdot56}{37,6}\cdot100\%\approx14,89\%\)
\(\Rightarrow\%m_{Fe_2O_3}=85,11\%\)
Đúng 2
Bình luận (0)
Bài 3:
PTHH: \(2HNO_3+Ba\left(OH\right)_2\rightarrow Ba\left(NO_3\right)_2+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{HNO_3}=0,05\cdot1=0,05\left(mol\right)\\n_{Ba\left(OH\right)_2}=\dfrac{342\cdot5\%}{171}=0,1\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,05}{2}< \dfrac{0,1}{1}\) \(\Rightarrow\) Axit p/ứ hết, Bazơ còn dư sau p/ứ
\(\Rightarrow\) Dung dịch sau p/ứ làm quỳ tím hóa xanh
Theo PTHH: \(n_{Ba\left(NO_3\right)_2}=\dfrac{1}{2}n_{HNO_3}=0,025\left(mol\right)\) \(\Rightarrow m_{Ba\left(NO_3\right)_2}=0,025\cdot261=6,525\left(g\right)\)
Đúng 1
Bình luận (0)
Bài 2:
Theo đề bài: \(\%m_{Cu}=\dfrac{6,4}{14,2}\cdot100\%\approx45,07\%\)
PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
a_________________________\(\dfrac{3}{2}\)a (mol)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
b_____________________b (mol)
Ta lập được hệ phương trình \(\left\{{}\begin{matrix}27a+24b=14,2-6,4=7,8\\\dfrac{3}{2}a+b=\dfrac{8,96}{22,4}=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2\cdot27}{14,2}\cdot100\%\approx38,03\%\\\%m_{Mg}=100\%-38,03\%-45,07\%=16,9\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Hòa tan 12g hh Fe,Cu trong dd H2SO4 dư (loãng) thu đc 2,24l khí ở đktc. Chất rắn còn lại hòa tan trong H2SO4 98% ( dư 10% về khối lượng ) đc V lít khí A ở đktc
a) Tính % m trong hỗn hợp ban đầu
b) Tính V và mdd H2SO4 đã dùng
a/nH2= 0,1(mol)
Fe + H2SO4 -> FeSO4 + H2
0,1_________________0,1(mol)
=> mFe=0,1.56=5,6(g)
=> %mFe= (5,6/12).100\(\approx\) 46,667%
=> %mCu \(\approx\) 100% - 46,667% \(\approx\) 53,333%
b) mCu= 12-5,6=6,4(g) -> nCu= 0,1(mol)
Cu + 2 H2SO4(đ) -to-> CuSO4 + SO2 + 2 H2O
0,1___0,2__________________0,1(mol)
V=V(SO2,đktc)=0,1.22,4=2,24(l)
mH2SO4(p.ứ)=0,2.98=19,6(g)
=> mH2SO4(bđ)= 19,6 x 100/90 \(\approx21,778\left(g\right)\)
=> mddH2SO4 \(\approx\) (21,778 x 100)/98\(\approx22,222\left(g\right)\)
Đúng 3
Bình luận (0)
Hòa tan 8,8g hỗn hợp gồm bột sắt và bột đồng bằng lượng dư dung dịch H2SO4 loãng thu đc 2,24 lit khí sinh ra (đktc) và chất rắn X
a) Tính % (m) các kim loại có trong hỗn hợp
b) hòa tan hoàn tan chất rắn X bằng H2SO4 đặc, thì thu đc bao nhiu lit khí bay ra (đktc)?
Cu không tác dụng với dung dịch H2SO4 loãng
\(n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,1 0,1
a) \(n_{Fe}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
\(m_{Cu}=8,8-5,6=3,2\left(g\right)\)
0/0Fe = \(\dfrac{5,6.100}{8,8}=63,64\)0/0
0/0Cu = \(\dfrac{3,2.100}{8,8}=36,36\)0/0
b) Có : \(m_{Cu}=3,2\left(g\right)\)
\(n_{Cu}=\dfrac{3,2}{64}=0,05\left(mol\right)\)
Pt : \(Cu+2H_2SO_{4đặc,nóng}\rightarrow CuSO_4+SO_2+2H_2O|\)
1 2 1 1 2
\(n_{SO2}=\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,05.22,4=1,12\left(l\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Hòa tan 8,8g hỗn hợp gồm bột sắt và bột đồng bằng lượng dư dung dịch H2SO4 loãng thu đc 2,24 lit khí sinh ra (đktc) và chất rắn X
a) Tính % (m) các kim loại có trong hỗn hợp
b) hòa tan hoàn tan chất rắn X bằng H2SO4 đặc, thì thu đc bao nhiu lit khí bay ra (đktc)?
a, \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4 → FeSO4 + H2
Mol: 0,1 0,1
\(\%m_{Fe}=\dfrac{0,1.56.100\%}{8,8}=63,64\%;\%m_{Cu}=100-63,64=36,36\%\)
Chất rắn X là Cu (Cu ko tác dụng với H2SO4 loãng)
b,\(n_{Cu}=\dfrac{8,8-5,6}{64}=0,05\left(mol\right)\)
PTHH: Cu + 2H2SO4 (đ) → CuSO4 + SO2 + 2H2O
Mol: 0,05 0,05
\(\Rightarrow V_{SO_2}=0,05.22,4=1,12\left(l\right)\)
Đúng 2
Bình luận (0)
Hòa tan M gam hỗn hợp Zn và Fe trong dd HCl dư thu đc 39g muối và 6,72 lít khí (đktc).
a. Tính % khối lượng từng chất trong hỗn hợp ban đầu.
b. Tính nồng độ phần trăm của 200g dd HCl.
Nung hỗn hợp x gồm fe và s trong điều kiện ko có không khí thu đc hỗn hợp Y . Hòa tan Y trong dd hcl dư thu đc 1,2 gam chất rắn' ko tan và khí Z. dẫn Z qua dd CuSo4 dư thu đc 14,4 g kết tủa.Khối lượng lưu huỳnh trong X?
Xem chi tiết
Khi hòa tan Y vào dd HCl dư thu được chất rắn
=> Chất rắn là lưu huỳnh
mS(dư) = 1,2 (g)
\(n_{CuS}=\dfrac{14,4}{96}=0,15\left(mol\right)\) => nS(Z) = 0,15 (mol)
Bảo toàn S: mS(X) = 1,2 + 0,15.32 = 6 (g)
Đúng 1
Bình luận (0)
Nung nóng 3,72g hỗn hợp bột các kim loại Zn và Fe trong bột S dư. Chất rắn thu được sau phản ứng được hòa tan hoàn toàn bằng dung dịch H2SO4 loãng, nhận thấy có 1,344 lít khí (đktc) thoát ra. Xác định khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Đặt nZn = x mol; nFe = y mol.
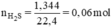
Ta có hệ phương trình: 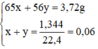
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g
Đúng 1
Bình luận (0)
1 Hòa tan hết 20g hỗn hợp Fe và FeO cần dùng vừa đủ 300g dd H2SO4 loãng , thu được dd X và 2,24l khí thoát ra ở đktc.Tính % khối lượng của sắt trong hõn hợp trên Tính C% của dd H2SO4 ban đầu và C%muối trong dd X2 Cho 8,4 gam bột sắt vào 100ml dd CuSO4 1M(D1,08g/ml) đến khi phản ứng kết thúc thu được chất rắn X và dd Y Viết PTHHTính a và C% chất tan có trong dd Y3Cho Ag hỗn hợp Fe,Cu có khối lượng bằng nhau vào dd H2SO4 loãng dư thu được 2,24 l khí (đktc), chất rắn ko tan đem hòa tan hết trong dd...
Đọc tiếp
1 Hòa tan hết 20g hỗn hợp Fe và FeO cần dùng vừa đủ 300g dd H2SO4 loãng , thu được dd X và 2,24l khí thoát ra ở đktc.Tính % khối lượng của sắt trong hõn hợp trên
Tính C% của dd H2SO4 ban đầu và C%muối trong dd X
2 Cho 8,4 gam bột sắt vào 100ml dd CuSO4 1M(D=1,08g/ml) đến khi phản ứng kết thúc thu được chất rắn X và dd Y
Viết PTHH
Tính a và C% chất tan có trong dd Y
3Cho Ag hỗn hợp Fe,Cu có khối lượng bằng nhau vào dd H2SO4 loãng dư thu được 2,24 l khí (đktc), chất rắn ko tan đem hòa tan hết trong dd H2SO4 đậm đặc nóng thu được Vlít SO2 (đktc). Ngâm Ag hỗn hợp trên vào dd CuSO4 dư.
Tính V
Tính khối lượng chất rắn thu được sau phản ứng
Hòa tan hoàn toàn m gam hỗn hợp bột kim loại trong dung dịch H2SO4 loãng dư thu được 0,672 lít khí H2 (đktc) và 3,92 gam hỗn hợp muối sunfat. Giá trị của m là: A. 2,48 B. 1,84 C. 1,04 D. 0,98
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp bột kim loại trong dung dịch H2SO4 loãng dư thu được 0,672 lít khí H2 (đktc) và 3,92 gam hỗn hợp muối sunfat. Giá trị của m là:
A. 2,48
B. 1,84
C. 1,04
D. 0,98