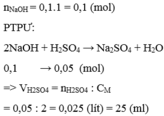Trung hòa 50 ml dd NaOH 2M cần V ml dd H2SO4 1M. Tính giá trị của V

Những câu hỏi liên quan
trung hòa 100 ml dd NaOH 1M cần Vml dd H2SO4 0,5M. TÌM giá trị V là
A.100 B.50 C.200 D.150
PTHH: \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
Ta có: \(n_{NaOH}=0,1\left(mol\right)\) \(\Rightarrow n_{H_2SO_4}=0,05\left(mol\right)\) \(\Rightarrow V_{H_2SO_4}=\dfrac{0,05}{0,5}=0,1\left(l\right)=100\left(ml\right)\)
Đúng 1
Bình luận (0)
Cho 200 ml dd NaOH 2M tác dụng vừa đủ với V ml dd H2SO4 1M,thu đc dd chỉ có muối trung hòa.hãy tìm giá trị V
Xem chi tiết
Đổi: \(200ml=0,2l\)
\(n_{NaOH}=C_{M_{NaOH}}\cdot V_{dd_{NaOH}}=2\cdot0,2=0,4mol\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+4H_2O\)
\(0,4----0,2---\left(mol\right)\)
Theo phương trình: \(n_{NaOH}=2n_{H_2SO_4}=0,4mol\Rightarrow n_{H_2SO_4}=0,2mol\)
\(V_{dd_{H_2SO_4}}=\dfrac{n_{H_2SO_4}}{C_{M_{H_2SO_4}}}=\dfrac{0,2}{1}=0,2l=200ml\)
Đúng 2
Bình luận (0)
Trung hòa 30ml dd H2SO4 1m cần dung 50 ml dung dịch NaOH:
a) Viết PTHH
b)Tính nồng độ dd NaOH đã dùng
c) Nếu trung hòa dd H2SO4 ở trên bằng dd KOH 5,6% có khối lượng riêng 1,045g/ml thì cần bao nhiêu ml KOH
a) $2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
b)
n H2SO4 = 0,03.1 = 0,03(mol)
n NaOH = 2n H2SO4 = 0,06(mol)
=> CM NaOH = 0,06/0,05 = 1,2M
c) $H_2SO_4 + 2KOH \to K_2SO_4 + 2H_2O$
n KOH = 2n H2SO4 = 0,06(mol)
=> m KOH = 0,06.56 = 3,36 gam
=> m dd KOH = 3,36/5,6% = 60(gam)
=> V dd KOH = m/D = 60/1,045 = 57,42(ml)
Đúng 6
Bình luận (0)
cho 200ml dd gồm naoh 1m và ba(oh)2 1m tac dung voi v ml dung dịch gom hcl 2m và h2so4 1m.duoc dung dich a. dung dich a duoc trung hoa boi 200ml dd hno3 1m tính giá trị của v
\(n_{OH^-}=0,2.1+0,2.1.2=0,6\left(mol\right)\)
\(n_{H^+}=V.2+V.1.2=4V\left(mol\right)\)
H+ + OH- --------> H2O (1)
Vì dung dịch A được trung hòa bởi 200 ml dd HNO3 1M
=>Dung dịch A có OH- dư sau phản ứng
\(n_{H^+}=0,2.1=0,2\left(mol\right)\)
H+ + OH- dư --------> H2O
=> \(n_{OH^-\left(dư\right)}=n_{H^+\left(củaHNO3\right)}=0,2\left(mol\right)\)
=> \(n_{OH^-\left(pứ\right)}=0,6-0,2=0,4\left(mol\right)\)
Từ (1) => \(n_{H^+}=n_{OH^-\left(pứ\right)}=0,4\left(mol\right)\)
=> 4V=0,4
=> V= 0,1 (lít)
Đúng 3
Bình luận (0)
Trung hòa 200 ml dd A gồm HCl 1M và H2SO4 2M cần V ml dd B gồm NaOH 1M và Ba(OH)2 0.2 M
Tìm V và m muối thu đc
tìm m kết tủa max
Hòa tan hoàn toàn 12,8g hh A gồm Fe và FeO trong 250 ml dd H2SO4 1M loãng (lấy dư) thu được 2,24l H2 (đktc) và dung dịch B.
a. Tính phần trăm khối lượng mỗi chất trong hh A .
b, Trung hòa dung dịch B cần dùng V ml dung dịch NaOH 1M. Tính giá trị V
a, gọi a= nFe
b= nFeO
=> 56a + 72b= 12,8 (1)
Fe +H2SO4 -> FeSO4 +H2
a b b a
FeO +H2SO4 -> FeSO4 +H2O
b b b
a=nH2 = 2,24/22,4= 0,1 mol
từ (1) => b= 0,1
mFe= 56.0,1=5,6(g)
m FeO = 72.0,1= 7,2(g)
b, nH2SO4 (bđ) = 0,25 mol
nH2SO4 pứ = a+b =0,2 mol
=> nH2SO4 dư = 0,25-0,2=0,05 mol
2NaOH +H2SO4 -> Na2SO4 +2H2O
0,1 0,05
V(NaOH)= 0,1/ 1= 0,1 lit =100ml
Đúng 1
Bình luận (1)
E tham khảo! Anh nãy làm tại câu hỏi bấm lộn xóa

Đúng 2
Bình luận (0)
Để trung hòa hoàn toàn 100ml dung dịch NaOH 1M cần vừa đủ V ml dung dịch H 2 S O 4 2M. Giá trị của V là:
A. 25ml
B. 50ml
C. 100ml
D. 200ml
Cho 100(ml) dd H2SO4 0,05M và Al2(SO4)3 1M vào V(ml) dd NaOH 1M. Kết thúc thu được 3,9 g kết tủa. Tính giá trị lớn nhất của V ?
Al2(SO4)3 +6NaOH---->2Al(OH)3 +3Na2SO4(1)
Al(OH)3 +NaOH----->NaAlO2 +2H2O(2)
Ta có
nAl2(SO4)3=0,05.0,1=0,005(mol)Al2(SO4)3=0,05.0,1=0,005(mol)
Theo pthh1
nAl(OH)3=2nAl2(SO4)3=0,01(mol)Al(OH)3=2nAl2(SO4)3=0,01(mol)
Mà nAl(OH)3=0,7878=0,01(mol)Al(OH)3=0,7878=0,01(mol)
=> NaOH dư
Theo pthh
nNaOH=6nAl2(SO4)3=0,06(mol)NaOH=6nAl2(SO4)3=0,06(mol)
VNaOH=0,060,2=0,3(M)
Đúng 1
Bình luận (1)
Trung hoà 100 ml dd axit (chứa HCl nồng độ 2M: H2SO4 nồng độ 1M) cần V(ml) dung dịch Ba(OH)z nồng độ 2M. Giá trị của V là A 200. B 150.C300. D 100.
Ta có: \(n_{HCl}=0,1.2=0,2\left(mol\right)\)
\(n_{H_2SO_4}=0,1.1=0,1\left(mol\right)\)
PT: \(2HCl+Ba\left(OH\right)_2\rightarrow BaCl_2+2H_2O\)
_____0,2_____0,1 (mol)
\(H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_{4\downarrow}+2H_2O\)
0,1________0,1 (mol)
⇒ nBa(OH)2 = 0,1 + 0,1 = 0,2 (mol)
\(\Rightarrow V_{Ba\left(OH\right)_2}=\dfrac{0,2}{2}=0,1\left(l\right)=100\left(ml\right)\)
⇒ Đáp án: D
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)