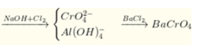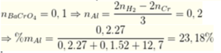Cho 23.3 gam hỗn hợp (Fe, Cu) tác dụng với dung dịch HCl dư tạo ra 12,7 gam muối. Tính khối lượng và thành phần % khối lượng

Những câu hỏi liên quan
Cho hỗn hợp 2 kim loại Fe và Cu tác dụng với khí clo dư thu được 59,5 gam hỗn hợp muối. Cũng lượng hỗn hợp trên cho tác dụng với lượng dư dung dịch HCl 10% thu được 25,4 gam một muối. Tính phần trăm khối lượng mỗi muối trong hỗn hợp muối thu được.
2Fe + 3 Cl 2 → t ° 2Fe Cl 3 ( M FeCl 3 = 162,5 gam)
Cu + Cl 2 → t ° Cu Cl 2
Fe + 2HCl → Fe Cl 2 + H 2 ( M FeCl 2 = 127 gam)
n Fe = x mol
Theo đề bài và phương trình hóa học trên ta có:
127x = 25,4 => 0,2 mol
162,5x + 135y = 59,5. Thay x = 0,2 vào phương trình, ta có:
32,5 + 135y = 59,5 => y = 0,2
m FeCl 3 = 0,2 x 162,5 = 32,5g
m CuCl 2 = 0,2 x 135 = 27g
% m FeCl 3 = 32,5 : (32,5 + 27).100% = 54,62%
% m CuCl 2 = 100% - 54,62% = 45,38%
Đúng 0
Bình luận (0)
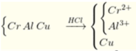
Hỗn hợp Cr, Al, Cu tác dụng với lượng dư dung dịch HCl (không có mặt không khí) tạo nên 8,96 lít khí (đktc) và 12,7 gam bã rắn không tan. Lọc lấy dung dịch, thêm một lượng dư dung dịch NaOH và nước clo rồi thêm dư dung dịch BaCl2, thu được 25,3 gam kết tủa vàng. Phần trăm khối lượng Al trong hỗn hợp là A. 23,18 B. 22,31 C. 19,52 D. 40,15
Đọc tiếp
Hỗn hợp Cr, Al, Cu tác dụng với lượng dư dung dịch HCl (không có mặt không khí) tạo nên 8,96 lít khí (đktc) và 12,7 gam bã rắn không tan. Lọc lấy dung dịch, thêm một lượng dư dung dịch NaOH và nước clo rồi thêm dư dung dịch BaCl2, thu được 25,3 gam kết tủa vàng. Phần trăm khối lượng Al trong hỗn hợp là
A. 23,18
B. 22,31
C. 19,52
D. 40,15
Hỗn hợp Cr, Al, Cu tác dụng với lượng dư dung dịch HCl (không có mặt không khí) tạo nên 8,96 lít khí (đktc) và 12,7 gam bã rắn không tan. Lọc lấy dung dịch, thêm một lượng dư dung dịch NaOH và nước clo rồi thêm dư dung dịch BaCl2, thu được 25,3 gam kết tủa vàng. Phần trăm khối lượng Al trong hỗn hợp là A. 23,18. B. 22,31. C. 19,52. D. 40,15.
Đọc tiếp
Hỗn hợp Cr, Al, Cu tác dụng với lượng dư dung dịch HCl (không có mặt không khí) tạo nên 8,96 lít khí (đktc) và 12,7 gam bã rắn không tan. Lọc lấy dung dịch, thêm một lượng dư dung dịch NaOH và nước clo rồi thêm dư dung dịch BaCl2, thu được 25,3 gam kết tủa vàng. Phần trăm khối lượng Al trong hỗn hợp là
A. 23,18.
B. 22,31.
C. 19,52.
D. 40,15.
Cho 16 gam hỗn hợp bột Fe và Mg tác dụng với dung dịch HCl dư thấy có 1 gam khí H2 bay ra. Khối lượng muối clorua tạo ra trong dung dịch là bao nhiêu gam?
A. 33,75 gam.
B. 1,5 gam.
C. 87 gam.
D. 51,5 gam
Đáp án D.
Số mol của Hiđro bằng: n H 2 = 1 2 = 0 , 5 ( m o l )
Lại có n C l - ( t r o n g m u ố i ) = 2 n H 2 = 2 . 0 , 5 = 1 ( m o l )
Khối lượng muối tạo thành bằng: 16 + 1. 35,5 = 51,5 (gam).
Đúng 0
Bình luận (0)
1.Cho 8 gam hỗn hợp gồm Cu và Fe tác dụng với dung dịch HCl dư tạo thành 1,68 lít khí H2 thoát ra ở đktc . Tính % về khối lượng của từng kim loại có trong hỗn hợp ?2.Cho hỗn hợp gồm Ag và Al tác dụng với dung dịch H2SO4 dư tạo thành 6,72 lít khí H2 thoát ra ở đktc và 4,6 g chất rắn không tan . Tính % về khối lượng của từng kim loại có trong hỗn hợp ?3.Cho 11 gam hỗn hợp gồm Al và Fe tác dụng vừa đủ với dung dịch HCl 2M tạo thành 8,96 lít khí H2 thoát ra ở đktc .a)Tính % về khối lượng c...
Đọc tiếp
1.Cho 8 gam hỗn hợp gồm Cu và Fe tác dụng với dung dịch HCl dư tạo thành 1,68 lít khí H2 thoát ra ở đktc . Tính % về khối lượng của từng kim loại có trong hỗn hợp ?
2.Cho hỗn hợp gồm Ag và Al tác dụng với dung dịch H2SO4 dư tạo thành 6,72 lít khí H2 thoát ra ở đktc và 4,6 g chất rắn không tan . Tính % về khối lượng của từng kim loại có trong hỗn hợp ?
3.Cho 11 gam hỗn hợp gồm Al và Fe tác dụng vừa đủ với dung dịch HCl 2M tạo thành 8,96 lít khí H2 thoát ra ở đktc .
a)Tính % về khối lượng của từng kim loại có trong hỗn hợp ?
b)Tính thể tích dung dịch HCl đã tham gia phản ứng ?
4. Cho 8,8 gam hỗn hợp gồm Mg và MgO tác dụng vừa đủ với dung dịch HCl 14,6% .Cô cạn dung dịch sau phản ứng thu được 28,5 gam muối khan
a)Tính % về khối lượng của từng chất có trong hỗn hợp ?
b)Tính khối lượng dung dịch HCl đã tham gia phản ứng ?
c)Tính nồng độ phần trăm của muối tạo thành sau phản ứng ?
5. Cho 19,46 gam hỗn hợp gồm Mg , Al và Zn trong đó khối lượng của Magie bằng khối lượng của nhôm tác dụng với dung dịch HCl 2M tạo thành 16, 352 lít khí H2 thoát ra ở đktc .
a)Tính % về khối lượng của từng kim loại có trong hỗn hợp ?
b)Tính thể tích dung dịch HCl đã dùng biets người ta dùng dư 10% so với lý thuyết ?
6. Hòa tan 13,3 gam hỗn hợp NaCl và KCl vào nước thu được 500 gam dung dịch A Lấy 1/10 dung dịch A cho phản ứng với AgNO3 tạo thành 2,87 gam kết tủa
a)Tính % về khối lượng của mỗi muối có trong hỗn hợp ?
b)Tính C% các muối có trong dung dịch A
7. Dẫn 6,72 lít (đktc) hỗn hợp khí gồm CH4 , C2H4 qua bình Brom dư thấy khối lượng bình đựng dung dịch Brom tăng 5,6 gam . Tính % về khối lượng của mỗi hiddro cacbon có trong hỗn hợp ?
8. Dẫn 5,6 lít (đktc) hỗn hợp khí gồm CH4 , C2H4 và C2H2 qua bình Brom dư thấy khối lượng bình đựng dung dịch Brom tăng 5,4 gam . Khí thoát ra khỏi bình được đốt cháy hoàn toàn thu được 2,2 gam CO2 . Tính % về khối lượng của mỗi hiddro cacbon có trong hỗn hợp ?
9. Chia 26 gam hỗn hợp khí gồm CH4 , C2H6 và C2H4 làm 2 phần bằng nhau
– Phần 1 : Đốt cháy hoàn toàn thu được 39,6 gam CO2
– Phần 2 : Cho lội qua bình đựng d/dịch brom dư thấy có 48 gam brom tham gia phản ứng
Tính % về khối lượng của mỗi hiddro cacbon có trong hỗn hợp ?
10. Hòa tan hoàn toàn 10 gam hỗn hợp của Mg và MgO bằng dung dịch HCl . Dung dịch thu được cho tác dụng với với dung dịch NaOH dư . Lọc lấy kết tủa rửa sạch rồi nung ở nhiệt độ cao cho đến khi khối lượng không đổi thu được 14 gam chất rắn
Chú ý: Mỗi lần hỏi bạn up lên từng câu hỏi thôi, không nên đưa một lúc nhiều câu hỏi trong 1 lần hỏi, vì như thế chỉ có 1 câu được trả lời thôi nhé.
Đúng 0
Bình luận (0)
HD:
Bài 1.
Vì Cu đứng sau H trong dãy các kim loại nên Cu không phản ứng với HCl.
Fe + 2HCl \(\rightarrow\) FeCl2 + H2
0,075 mol
Theo phản ứng trên, số mol Fe = số mol H2 = 0,075 mol. Suy ra khối lượng Fe = 56.0,075 = 4,2 g.
Khối lượng Cu = 8 - 4,2 = 3,8 g. Từ đó, %Fe = 4,2.100/8 = 52,5%; %Cu = 100 - 52,5 = 47,5%.
Đúng 1
Bình luận (1)
Bài 3
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2 (1)
x 1,5x
Fe + 2HCl \(\rightarrow\) FeCl2 + H2 (2)
y y
a) Gọi x, y tương ứng là số mol của Al và Fe trong hh. Ta có: 27x + 56y = 11 và 1,5x + y = số mol H2 = 0,4. Giải hệ trên thu được x = 0,2; y = 0,1.
Khối lượng của Al = 27.0,2 = 5,4 g; khối lượng Fe = 56.0,1 = 5,6 g. %Al = 5,4.100/11 = 49,09%; %Fe = 50,91%.
b) Số mol HCl = 6x + 2y = 6.0,2 + 2.0,1 = 1,4 mol. Như vậy V = 1,4/2 = 0,7 lít = 700 ml.
Đúng 0
Bình luận (10)
Xem thêm câu trả lời
Cho 12,45 gam hỗn hợp Mg, Zn, Fe tác dụng hết với dung dịch HCl thấy thoát ra 6,72 lít H2 (đktc). Tính khối lượng muối tạo thành?
A. 33 gam
B. 33,75 gam
C. 34 gam
D. 33,50 gam
Đáp án B.
Số mol của Hiđro bằng:
n H 2 = 6 , 72 22 , 4 = 0 , 3 ( m o l )
lại có n C l - t r o n g m u ố i = 2 n H 2 = 2 . 0 , 3 = 0 , 6
Khối lượng muối tạo thành bằng: 12,45 + 0,6. 35,5 = 33,75 (gam).
Đúng 0
Bình luận (0)
Cho 15 gam hỗn hợp gồm 2 kim loại Cu và Fe tác dụng với dung dịch HCl dư thấy thoát ra 3,36l khí H2 ở đktc
a)Tính thành phần % khối lượng mỗi kim loại trong hỗn hợp ban đầu
b)Tính thể tích dung dịch HCl 1M đã dùng cho phản ứng trên?
Ta có nH2 = 3,36/22,4 = 0,15 mol
Fe +2 HCl -> FeCl2 + H2
0,15. 0,3 <-. 0,15. ( Mol)
=> mFe = 0,15 × 56 = 8,4g
=> %Fe = 8,4/15×100% = 56%
=> %Cu = 100% - 56% = 44%
=>VHCl =1\0,3=10\3 l
Đúng 3
Bình luận (0)
PTHH : 2Fe + 6HCl --> 2FeCl3 + 3H2 (1)
nH2 = \(\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
Từ (1) -> nFe = \(\dfrac{2}{3}n_{H_2}=0.1\left(mol\right)\)
-> mFe = n.M = 0,1 . 56 = 5.6 (g) => %mFe = \(\dfrac{5.6}{15}x100\%\approx37.3\%\)
-> %mCu = 100% - 37.3% = 62.7 %
Đúng 1
Bình luận (2)
Một hỗn hợp gồm hai kim loại Fe và Cu ở điều kiện thích hợp tác dụng với khí clo dư thu được 59,5 gam hỗn hợp hai muối. Cũng lượng hỗn hợp trên cho tác dụng với lượng dư dung dịch HCl 10% thì thu được 25,4 gam một muối duy nhất. 1) Tính thành phần phần trăm khối lượng mỗi muối trong trường hợp thứ nhất. 2) Tính thể tích dung dịch HCl 10% (d 1,0g/ml) đã dùng.
Đọc tiếp
Một hỗn hợp gồm hai kim loại Fe và Cu ở điều kiện thích hợp tác dụng với khí clo dư thu được 59,5 gam hỗn hợp hai muối. Cũng lượng hỗn hợp trên cho tác dụng với lượng dư dung dịch HCl 10% thì thu được 25,4 gam một muối duy nhất.
1) Tính thành phần phần trăm khối lượng mỗi muối trong trường hợp thứ nhất.
2) Tính thể tích dung dịch HCl 10% (d = 1,0g/ml) đã dùng.
Gọi số mol của Fe và Cu trong hỗn hợp lần lượt là x và y.
2Fe + 3Cl2 → 2FeCl3 (1)
x(mol) x(mol)
Cu + Cl2 → CuCl2 (2)
y(mol) y(mol)
Fe + 2HCl → FeCl2 + H2 (3)
x (mol) 2x(mol) x(mol).
Theo điều kiện bài toán và phương trình hoá học (3) ta có: 127x = 25,4 → x = 0,2
Theo phương trình phản ứng (1) và (2) ta có: 162,5x + 135y = 59,5
Vậy y = 0,2.
Khối lượng mỗi muối là: m FeCl3=32,5gam
m CuCl2=27gam
%FeCl3 = 54,62%.
%CuCl2 = 45,38%
Đúng 0
Bình luận (0)
câu b
Khối lượng dung dịch HCl 10% đã dùng là:146 gam 0,25 đ
Vậy VHCl = 146 ml.
Đúng 0
Bình luận (0)
Cho 8 gam hỗn hợp gồm Cu và Fe tác dụng với dung dịch HCl dư tạo thành 1,68 lít khí H2 thoát ra ở đktc . Tính khối lượng của mỗi chất rắn có trong hỗn hợp ban đầu
Bài tập của bạn hình như là sai số nên mk tính ko ra.
Đúng 0
Bình luận (0)
nH2 = 1,68/22,4 = 0,075 mol
Fe (0,075) + 2HCl ------> FeCl2 + H2 (0,075)
-Theo PTHH: nFe = 0,075 mol
=> mFe= 0,075 . 56 = 4,2 gam
=> mCu = 8 - 4,2 = 3,8 gam
Đúng 0
Bình luận (0)