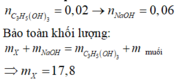Hòa tan hoàn toàn 10g oxit của một kim loại có hóa trị 2trong dung dịch hcl. Cô cạn dd sau phản ứng thu 23,75g muối, kim loại đó là

Những câu hỏi liên quan
Hòa tan hoàn toàn 5,95g hỗn hợp muối cacbonat của kim loại hóa trị I và kim loại hóa trị II trong dd HCl thì sinh ra 1,12l khí (đktc). Đem cô cạn dung dịch sau phản ứng thì thu được bao nhiêu (g) muối khan.
Ta có:
\(n_{CO_2}=\frac{1.12}{22.4}=0.05\left(mol\right)\) \(\Rightarrow m_{CO_2}=0.05\times44=2.2\left(g\right)\)
\(X_2CO_3+2HCl\rightarrow2XCl+H_2O+CO_2\)
\(YCO_3+2HCl\rightarrow YCl_2+H_2O+CO_2\)
Ta thấy
\(n_{HCl}=2n_{CO_2}=2\times0.05=0.1\left(mol\right)\)
\(\Rightarrow\) \(m_{HCl}=0.1\times36.5=3.65\left(g\right)\)
\(n_{H_2O}=n_{CO_2}=0.05\left(mol\right)\)
\(\Rightarrow\) \(m_{H_2O}=0.05\times18=0.9\left(g\right)\)
Áp dụng định luật bảo toàn khối lượng ta được:
\(m_{XCl+YCl_2}=\left(5.95+3.65\right)-\left(2.2+0.9\right)=9.6-3.1=6.5\left(g\right)\)
Đúng 0
Bình luận (1)
Nhúng một lá kim loại M (hóa trị II) nặng 56 gam vào 200 ml dung dịch AgNO3 1M cho đến khi phản ứng xảy ra hoàn toàn. Lọc dung dịch, đem cô cạn đượng 18,8 g muối khan kim loại M là:
A. Mg
B. Zn
C. Cu
D. Fe
Đáp án C
Ta có:
![]()
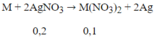
M + 62,2 = 18,8/0,1 = 188 → M = 64
Đúng 0
Bình luận (0)
Câu 1: Nhiệt phân hoàn toàn 10g muối cacbonat của kim laoij R (hóa trị II). Sau phản ứng thu được 5,6g một oxit và V (lít) khí ở đktc
a, Tính giá trị của V
b, Xác định kim loại M
Câu 2: Hòa tan 0,54g một kim loại R (có hóa trị III trong hợp chất) bằng 50 ml dung dịch HCl 2M. Sau phản ứng thu được 0,672 lít khí (ở đktc). Xác định kim loại R.
Câu 3: Hòa tan 21g một kim loại M hóa trị II trong dd H2SO4 loãng dư, người ta thu được 8,4 lít hiđro (...
Đọc tiếp
Câu 1: Nhiệt phân hoàn toàn 10g muối cacbonat của kim laoij R (hóa trị II). Sau phản ứng thu được 5,6g một oxit và V (lít) khí ở đktc
a, Tính giá trị của V
b, Xác định kim loại M
Câu 2: Hòa tan 0,54g một kim loại R (có hóa trị III trong hợp chất) bằng 50 ml dung dịch HCl 2M. Sau phản ứng thu được 0,672 lít khí (ở đktc). Xác định kim loại R.
Câu 3: Hòa tan 21g một kim loại M hóa trị II trong dd H2SO4 loãng dư, người ta thu được 8,4 lít hiđro (đktc) và dung dịch A. Xác định kim loại M.
Câu 4: Cho 12g một kim loại hóa trị II tác dụng hết với dd H2SO4 loãng thu được 11,21 lít khí (đktc). Xác định kim loại hóa trị II?
1.
RCO3 -> RO + CO2
Áp dụng ĐLBTKL ta có:
mRCO3=mRO+mCO2
=>mCO2=10-5,6=4,4((g)\(\Leftrightarrow\)0,1(mol)
VCO2=22,4.0,1=2,24(lít)
Theo PTHH ta có:
nRCO3=nCO2=0,1(mol)
MRCO3=\(\dfrac{10}{0,1}=100\)
=>MR=100-60=40
=>R là Ca
Đúng 0
Bình luận (0)
4.
R + H2SO4 -> RSO4 + H2
nH2=0,5(mol)
Theo PTHH ta có:
nR=nH2=0,5(mol)
MR=\(\dfrac{12}{0,5}=24\)
=>R là Mg
Đúng 0
Bình luận (0)
3.
M + H2SO4 -> MSO4 + H2
nH2=0,375(mol)
Theo PTHH ta có:
nM=nH2=0,375(mol)
MM=\(\dfrac{21}{0,375}=56\)
=> M là Fe
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
A là hỗn hợp của cacbonat trung hòa của 2 kim loại X( hóa trị i ) và Y hóa trị ii. Hòa tan hoàn toàn 18g hỗn hợp a bằng ddHCl vừa đủ thì thu được 2,24l khí ở đktc và dd B
a)nếu cô cạn dd B thì thu được bao nhiêu gam muối khan
b) Nếu tỉ lệ số mol muối cacbonat của X và muối cacbonat của Y là 2:1, NTK X>Y là 15đvC. Xác định công thức của 2 muối
Hòa tan hoàn toàn 7,02 gam một kim loại kiềm M trong nước. Sau phản ứng, đem cô cạn dung dịch được một chất rắn khan có khối lượng là 10,08 gam. Kim loại M là?
Xem chi tiết
Gọi: CTHH của bazo : M(OH)n
TH1: n = 1
M + H2O --> MOH + H2
M__________M+17
7.02________10.08
<=> 7.02*(M+17) = 10.08M
=> M = 39 (n)
Vậy: M là Kali
TH2: n= 2
M + 2H2O --> M(OH)2 + H2
M____________M+ 34
7.02__________10.08
<=> 7.02(M+34) = 10.08M
=> M = 78 => loại
Cù Văn Thái
Đúng 0
Bình luận (4)
Hòa tan hoàn toàn 7,02 gam một kim loại kiềm M trong nước. Sau phản ứng, đem cô cạn dung dịch được một chất rắn khan có khối lượng là 10,08 gam. Kim loại M là ?
Xem chi tiết
M -----pứ---> MOH
=> m tăng= 10,08-7,02 =mOH=3,06g
=>nOH=0,18 mol=nM
=> MM=7,02/0,18=39 =>K
Đúng 0
Bình luận (0)
Xà phòng hóa hoàn toàn m gam chất béo X với một lượng vừa đủ NaOH. Cô cạn dung dịch sau phản ứng, thu được 1,84 gam glixerol và 18,36 muối khan. Giá trị của m là
A. 19,12.
B. 17,8.
C. 19,04.
D. 14,68.
Xà phòng hóa hoàn toàn m gam chất béo X với một lượng vừa đủ NaOH. Cô cạn dung dịch sau phản ứng, thu được 1,84 gam glixerol và 18,36 muối khan. Giá trị của m là
A. 19,12
B. 17,8
C. 19,04
D. 14,68
Chọn đáp án B
nC3H5(OH)3 = 0,2 => nNaOH = 0,06.
Bảo toàn khối lượng:
mX + mNaOH = mC3H5(OH)3 + mmuối
=> mX = 17,8.
Đúng 0
Bình luận (0)
Cho 0,1 mol este X (no, đơn chức, mạch hở) phản ứng hoàn toàn với dung dịch chứa 0,18 mol MOH (M là kim loại kiểm). Cô cạn dung dịch sau phản ứng thu được chất rắn Y và 4,6 gam ancol Z. Đốt cháy hoàn toàn Y, thu được , và 4,84 gam . Tên gọi của X là: A. etyl fomat B. Metyl axetat C. Etyl axetat D. Metyl fomat
Đọc tiếp
Cho 0,1 mol este X (no, đơn chức, mạch hở) phản ứng hoàn toàn với dung dịch chứa 0,18 mol MOH (M là kim loại kiểm). Cô cạn dung dịch sau phản ứng thu được chất rắn Y và 4,6 gam ancol Z. Đốt cháy hoàn toàn Y, thu được , và 4,84 gam . Tên gọi của X là:
A. etyl fomat
B. Metyl axetat
C. Etyl axetat
D. Metyl fomat