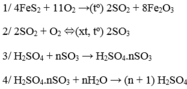Giải thích tại sao để sản xuất axit sunfuric trong công nghiệp lại sử dụng axit sunfuric đặc 98% để hấp thụ SO3 mà không cho SO3 tác dụng với nước?

Những câu hỏi liên quan
Trong công nghiệp người ta sản xuất axit sunfuric theo sơ đồ sau: FeS2 → SO2 → SO3 → H2SO4. Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axit sunfuric từ quặng trên là: A. 40%. B. 60%. C. 80%. D. 62,5%
Đọc tiếp
Trong công nghiệp người ta sản xuất axit sunfuric theo sơ đồ sau:
FeS2 → SO2 → SO3 → H2SO4.
Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axit sunfuric từ quặng trên là:
A. 40%.
B. 60%.
C. 80%.
D. 62,5%
Đáp án C.
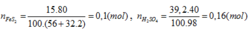
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%
Đúng 0
Bình luận (0)
Axit sunfuric H2SO4 là một trong những hóa chất có ứng dụng hàng đầu trong đời sống như: sản xuất phân bón, thuốc trừ sâu, chất giặt rửa tổng hợp, tơ sợi hóa học, chất dẻo, sơn, dược phẩm. Trên thế giới mỗi năm người ta sản xuất khoảng 160 triệu tấn H2SO4 từ lưu huỳnh hoặc quặng pirit FeS2 theo sơ đồ sau: a. Hoàn thành sơ đồ chuyển hóa trên (ghi rõ điều kiện phản ứng nếu có) b. Trong thực tế sản xuất, để an toàn người ta không hấp thụ trực tiếp SO3 vào nước mà hấp thụ SO2 vào H2SO4 đặc để tạot...
Đọc tiếp
Axit sunfuric H2SO4 là một trong những hóa chất có ứng dụng hàng đầu trong đời sống như: sản xuất phân bón, thuốc trừ sâu, chất giặt rửa tổng hợp, tơ sợi hóa học, chất dẻo, sơn, dược phẩm. Trên thế giới mỗi năm người ta sản xuất khoảng 160 triệu tấn H2SO4 từ lưu huỳnh hoặc quặng pirit FeS2 theo sơ đồ sau:
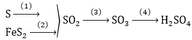
a. Hoàn thành sơ đồ chuyển hóa trên (ghi rõ điều kiện phản ứng nếu có)
b. Trong thực tế sản xuất, để an toàn người ta không hấp thụ trực tiếp SO3 vào nước mà hấp thụ SO2 vào H2SO4 đặc để tạothành Oleum (H2SO4.nSO3). Tùy theo mục đích sử dụng người ta hòa tan Oleum vào nước để thu được dung dịch H2SO4 có nồng độ theo yêu cầu. Hòa tan hoàn toàn 16,9 gam Oleum vào nước thu được 25 gam dung dịch H2SO4 78,4%. Xác định công thức của Oleum.
Trong công nghiệp người ta sản xuất axít sunfuric theo sơ đồ sau: FeS2
→
SO2
→
SO3
→
H2SO4 . Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axít sunfuric từ quặng trên là: A. 40% B. 60% C. 80% D. 62,5%
Đọc tiếp
Trong công nghiệp người ta sản xuất axít sunfuric theo sơ đồ sau: FeS2 → SO2 → SO3 → H2SO4 . Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axít sunfuric từ quặng trên là:
A. 40%
B. 60%
C. 80%
D. 62,5%
Câu 11. Phương pháp nào sau đây được dùng để sản xuất khí sunfurơ trong công nghiệp. a. Phân hủy canxisunfat ở nhiệt độ cao . b. Đốt cháy lưu huỳnh trong oxi . c. Cho đồng tác dụng với axit sunfuric đặc, nóng. d. Cho muối natrisunfit tác dụng với axit clohiđric.Câu 12. Chất nào sau đây khi tan trong nước cho dung dịch, làm quỳ tím hóa đỏ : a. KOH b. KNO3 c. SO3 d. CaOCâu 1...
Đọc tiếp
Câu 11. Phương pháp nào sau đây được dùng để sản xuất khí sunfurơ trong công nghiệp.
a. Phân hủy canxisunfat ở nhiệt độ cao .
b. Đốt cháy lưu huỳnh trong oxi .
c. Cho đồng tác dụng với axit sunfuric đặc, nóng.
d. Cho muối natrisunfit tác dụng với axit clohiđric.
Câu 12. Chất nào sau đây khi tan trong nước cho dung dịch, làm quỳ tím hóa đỏ :
a. KOH b. KNO3 c. SO3 d. CaO
Câu 13. Chất nào sau đây tác dụng với axit sunfuric loãng tạo thành muối và nước:
a. Cu b. CuO c. CuSO4 d. CO2
Câu 14. Canxioxit có thể làm khô khí nào có lẫn hơi nước sau đây:
a. Khí CO2 b. Khí SO2 c. Khí HCl d. CO
Câu 15. Một hỗn hợp rắn gồm Fe2O3 và CaO, để hòa tan hoàn toàn hỗn hợp này người ta phải dùng dư:
a. Nước. b. Dung dịch NaOH.
c. Dung dịch HCl. D. dung dịch NaCl.
Câu 16. Dung dịch axit mạnh không có tính nào sau đây:.
a. Tác dụng với oxit axit tạo thành muối và nước .
b. Tác dụng với bazơ tạo thành muối và nước .
. c. Tác dụng với nhiều kim loại giải phóng khí hiđrô.
d. Làm đổi màu quỳ tím thành đỏ.
Câu 17. Đơn chất nào sau đây tác dụng với H2SO4 loãng sinh ra chất khí :
a. Bạc b. Đồng c. Sắt d. cacbon.
Câu 18. Trong phòng thí nghiệm khí SO2 không thu bằng cách đẩy nước vì SO2 :
a. Nhẹ hơn nước b. Tan được trong nước.
c. Dễ hóa lỏng D. Tất cả các ý trên .
Câu 19. Để trung hòa 11,2gam KOH 20%, thì cần lấy bao nhiêu gam dung dịch axit H2SO435%
a. 9gam b. 4,6gam c. 5,6gam d. 1,7gam
Câu 20. Hòa tan 23,5 gam K2O vào nước. Sau đó dùng 250ml dung dịch HCl để trung hòa dung dịch trên. Tính nồng độ mol HCl cần dùng.
a. 1,5M b. 2,0 M c. 2,5 M d. 3,0 M.
Câu 11. Phương pháp nào sau đây được dùng để sản xuất khí sunfurơ trong công nghiệp.
a. Phân hủy canxisunfat ở nhiệt độ cao .
b. Đốt cháy lưu huỳnh trong oxi .
c. Cho đồng tác dụng với axit sunfuric đặc, nóng.
d. Cho muối natrisunfit tác dụng với axit clohiđric.
Câu 12. Chất nào sau đây khi tan trong nước cho dung dịch, làm quỳ tím hóa đỏ :
a. KOH b. KNO3 c. SO3 d. CaO
Câu 13. Chất nào sau đây tác dụng với axit sunfuric loãng tạo thành muối và nước:
a. Cu b. CuO c. CuSO4 d. CO2
Câu 14. Canxioxit có thể làm khô khí nào có lẫn hơi nước sau đây:
a. Khí CO2 b. Khí SO2 c. Khí HCl d. CO
Câu 15. Một hỗn hợp rắn gồm Fe2O3 và CaO, để hòa tan hoàn toàn hỗn hợp này người ta phải dùng dư:
a. Nước. b. Dung dịch NaOH.
c. Dung dịch HCl. D. dung dịch NaCl.
Câu 16. Dung dịch axit mạnh không có tính nào sau đây:.
a. Tác dụng với oxit axit tạo thành muối và nước .
b. Tác dụng với bazơ tạo thành muối và nước .
. c. Tác dụng với nhiều kim loại giải phóng khí hiđrô.
d. Làm đổi màu quỳ tím thành đỏ.
Câu 17. Đơn chất nào sau đây tác dụng với H2SO4 loãng sinh ra chất khí :
a. Bạc b. Đồng c. Sắt d. cacbon.
Câu 18. Trong phòng thí nghiệm khí SO2 không thu bằng cách đẩy nước vì SO2 :
a. Nhẹ hơn nước b. Tan được trong nước.
c. Dễ hóa lỏng D. Tất cả các ý trên .
Câu 19. Để trung hòa 11,2gam KOH 20%, thì cần lấy bao nhiêu gam dung dịch axit H2SO4 35%
a. 9gam b. 4,6gam c. 5,6gam d. 1,7gam
---
Không có đáp án đúng
_____________
Câu 20. Hòa tan 23,5 gam K2Ovào nước. Sau đó dùng 250ml dung dịch HCl để trung hòa dung dịch trên. Tính nồng độ mol HCl cần dùng.
a. 1,5M b. 2,0 M c. 2,5 M d. 3,0 M.
Đúng 0
Bình luận (1)
Để sản xuất axit sunfuric, người ta dung nhiên liệu là quặng pirit sắt
(
F
e
S
2
)
đem nghiền nhỏ rồi nung ở nhiệt độ cao thu được sắt III oxit
(
F
e
2
O
3
)
và khí sunfuro
(
S
O
2
)
.
Oxi hóa có
V
2
O
5
làm xúc tác ở nhiệt độ...
Đọc tiếp
Để sản xuất axit sunfuric, người ta dung nhiên liệu là quặng pirit sắt ( F e S 2 ) đem nghiền nhỏ rồi nung ở nhiệt độ cao thu được sắt III oxit ( F e 2 O 3 ) và khí sunfuro ( S O 2 ) . Oxi hóa có V 2 O 5 làm xúc tác ở nhiệt độ 450 ° C thu được S O 3 , cho S O 3 hợp với nước thu được axit sunfuric ( H 2 S O 4 ) . Hãy xác định đâu là hiện tượng vật lý, đâu là hiện tượng hóa học?
- Hiện tượng vật lý: nghiền nhỏ quặng pirit sắt ( F e S 2 )
- Hiện tượng hóa học:
+Quặng pirit sắt cháy tạo thành F e 2 O 3 và S O 2
+Oxi hóa S O 2 thành S O 3
+Hợp chất nước và S O 3 tạo thành axit sunfuric ( H 2 S O 4 )
Đúng 0
Bình luận (0)
cho 32 gam lưu huỳnh trioxit (SO3) tác dụng hết với nước thu được dung dịch axit sunfuric (H2SO4)
a, Viết PTHH của phản ứng xảy ra
b, tính khối lượng axit sunfuric thu được
a) \(n_{SO_3}=\dfrac{m}{M}=\dfrac{32}{80}=0,4\left(mol\right)\)
PTHH: `SO_3 + H_2O -> H_2SO_4`
b) Theo PTHH: `n_{H_2SO_4} = n_{SO_3} = 0,4 (mol)`
`=> m_{H_2SO_4} = 0,4.98 = 39,2 (g)`
Đúng 0
Bình luận (0)
Có thể điều chế được bao nhiêu mol axit sunfuric khi cho 240g lưu huỳnh trioxit S O 3 tác dụng với nước?
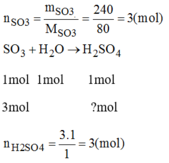
Vậy 3mol S O 3 tac dụng với H 2 O cho 3 mol H 2 S O 4
Đúng 0
Bình luận (0)
II-Tự luậnAxit sunfuric là hóa chất hàng đầu được dùng trong nhiều ngành công nghiệp. Hàng năm, các nước trên thế giới sản xuất ra khoảng 160 triệu tấn. Viết PTHH sản xuất
H
2
S
O
4
từ
F
e
S
2
theo sơ đồ:
F
e
S
2
→
S
O
2
→
S
O
3...
Đọc tiếp
II-Tự luận
Axit sunfuric là hóa chất hàng đầu được dùng trong nhiều ngành công nghiệp. Hàng năm, các nước trên thế giới sản xuất ra khoảng 160 triệu tấn. Viết PTHH sản xuất H 2 S O 4 từ F e S 2 theo sơ đồ: F e S 2 → S O 2 → S O 3 → o l e u m → H 2 S O 4 .
Cho các cách phát biểu sau: (1) Trong quá trình sản xuất axit H2SO4 để hấp thụ SO3 người ta dùng H2SO4 đặc. (2) Trong công nghiệp, người ta sản xuất oxi bằng cách cho MnO2 tác dụng với dung dịch axit HCl. (3) Kim cương, than chì, fuleren và cacbon vô định hình là các dạng thù hình của cacbon. (4) CaOCl2 là muối kép. (5) SO2 là khí độc và khi tan trong nước mưa tạo thành axit gây ra sự ăn mòn kim loại và các vật liệu. (6) Muốn pha loãng dung dịch H2SO4 đặc, cần rót từ từ dung dịch axit đặc vào nư...
Đọc tiếp
Cho các cách phát biểu sau:
(1) Trong quá trình sản xuất axit H2SO4 để hấp thụ SO3 người ta dùng H2SO4 đặc.
(2) Trong công nghiệp, người ta sản xuất oxi bằng cách cho MnO2 tác dụng với dung dịch axit HCl.
(3) Kim cương, than chì, fuleren và cacbon vô định hình là các dạng thù hình của cacbon.
(4) CaOCl2 là muối kép.
(5) SO2 là khí độc và khi tan trong nước mưa tạo thành axit gây ra sự ăn mòn kim loại và các vật liệu.
(6) Muốn pha loãng dung dịch H2SO4 đặc, cần rót từ từ dung dịch axit đặc vào nước.
(7) Để loại bỏ H2S ra khỏi hỗn hợp khí với H2 bằng cách cho hỗn hợp lội qua dung dịch NaOH hoặc Pb(NO3)2.
(8) Axit H3PO4 là axit mạnh vì nguyên tố P ở trạng thái oxi hóa cao nhất (+5).
(9) Thuốc thử để phân biệt O2 và O3 là KI có tẩm hồ tinh bột.
Trong các cách phát biểu trên, số phát biểu đúng là:
A. 6
B. 7
C. 3
D. 8
Đáp án A
Phát biểu (1) đúng. Trong quá trình sản xuất axit H2SO4 để hấp thụ SO3 người ta dùng H2SO4 đặc để tạo oleum H2SO4.nSO3. Pha loãng oleum sẽ thu được axit đặc.
Phát biểu (2) sai. Trong công nghiệp người ta sản xuất oxi bằng 2 cách: từ không khí và từ nước.
Phát biểu (3) đúng. Kim cương, than chì, fuleren và cacbon vô định hình là các dạng thù hình của cacbon.
Phát biểu (4) sai. CaOCl2 là muối hỗn tạp, không phải muối kép. Nó được tạo bởi 2 gốc axit là HCl; HClO
Phát biểu (5) đúng. SO2 là khí độc và khi tan trong nước mưa tạo thành axit gây ra sự ăn mòn kim loại và các vật liệu. Ngoài SO2, các khí NOx cũng là nguyên nhân gây ra mưa axit.
Phát biểu (6) đúng. Muốn pha loãng dung dịch H2SO4 đặc, cần rót từ từ dung dịch axit đặc vào nước. nếu làm ngược lại sẽ dễ bị bắn axit và quá trình tỏa nhiệt rất mạnh gây nguy hiểm.
Phát biểu (7) đúng. Để loại bỏ H2S ra khỏi hỗn hợp khí với H2 bằng cách cho hỗn hợp lội qua dung dịch NaOH hoặc Pb(NO3)2.
2NaOH + H2S → Na2S + 2H2O
Pb(NO3)2 + H2S → PbS↓ + 2HNO3
Phát biểu (8) sai. Axit H3PO4 là axit yếu vì trong dung dịch H3PO4 điện ly yếu (phân ly không hoàn toàn).
Phát biểu (9) đúng. Thuốc thử để phân biệt O2 và O3 là KI có tẩm hồ tinh bột
ü O3 phản ứng với KI tạo I2 làm xanh hồ tinh bột.
2KI + O3 + H2O → 2KOH + I2 + O2
ü O2 không phản ứng với KI
Đúng 0
Bình luận (0)