Bài tập 2: Trong ống khí có đựng 1,68 lít H2 và 1,12 lít O2 (đktc). Bật tia lửa điện để đốt hỗn hợp khí trên đến phản ứng hoàn toàn. Tính khối lượng nước tạo thành khi phản ứng kết thúc.
Trong bình kín chứa hỗn hợp X gồm hidrocacbon A mạch hở (thể khí ở điều kiện thường) và 0,06 mol O2, bật tia lửa điện để đốt X (chỉ xẩy ra phản ứng X cháy tạo thành CO2 và H2O). Toàn bộ hỗn hợp sau phản ứng cho đi qua bình đựng 3,5 lít dung dịch Ca(OH)2 0,01M thì thu được 3 gam kết tủa. Khí duy nhất thoát ra khỏi bình có thể tích 0,224 lít (đktc). Biết các phản ứng xẩy ra hoàn toàn, nước bị ngưng tụ khi cho qua dung dịch, có bao nhiêu CTPT thỏa mãn A?
A. 3
B. 8
C. 7
D. 5
Đáp án : C
Vì phản ứng cháy không cho biết có hoàn toàn hay không :
(*) TH1 : Lượng khí thoát ra chính là O2 dư => nO2 pứ = 0,05 mol
, nCaCO3 = 0,03 mol ; nCa(OH)2 = 0,035 mol
+) Nếu OH dư => nCO2 = nCaCO3 = 0,03 mol
Bảo toàn O : 2nO2 = 2nCO2 + nH2O => nH2O = 0,04 mol
=> nC : nH = 0,03 : 0,08 = 3 : 8 => C3H8
+) Nếu có HCO3- => nCaCO3 = nCO3 = nOH – nCO2 => nCO2 = 0,04 mol
Bảo toàn O => nH2O = 0,02
=> nC: nH = 0,04 : 0,04 = 1 : 1 => C2H2 hoặc C4H4
(*) TH2 : Hydrocacbon chưa cháy hết và 2,24 lit khí thoát ra chính là A
+) Nếu OH dư => nCO2 = nCaCO3 = 0,03 mol
Bảo toàn O : 2nO2 = 2nCO2 + nH2O => nH2O = 0,06 mol
=> nC : nH = 0,03 : 0,12 = 1 : 4 => CH4
+) Nếu có HCO3- => nCaCO3 = nCO3 = nOH – nCO2 => nCO2 = 0,04 mol
Bảo toàn O => nH2O = 0,04
=> nC: nH = 0,04 : 0,084 = 1 : 2 => C2H4 ; C3H6 hoặc C4H8
Tổng cộng có 7 chất thỏa mãn
Đốt cháy hỗn hợp khí gồm 1,12 lít khí hidro và 1,68 lít khí oxi ở đktc. Tính khối lượng nước tạo thành sau phản ứng
2h2+o2→2h2o
nH2=1.12/22.4=0.05(mol)
nO2=1.68/22.4=0.075(mol)
ta có nH2/2=0.05/2=0.025<nO2/1=0.075
→H2 hết ,O2 dư.
theo pt nH2o=nH2=0.05(mol)
mH2o=0.05*18=0.9 (g)
xong![]()
có hỗn hợp 8,96 lít hỗn hợp A gồm H2 và O2 có tỉ lệ 1:1. Bật tia lửa điện đốt cháy hỗn hợp A. khi phản ứng kết thúc thu được những chất nào? khối lượng là bao nhiêu?
Dẫn 1,68 lít hỗn hợp khí X gồm 2 hidrocacbon mạch hở vào bình đựng dung dịch brom (dư). Sau phản ứng hoàn toàn thấy phản ứng hoàn toàn thấy thoát ra 1,12 lít khí và lượng brom phản ứng là 4 gam. Nếu đốt cháy hoàn toàn 1,68 lít hỗn hợp X thì thu được 2,8 lít CO2. Công thức phân tử của 2 hidrocacbon trong X là:
A. CH4 và C2H4.
B. CH4 và C3H4.
C. CH4 và C3H6.
D. C2H6 và C3H6.
Vì sau phản ứng với dung dịch brom dư, có khí thoát ra khỏi bình nên trong hỗn hợp X ban đầu có ankan.

Do đó trong hỗn hợp X có 1 hidrocacbon có số nguyên tử C trong phân tử nhỏ hơn 1,67 và 1 hidrocacbon có số nguyên tử C trong phân tử lớn hơn 1,67.
Mà anken luôn có số nguyên tử C trong phân tử lớn hơn hoặc bằng 2.
Nên ankan trong X có số nguyên tử C nhỏ hơn 1,67.
Suy ra ankan đó là CH4.
Gọi công thức của anken trong X là CnH2n.
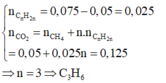
Do đó 2 hidrocacbon trong X là CH4 và C3H6.
Đáp án C.
Đốt cháy hỗn hợp gồm 1,12 (l) khí hiđro và 1,68 (l) khí oxi. Tính khối lượng nước tạo thành sau phản ứng kết thúc
Hỗn hợp khí B có thể tích 22,4 lít (đktc) gồm H2 và O2. Tỉ khối của B so với H2 bằng 5,5. Đốt nóng hỗn hợp khí B để phản ứng xảy ra hoàn toàn. Tính khối lượng chất thu được sau phản ứng
Gọi số mol H2, O2 là a, b (mol)
=> \(\left\{{}\begin{matrix}a+b=\dfrac{22,4}{22,4}=1\\M_B=\dfrac{2a+32b}{a+b}=5,5.2=11\left(g/mol\right)\end{matrix}\right.\)
=> a = 0,7 (mol); b = 0,3 (mol)
PTHH: 2H2 + O2 --to--> 2H2O
Xét tỉ lệ: \(\dfrac{0,7}{2}>\dfrac{0,3}{1}\) => H2 dư, O2 hết
PTHH: 2H2 + O2 --to--> 2H2O
0,6<--0,3------->0,6
=> \(\left\{{}\begin{matrix}m_{H_2O}=0,6.18=10,8\left(g\right)\\m_{H_2\left(dư\right)}=\left(0,7-0,6\right).2=0,2\left(g\right)\end{matrix}\right.\)
Dẫn 1,68 lít hỗn hợp khí X gồm hai hiđrocacbon vào bình đựng dung dịch brom (dư). Sau khi phản ứng xảy ra hoàn toàn, có 4 gam brom đã phản ứng và còn lại 1,12 lít khí. Nếu đốt cháy hoàn toàn 1,68 lít X thì sinh ra 2,8 lít khí CO2. Công thức phân tử của hai hiđrocacbon là (biết các thể tích khí đều đo ở đktc)
A. CH4 và C2H4
A. CH4 và C2H4
C. CH4 và C3H6
D. C2H6 và C3H6
Chọn đáp án C
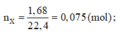
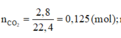
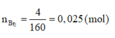
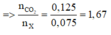
=> có một khí là CH4
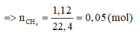
=> số mol khí còn lại trong X là : 0,075 – 0,05 = 0,025 (mol) = nBr2
=> Gọi CTPT của anken là CnH2n: 0,025 (mol)
BTNT C => 0,025n + 0,05 = 0,125
=> n = 3 => C3H6
Vậy hỗn hợp X gồm CH4 và C3H6
Dẫn 1,68 lít hỗn hợp khí X gồm hai hiđrocacbon vào bình đựng dung dịch brom (dư). Sau khi phản ứng xảy ra hoàn toàn, có 4 gam brom đã phản ứng và còn lại 1,12 lít khí. Nếu đốt cháy hoàn toàn 1,68 lít X thì sinh ra 2,8 lít khí CO2. Biết các thể tích khí đều đo ở đktc. Công thức phân tử của hai hiđrocacbon là):
A. C2H6 và C3H6
B. CH4 và C3H6
C. CH4 và C3H4
D. CH4 và C2H4
Dẫn 1,68 lít hỗn hợp khí X gồm hai hiđrocacbon vào bình đựng dung dịch brom (dư). Sau khi phản ứng xảy ra hoàn toàn, có 4 gam brom đã phản ứng và còn lại 1,12 lít khí. Nếu đốt cháy hoàn toàn 1,68 lít X thì sinh ra 2,8 lít khí CO2. Công thức phân tử của hai hiđrocacbon là (biết các thể tích khí đều đo ở đktc)
A. CH4 và C2H4
B. CH4 và C3H4
C. CH4 và C3H6
D. C2H6 và C3H6
Chọn đáp án C

=> có một khí là CH4 ⇒ n C H 4 = 1 , 12 22 , 4 = 0 , 05 (mol)
=> số mol khí còn lại trong X là : 0,075 – 0,05 = 0,025 (mol) = nBr2
=> Gọi CTPT của anken là CnH2n: 0,025 (mol)
BTNT C => 0,025n + 0,05 = 0,125
=> n = 3 => C3H6
Vậy hỗn hợp X gồm CH4 và C3H6