Đốt cháy 125g quặng pirit sắt ( chứa 96% là FeS, còn lại là tạp chất trơ ) trong oxi dư thu được sắt (III) axit và khí sunfuro. Tính thể tích khí sunfuro
Giúp mình với ạ
đốt cháy 125g quặng pirit sắt (FeS2) chứa 10% tạp chất trong oxi thì đc sắt (III) oxit và khí sunfuro. hãy tính thể tích sunfuro thu được (ở đktc)
Do quặng chứa 10% tạp chất
=> FeS2 chiếm 90%
\(m_{FeS_2}=\dfrac{125.90}{100}=112,5\left(g\right)\)
=> \(n_{FeS_2}=\dfrac{112,5}{120}=0,9375\left(mol\right)\)
PTHH: 4FeS2 + 11O2 --to--> 2Fe2O3 + 8SO2
0,9375---------------------->1,875
=> VSO2 = 1,875.22,4 = 42 (l)
Đốt cháy 400g quặng Pirit sắt (FeS2) chứa 10% tạp chất trong khí O2. Thu được SO2 và Fe2O3. a) Tính thể tích SO2 (đktc) b) Phân loại 2 oxit tạo thành
\(m_{FeS_2}=400.\left(100-10\right)\%=360\left(g\right)\\ \rightarrow n_{FeS_2}=\dfrac{360}{120}=3\left(mol\right)\)
PTHH: 4FeS2 + 11O2 --to--> 2Fe2O3 + 8SO2
3 3
\(\rightarrow V_{SO_2}=6.22,4=134,4\left(l\right)\)
Fe2O3 oxit bazo, SO2 oxit axit
Đốt cháy 125g quặng pirit sắt chứa 4% tạp chất trong oxi thì được sắt (III) oxit và khí sunfurơ. Thể tích khí sunfurơ thu được là bao nhiêu lít?
\(m_{FeS_2}=125.\left(1-4\%\right)=120\left(g\right)\)
\(n_{FeS_2}=\frac{m_{FeS_2}}{M_{FeS_2}}=\frac{120}{120}=1\left(mol\right)\)
\(PTHH:4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\)
\(Theo\) \(PTHH,\) \(ta có:\)
\(n_{SO_2}=\frac{8}{4}n_{FeS_2}=2n_{FeS_2}=2.1=2\left(mol\right)\)
\(V_{SO_2}=n_{SO_2}.22,4=2.22,4=44,8\left(l\right)\)
Để sản xuất axit sunfuric, người ta dung nhiên liệu là quặng pirit sắt ( F e S 2 ) đem nghiền nhỏ rồi nung ở nhiệt độ cao thu được sắt III oxit ( F e 2 O 3 ) và khí sunfuro ( S O 2 ) . Oxi hóa có V 2 O 5 làm xúc tác ở nhiệt độ 450 ° C thu được S O 3 , cho S O 3 hợp với nước thu được axit sunfuric ( H 2 S O 4 ) . Hãy xác định đâu là hiện tượng vật lý, đâu là hiện tượng hóa học?
- Hiện tượng vật lý: nghiền nhỏ quặng pirit sắt ( F e S 2 )
- Hiện tượng hóa học:
+Quặng pirit sắt cháy tạo thành F e 2 O 3 và S O 2
+Oxi hóa S O 2 thành S O 3
+Hợp chất nước và S O 3 tạo thành axit sunfuric ( H 2 S O 4 )
Đốt cháy hoàn toàn m gam quặng pirit sắt (chứa 80% FeS2 về khối lượng, còn lại là tạp chất trơ) bằng một lượng oxi dư. Lấy toàn bộ lượng SO2 thu được cho hấp thụ hết vào 100ml dung dịch X chứa Ba(OH)2 1,5M và NaOH 1M thì thu được 26,04 gam kết tủa. Giá trị lớn nhất của m là
A. 13,44
B. 18,99
C. 16,80
D. 21,00
Đáp án C
![]()
Vì ![]() nên chỉ có hai trường hợp là SO2 thiếu hoặc phản ứng tạo hai muối. Đề bài yêu cầu tìm giá trị lớn nhất của m nên khi cho SO2 vào dung dịch X sẽ tạo hai muối
H
S
O
-
3
và
S
O
2
-
3
nên chỉ có hai trường hợp là SO2 thiếu hoặc phản ứng tạo hai muối. Đề bài yêu cầu tìm giá trị lớn nhất của m nên khi cho SO2 vào dung dịch X sẽ tạo hai muối
H
S
O
-
3
và
S
O
2
-
3
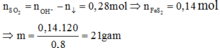
Đốt cháy hoàn toàn m gam quặng pirit sắt (chứa 80% FeS2 về khối lượng, còn lại là tạp chất trơ) bằng một lượng oxi dư. Lấy toàn bộ lượng SO2 thu được cho hấp thụ hết vào 100ml dung dịch X chứa Ba(OH)2 1,5M và NaOH 1M thì thu được 26,04 gam kết tủa. Giá trị lớn nhất của m là:
A. 13,44
B. 18,99
C. 16,80
D. 21,00
Đáp án C
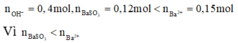
nên chỉ có hai trường hợp là SO2 thiếu hoặc phản ứng tạo hai muối. Đề bài yêu cầu tìm giá trị lớn nhất của m nên khi cho SO2 vào dung dịch

Hãy viết phương trình bằng chữ biểu diễn hiện tượng được mô tả sau đây :
Quặng pirit sắt ( F e S 2 ) được nghiền nhỏ rồi đưa vào lò nung, thu được một chất rắn màu đen (sắt III oxit) và khí có mùi hắc (khí sunfuro).
đốt cháy 250g quặng pirit sắt chứa 4% tạp chất trong oxi thì đc sắt III oxit Fe2O3 và khí sunfuro
a) Viết PTHH
b) tính thể tích khí sunfuro thu đc ( ở đktc)
c) Phân loại các loại oxit tạo thành
giúp mkvs còn nhìu bài lắm
a) PTHH:
4FeS2 + 11O2 \(\rightarrow\) 2Fe2O3 + 8SO2
b)
ta có lượng FeS2 nguyên chất : mFeS2 = \(\dfrac{250.96}{100}=240\left(g\right)\)
=> nFeS2 = \(\dfrac{240}{120}=2\left(mol\right)\)
thể tích khí sunfuro thu được là :
VO2 = \(\dfrac{2.8}{4}.22,4=89,6\left(l\right)\)
c) Fe2O3 : oxit bazo
SO2 : oxit axit
a) mFeS2 sao khi loại bỏ tạp chất = 250 . (100% - 4%) = 240 (g)
=> nFeS2 = \(\frac{240}{120}=2\) mol
Pt: 4FeS2 + 11O2 --to--> 2Fe2O3 + 8SO2
.......2 mol----------------------------> 4 mol
b) VSO2 = 4 . 22,4 = 89,6 (lít)
c) Fe2O3 : oxit bazơ
.....SO2 : oxit axit
1) Đốt cháy sắt thu được 0,3 mol Fe3O4.Tính thể tích khí oxi (ở đktc) đã dùng
2) Đốt cháy sắt thu được 0,2 mol Fe3O4. Thể tích khí oxi (ở đktc ) đã dùng là bao nhiêu ?
3) Trong x gam quặng sắt hematit có chứa 5,6g Fe. Khối lượng Fe2O3 có trong quặng đó là:
4) Muốn điều chế được 3,36 lít oxi (đktc) thì khối lượngKMnO4 cần nhiệt phân là bao nhiêu, viết phương trình điều chế.
5) Trong oxit, kim loại có hóa trị III và chiếm 70 phần trăm về khối lượng là:
6) Cho 28,4g điphotpho pentaoxit P2O5 vào cốc chứa 90g nước để tạo thành axit photphoric. Tính khới lượng axit H3PO4 được tạo thành ?
3Fe+2O2-to>Fe3O4
0,9-----0,6--------------0,3
=>VO2=0,6.22,4=13,44l
2
3Fe+2O2-to>Fe3O4
0,4--------0,2
=>VO2=0,4.22,4=8,96l