Nguyên tử của nguyên tố X có tổng số hạt là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12. Xác định số hạt proton, electron và notron trong X.

Những câu hỏi liên quan
Nguyên tử (A) có tổng số proton, nơtron, electron là 94 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Xác định số hạt electron, proton, notron và xác định tên nguyên tố và kí hiệu nguyên tử của A?
ta có
P+E+N=94 =>2P+N=94
P+E-N=22 => 2P-N=22
=> P=E=29,N = 36
=> A là kim loại đồng (Cu)
Đúng 3
Bình luận (1)
tổng số hạt proton notron và electron trong 2 nguyên tử X và Y là 134. trong đó tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 38.Số hạt mang điện trong nguyên tử Y nhiều hơn số hạt mang điện trong nguyên tử X là 18. Xác định thành phần nguyên tử cửa X và Y
Tổng số hạt proton notron và electron trong 2 nguyên tử X và Y là 134
\(2\left(p_X+p_Y\right)+n_X+n_Y=134\left(1\right)\)
Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 38
\(2\left(p_X+p_Y\right)-\left(n_X+n_Y\right)=38\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(p_X+p_Y=43\left(3\right)\)
\(n_X+n_Y=48\)
Số hạt mang điện trong nguyên tử Y nhiều hơn số hạt mang điện trong nguyên tử X là 18
\(2p_Y-2p_X=18\left(4\right)\)
\(\left(3\right),\left(4\right):\)
\(p_X=17,p_Y=26\)
Đề này tính được số proton thoi em nhé !
Đúng 5
Bình luận (0)
Tổng số hạt của nguyên tử X là 40 trong đó số hạt mang điện nhiều hơn số hạt không mang điện lá 12. Tìm số hạt proton, notron , electron trong nguyên tử X.
Gọi số hạt proton = số hạt electron = p
Gọi số hạt notron = n
Ta có :
Tổng số hạt : 2p + n = 40
Hạt mang điện nhiều hơn không mang điện là 12 : 2p - n = 12
Suy ra p = 13 ; n = 14
Vậy có 13 hạt proton, 13 hạt electron và 14 hạt notron
Đúng 10
Bình luận (5)
Gọi số hạt proton = Số hạt electron = p
Gọi số hạt notron = n
Hạt mang điện là proton, electron
Hạt không mang điện là notron
Bài 1 :
Ta có :
2p+n=402�+�=40 và 2p−n=122�−�=12
Suy ra p = 13 ; n = 14
Bài 2 :
Ta có :
2p+n=582�+�=58 và n−p=1�−�=1
Suy ra p = 19 ; n = 20
Bài 3 :
Ta có :
2p+n=482�+�=48 và 2p=2n2�=2�
Suy ra p = n = 16
Đúng 0
Bình luận (0)
Bài 1: Nguyên tử của nguyên tố hóa học X có tổng các hạt proton, electron, notron bằng 58, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 18 hạt. Xác định tên của nguyên tố X.
Theo đề ta có: số e+số p+số n=58
Mà số e=số p nên: 2.(số e)+số n=58 (1)
Ta lại có số hạt mang điện nhiều hơn hạt không mang điên là 18 hạt nên:
số e-số n=18 (2)
Công 2 vế (1) và (2) ta được:
3.(số e)=76
=>số e = số p =76:3 gần =25
=>X là Mn
Hình như là vậy tại quên òi
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Tổng số hạt proton , notron và electron trong hai nguyên tử phi kim X và Y là 76 . Trong đó tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 24 . Tổng số hạt mang điên của nguyên tử Y nhiều hơn tổng số hạt mang điện của nguyên tử X là 18 . Xác định 2 kim loại X và Y.
Gọi tổng số hạt proton , electron , notron của 2 nguyên tử X và Y là M
gọi số proton , electron , notron của M lần lượt là p ,e ,n . TA CÓ :
p+e+n = 76 => 2p + n = 76 ( vì nguyên tử trung hòa về điện) (1)
do tổng số hạt mang điện tích lớn hơn tổng số hạt không mang điện tích là 24 hạt
=> 2p - n = 24
Kết hợp (1) ta được 2p = 50 => tổng số hạt mang điện tích của 2 nguyên tử X và Y là 50 hạt (*)
Từ đề ra ta lại có :
số hạt mang điện(Y) - số hạt mang điện(X) = 18(**)
Từ (*) và (**) => số hạt mang điện của Y = 34 (hạt) => Y có 17 proton => Y là nguyên tố Clo
=> số hạt mang điện của X = 16 (hạt) => X có 8 proton => X là nguyên tố Oxi
Đúng 0
Bình luận (1)
Nguyên tử nguyên tố x có tổng số hạt proton notron electron là 34 hạt trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10 hạt
a, xác định nguyên tố x
b, tính khối lượng bằng gam của một nguyên tử x biết khối lượng của một nguyên tử C là 1,9926×10^_23 gam và nguyên tử khối của Cacbon bằng 12 dvc
Xem chi tiết
a, Gọi số proton, electron và notron của X lần lượt là p;e;n
Theo gt ta có:
\(\left\{{}\begin{matrix}2p+n=34\\2p-n=10\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p=11\\n=12\end{matrix}\right.\)
Vậy X là Na
b, Ta có: $m_{Na}=23.1,9926.10^{-23}:12=3,819.10^{-23}$
Đúng 1
Bình luận (0)
Nguyên tử X có số hạt p, n, e là 34 → p + n + e = 34 → 2p + n = 34 (1)
Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 10 → p + e – n = 10 → 2p – n = 10 (2)
Từ (1) và (2) → p = 11, n = 12
Số khối A = p + n = 11 + 12 = 23
Đúng 0
Bình luận (0)
Trong nguyên tử nguyên tố X có tổng số hạt proton , notron , electron là 34. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10 hạt. Số hiệ nguyên tử của X là :
A. 11
B. 23
C. 12
D. 17
Đáp án : A
Đặt Z;N là số p ; số n của X ta có :
2Z + N = 31 và 2Z – N = 10
=> Z = 11 ; N = 12
Đúng 0
Bình luận (0)
Tổng số hạt proton,notron,electron của nguyên tử nguyên tố x là 60 trong đó số hạt không mang điện tích ít hơn số hạt mang điện là 20.Xác định Z,A và viết kí hiệu của nguyên tố x
Ta có: \(\left\{{}\begin{matrix}p+e+n=60\\p=e\\p+e-n=20\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2n=40\\p=e\\p+e-n=20\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}p=e=20\\n=20\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=z=20\\n=20\end{matrix}\right.\)
\(\Rightarrow A=z+n=20+20=40\left(u\right)\)
\(KHNT:^{40}_{20}Ca\)
Đúng 0
Bình luận (0)
\(\left\{{}\begin{matrix}2Z+N=60\\2Z-n=20\end{matrix}\right.\)
\(\Rightarrow\)\(\left\{{}\begin{matrix}Z=20\\N=20\end{matrix}\right.\)
\(\Rightarrow\)\(A=Z+N=20+20=40u\)
Kí hiệu nguyên tử \(^{40}_{20}X\)
Đúng 0
Bình luận (0)
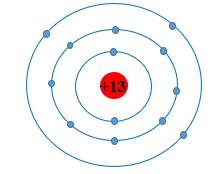
tổng số hạt proton,nơtron,electron của một nguyên tố x là 40,trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.xác định số p,số n, số e của x và vẽ sơ đồ cấu tạo nguyên tử của nguyên tố x.
Ta có :
Tổng số hạt : 2p + n = 40
Hạt mang điện nhiều hơn không mang điện là 12 : 2p - n = 12
Suy ra p = 13 ; n = 14
Vậy có 13 hạt proton, 13 hạt electron và 14 hạt notron.
------
Đúng 0
Bình luận (1)
`#3107.101107`
Gọi số hạt proton, neutron, electron trong nguyên tử nguyên tố x lần lượt là `p, n, e`
Tổng số hạt trong nguyên tử nguyên tố x là `40`
`=> p + n + e = 40`
Mà trong nguyên tử, số `p = e`
`=> 2p + n = 40`
Số hạt mang điện nhiều hơn số hạt không mang điện là `12`
`=> 2p - n = 12`
`=> n = 2p - 12`
Ta có:
`2p + n = 40`
`=> 2p + 2p - 12 = 40`
`=> 4p = 40 + 12`
`=> 4p = 52`
`=> p = 13 => p = e = 13`
Số hạt neutron có trong nguyên tử nguyên tố x là:
`n = 13 * 2 - 12 = 14`
Vậy, số `p, n, e` có trong nguyên tử nguyên tố x lần lượt là `13; 14; 13.`
Bạn tham khảo sơ đồ cấu tạo nguyên tố x:
Đúng 2
Bình luận (0)
































