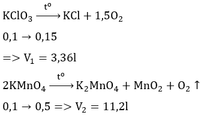Viết các phản ứng hóa học thường dùng để điều chế O2 trong phòng thí nghiệm

Những câu hỏi liên quan
Trong phòng thí nghiệm người ta điều chế CuO=cách dùng O2 oxi hóa Cu ở nhiệt độ cao
a Tính số gam Cu và O2 cần đung để điều chế 2,4g CuO
b Tính số gam KCIO3 cần dùng để điều chế lượng O2 cần dùng cho phản ứng trên
a, Ta có: \(n_{CuO}=\dfrac{2,4}{80}=0,03\left(mol\right)\)
PT: \(2Cu+O_2\underrightarrow{t^o}2CuO\)
____0,03_0,015___0,03 (mol)
\(\Rightarrow m_{Cu}=0,03.64=1,92\left(g\right)\)
\(m_{O_2}=0,015.32=0,48\left(g\right)\)
b, \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
Theo PT: \(n_{KClO_3}=\dfrac{2}{3}n_{O_2}=0,01\left(mol\right)\Rightarrow m_{KClO_3}=0,01.122,5=1,225\left(g\right)\)
Đúng 2
Bình luận (0)
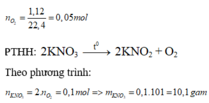
Trong phòng thí nghiệm, người ta thường dùng muối KN
O
3
để điều chế khí oxi bằng phản ứng phân hủy. Để điều chế 1,12 lít khí
O
2
(đktc) thì khối lượng muối cần dùng là A. 20,2 gam B. 10,1 gam C. 5,05 gam D. 7,07 gam
Đọc tiếp
Trong phòng thí nghiệm, người ta thường dùng muối KN O 3 để điều chế khí oxi bằng phản ứng phân hủy. Để điều chế 1,12 lít khí O 2 (đktc) thì khối lượng muối cần dùng là
A. 20,2 gam
B. 10,1 gam
C. 5,05 gam
D. 7,07 gam
Phản ứng hoá học dưới đây có thể được dùng để điều chế hidro trong phòng thí nghiệm?
2
H
2
O
→
đ
i
ệ
n
p
h
â
n
2
H
2
↑
+
O
2
↑
Đọc tiếp
Phản ứng hoá học dưới đây có thể được dùng để điều chế hidro trong phòng thí nghiệm?
2 H 2 O → đ i ệ n p h â n 2 H 2 ↑ + O 2 ↑
Phản ứng này không thể dùng để điều chế hidro trong phòng thí nghiệm
Đúng 0
Bình luận (0)
a) Trình bày thí nghiệm điều chế H2 trong phòng thí nghiệm. Viết phương trình phản ứng (nếu có)?
b) Trình bày thí nghiệm điều chế O2 trong phòng thí nghiệm. Viết phương trình phản ứng (nếu có)?
a. – Trong phòng thí nghiệm để điều chế H2 thường sử dụng axit HCl (hoặc H2SO4 loãng) và kim loại Zn (hoặc Fe, hoặc Al).
Zn + 2HCl → ZnCl2 + H2↑
– Khí H2 ít tan trong nước và nhẹ hơn không khí nên ta có thể thu H2 theo 2 cách: Đẩy nước và đẩy không khí.
b. – Trong phòng thí nghiệm, người ta điều chế khí oxi bằng cách đun nóng những hợp chất giàu oxi và dễ phân hủy ở nhiệt độ cao.
2KMnO4 ---t° → K2MnO4 + MnO2 + O2
2KClO3 ---t° → 2KCl + 3O2
– Khí O2 ít tan trong nước và nặng hơn không khí nên ta có thể thu O2 theo 2 cách: Đẩy nước và đẩy không khí.
Đúng 0
Bình luận (0)
Thực hiện các phản ứng sau:
(
a
)
2
K
C
l
O
3
→
t
o
2
K
C
l
+
3
O
2
(
b
)
2
K
M
n
O
4
→
t
o
K
2
M
n
O
4...
Đọc tiếp
Thực hiện các phản ứng sau:
( a ) 2 K C l O 3 → t o 2 K C l + 3 O 2 ( b ) 2 K M n O 4 → t o K 2 M n O 4 + M n O 2 + O 2 ( c ) 2 H 2 O → đ i ệ n p h â n 2 H 2 + O 2
(d) 2 Cu(NO3)2 → t o 2CuO+ 4NO2 + O2
Có bao nhiêu trường hợp thường dùng để điều chế oxi trong phòng thí nghiệm?
A. 2
B. 4
C. 3
D. 5
Trong phòng thí nghiệm có thể dùng muối KClO3 hoặc KMnO4 để điều chế oxi bằng phản ứng phân hủy. Viết phương trình hóa học của các phản ứng và tính thể tích khí oxi thu được (đktc) khi nhiệt phân hoàn toàn 0,1 mol mỗi chất trên.
Trong phòng thí nghiệm, quá trình điều chế khí Z thường bị lẫn SO2. Để loại bỏ SO2 ra khỏi hỗn hợp khí gồm Z và SO2, có thể dùng dung dịch chứa chất nào trong các chất ( riêng biệt) sau đây: BaCl2, Ca(OH)2, Br2 và K2SO3? Giải thích và viết phương trình hóa học minh họa cho các phản ứng.
Trong phòng thí nghiệm, quá trình điều chế khí Z thường bị lẫn SO2 nên Z là C2H4.
Vậy để tách SO2 ra khỏi hỗn hợp C2H4 và SO2 ta có thể dùng các chất: Ca(OH)2, K2SO3.
PTHH:
SO2 + Ca(OH)2 → CaSO3↓ + H2O
K2SO3 + SO2 + H2O → 2KHSO3
Đúng 0
Bình luận (0)
Phương trình hóa học nào dưới đây thường dùng để điều chế SO2 trong phòng thí nghiệm?
Đọc tiếp
Phương trình hóa học nào dưới đây thường dùng để điều chế SO2 trong phòng thí nghiệm?
![]()
![]()
![]()
![]()
Trong phòng thí nghiệm có các hóa chất KClO3 , MnO2 và dụng cụ cần thiết
a, Viết phương trình hóa học của phản ứng điều chế khí oxi
b, Hãy vẽ hình mô tả thí nghiệm điều chế và thu khí oxi bằng cách đẩy không khí
a) 2KClO3 -> 2KCl + 3O2
b) MnO2 + 4HCl -> MnCl2 + Cl2 + 2H2O
b) SGK
Đúng 0
Bình luận (1)
Trong các phản ứng sau, phản ứng nào có thể dùng để điều chế
SO
2
trong phòng thí nghiệm?
Đọc tiếp
Trong các phản ứng sau, phản ứng nào có thể dùng để điều chế SO 2 trong phòng thí nghiệm?
![]()
![]()
![]()
![]()
Đáp án C
Trong phòng thí nghiệm, SO 2 được điều chế bằng cách đun nóng dung dịch H 2 SO 4 với muối Na 2 SO 3 :
Na 2 SO 3 + H 2 SO 4 → Na 2 SO 4 + SO 2 ↑ + H 2 O
Đúng 0
Bình luận (0)