35. Cho 15g MnO2 ( chứa 13% tạp chất trơ) tác dụng hết với dd HCl đặc dư , khí thoát ra đc hấp thụ hết vào 400ml dd NaOH 1M ở nhiệt độ thường. Tổng nồng độ mol /l của muối tạo thành?

Những câu hỏi liên quan
Cho MnO2 tác dụng hoàn toàn với 20g dd HCl 36,5%. Khí thoát ra được hấp thụ hết vào 500ml dd KOH 2M ở nhiệt độ thường tạo ra dd A. Tính nồng độ mol chất tan trong dd A.
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
nHCl = \(\dfrac{20.36,5\%}{36,5}\)= 0,2 mol => nCl2 = 0,2 : 4 = 0,05 mol
Cl2 + 2KOH →KCl + KClO + H2O
nKOH = 0,5.2 = 1 mol
=> KOH dư , Cl2 hết
nKOH dư = 1 - 0,05.2 = 0,9 mol
dung dịch A gồm KCl và KClO có số mol = nCl2 = 0,05 mol và KOH dư 0,9mol
CKCl = CKClO = \(\dfrac{0,05}{0,5}\)=0,1 M
CKOH dư = \(\dfrac{0,9}{0,5}\)= 1,8 M
Đúng 1
Bình luận (0)
1. cho một lượng đơn chất halogen A tác dụng hết với Mg thu đc 9,5g muối. Nếu cho lượng halogen trên tác dụng hết với Al thu đc 8,9g muối. Halogen A là?
2.sục khí clo vào dd NaBr và NaI đến phản ứng hoàn toàn thu đc 1.17g NaCl. Xác định số mol hh NaBr và NaI có trong dd ban đầu?
3.cho 13.05g MnO2 td với dd HCl đặc dư khí thoát ra đc hấp thụ hết vào 400ml dd NaOH 1M ở nhiệt độ thường. Nồng độ mol/l của muối tạo thành là?
4.cho 2.13g hỗn hợp X gồm Mg, Cu, Al ở dạng bột td hoàn toàn với oxi thu...
Đọc tiếp
1. cho một lượng đơn chất halogen A tác dụng hết với Mg thu đc 9,5g muối. Nếu cho lượng halogen trên tác dụng hết với Al thu đc 8,9g muối. Halogen A là?
2.sục khí clo vào dd NaBr và NaI đến phản ứng hoàn toàn thu đc 1.17g NaCl. Xác định số mol hh NaBr và NaI có trong dd ban đầu?
3.cho 13.05g MnO2 td với dd HCl đặc dư khí thoát ra đc hấp thụ hết vào 400ml dd NaOH 1M ở nhiệt độ thường. Nồng độ mol/l của muối tạo thành là?
4.cho 2.13g hỗn hợp X gồm Mg, Cu, Al ở dạng bột td hoàn toàn với oxi thu đc hỗn hợp Y gồm các oxit có khối lượng 3.33g. V dd HCl 2M vừa đủ để pư hết với Y là?
Giúp nhanh với ạ
PTHH ( I ) : \(MnO_2+4HCl\rightarrow2H_2O+Cl_2+MnCl_2\)
\(n_{MnO2}=\frac{m_{MnO2}}{M_{MnO2}}=\frac{13,05}{87}=0,15\left(mol\right)\)
- Theo PTHH ( I ) : \(n_{Cl2}=n_{MnO2}=0,15\left(mol\right)\)
\(n_{NaOH}=C_{MNaOH}.V_{NaOH}=1.0,4=0,4\left(mol\right)\)
PTHH ( II ) :....... \(Cl_2+2NaOH\rightarrow NaClO+NaCl+H_2O\)
Trước phản ứng : 0,15......0,4
Trong phản ứng :0,15.......0,3
Sau phản ứng : ....0...........0,1
=> Sau phản ứng Cl2 hết, NaOH dư ( dư 01 mol )
Nên sau phản ứng thu được dung dịch NaOH dư, NaClO, NaCl .
Theo PTHH ( II ) : \(n_{NaCl}=n_{NaClO}=n_{Cl2}=0,15\left(mol\right)\)
=> \(\left\{{}\begin{matrix}C_{MNaOH}=\frac{n_{NaOH}}{V}=\frac{0,1}{0,4}=0,25M\\C_{MNaClO}=\frac{n_{NaClO}}{V}=\frac{0,15}{0,4}=0,375M\\C_{MNaCl}=\frac{n_{NaCl}}{V}=\frac{0,15}{0,4}=0,375M\end{matrix}\right.\)
Bài 1. Gọi A là X2
Mg + X2 → MgX2
2Al + 3X2→ 2AlX3
Bảo toàn nguyên tố X:
2nMgX2 = 3nAlX3 ⇒ 2.9,5/(24 + 2X) = 3.8,9/(27 + 31X) ⇒ X = 35,5 (Cl)
Bài 2. Áp dụng định luật bảo toàn khối lượng:
\(n_{NaBr}+n_{NaI}=n_{NaCl}=\frac{1,17}{58,5}=0,02mol\)
Xem thêm câu trả lời
Cho 69,6 gam MnO2 tác dụng với dd HCl đặc, dư. Dẫn khí thoát ra đi vào 500ml dd KOH 4M (ở nhiệt độ thường). Xác định nồng độ mol các chất trong dung dịch sau phản ứng (thể tích dd thay đổi không đáng kể).
\(n_{MnO_2}=\dfrac{69,6}{87}=0,8\left(mol\right)\)
nKOH = 0,5.4 = 2(mol)
PTHH: MnO2 + 4HCl --> MnCl2 + Cl2 + 2H2O
0,8------------------------>0,8
2KOH + Cl2 --> KCl + KClO + H2O
Xét tỉ lệ \(\dfrac{2}{2}>\dfrac{0,8}{1}\) => KOH dư, Cl2 hết
2KOH + Cl2 --> KCl + KClO + H2O
1,6<--0,8---->0,8---->0,8
=> \(\left\{{}\begin{matrix}n_{KOH\left(dư\right)}=2-1,6=0,4\left(mol\right)\\n_{KCl}=0,8\left(mol\right)\\n_{KClO}=0,8\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(KOH\right)}=\dfrac{0,4}{0,5}=0,8M\\C_{M\left(KCl\right)}=\dfrac{0,8}{0,5}=1,6M\\C_{M\left(KClO\right)}=\dfrac{0,8}{0,5}=1,6M\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho 17,4 gam MnO 2 tác dụng hết với dung dịch HCl. Toàn bộ khí cu sinh ra được hấp thụ hết vào 145,8 gam dung dịch NaOH 20% ở nhiệt độ thường tạo ra dung dịch A. Hỏi dung dịch A có chứa những chất tan nào ? Tính nồng độ % của từng chất tan đó.
MnO 2 + HCl → MnCl 2 + Cl 2 + 2 H 2 O
Cl 2 + 2NaOH → NaCl + NaClO + H 2 O
n MnO 2 = 0,2 mol; n NaOH = 0,729 mol
Theo phương trình (1) ta có: n Cl 2 = n MnO 2 = 0,2 mol
Theo phương trình (2) ta có: 2 n Cl 2 < n NaOH ⇒ NaOH dư
Dung dịch A gồm: n NaCl = n NaClO = n Cl 2 = 0,2 mol
n NaOH dư = 0,729 – 2.0,2 = 0,329 mol
m dd A = m Cl 2 + m dd NaOH = 0,2.71 + 145,8 = 160g
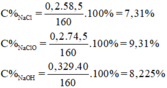
Đúng 0
Bình luận (0)
Cho 13,05 gam MnO2 tác dụng hoàn toàn với dd HCl đặc . Toàn bộ khí clo sinh ra được hấp thụ hết vào 500ml dd NaOH 1M ( ở nhiệt độ thường). Hãy xác định nồng độ mol của từng chất trong dung dịch sau phản ứng . Coi thể tích dung dịch không đổi ( Na= 23 ; Mn=55 ; O=16)
Phản ứng xảy ra:
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
Ta có:
\(n_{MnO2}=\frac{13,05}{55+16.2}=0,15\left(mol\right)\)
\(\Rightarrow n_{Cl2}=n_{MnO2}=0,15\left(mol\right)\)
\(2NaOH+Cl_2\rightarrow NaCl+NaClO+H_2O\)
Vì \(n_{NaOH}=0,5.1=0,5\left(mol\right)>2nCl_2\)
Nên NaOH dư.
\(\Rightarrow n_{NaCl}=n_{NaClO}=n_{Cl2}=0,15\left(mol\right)\)
\(n_{NaOH\left(Dư\right)}=0,5-0,15.2=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}CM_{NaCl}=\frac{0,15}{0,5}=0,3M\\CM_{NaClO}=\frac{0,15}{0,5}=0,3M\\CM_{NaOH\left(dư\right)}=\frac{0,2}{0,5}=0,4M\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 16.25 gam bột kẽm vào 500ml dd HCl a) Viết PTHH xảy ra? b) Tính thể tích khí hiđro thoát ra ở đktc? c) Tính nồng độ mol/l của axit trong dd lúc đầu? d) Cho toàn bộ lượn muối sinh ra vào 400ml dd nạo nồng độ 1M. Tính khối lượng chất rắn thu được trong dd sau PƯ?
a) $Zn + 2HCl \to ZnCl_2 + H_2$
b) Theo PTHH : $n_{H_2} = n_{Zn} = \dfrac{16,25}{65} = 0,25(mol)$
$\Rightarrow V_{H_2} = 0,25.22,4 = 5,6(lít)$
c) $n_{HCl} = 2n_{Zn} = 0,5(mol)$
$\Rightarrow C_{M_{HCl}} = \dfrac{0,5}{0,5} = 1M$
Đúng 1
Bình luận (0)
37. Cho 24,5g KCLO3 tác dụng với dd HCl đặc , dư ( hiệu suất 70%) thì thu đc V lít Cl2 ( đktc) . Hấp thụ hết V lít Cl2 vào dd NaOH loãng , vừa đủ , ở nhiệt độ thường thu đc dd X. Biết rằng dd X chứa m gam chất tan , giá trị của m là?
Phản ứng xảy ra:
\(n_{KClO3}=\frac{24,5}{39+35,5+16.3}=0,2\left(mol\right)\)
\(\Rightarrow n_{KClO2\left(pư\right)}=0,2.70\%=0,14\left(mol\right)\)
\(\Rightarrow n_{Cl2}=0,14.3=0,42\left(mol\right)\)
\(2NaOH+Cl_2\rightarrow NaCl+NaClO\)
\(\Rightarrow n_{NaCl}=n_{NaClO}=n_{Cl2}=0,42\left(mol\right)\)
\(\Rightarrow m=m_{NaCl}+m_{NaClO}=0,42.58,5+0,42.74,5=55,86\left(g\right)\)
| 6HCl | + |
KClO3 |
→ | 3Cl2 | + | 3H2O | + |
KCl |
-----------0,2----------0,6 mol
Cl2+2NaOH-->NaCl+NaClO+H2O
0,6-----------------0,6-----0,6 mol
nKClO3=24,5\122,5=0,2 mol
=>VCl2=0,6.22,4=13,44 l
=>mChất tan= 0,6.58,5+0,6.74,5=79,8 g
Cho 21,6g MnO2 tác dụng với dung dịch hcl chứa 20,072g HCL thu được khí A dẫn A qua 1 lít dd NAOH dư
a/ HCL có đủ để phản ứng hết MnO2 không ?
b/ Tính nồng độ mol của muối thu được trong Pư giữa CL và NAOH?
c/Nung quặng pirit Fe để tạo SO2, cho SO2 sục vào dd 2 muối trên sau đó thêm vào BA(NO3)2 dư. Tính khối lượng kết tủa và khối lượng quặng pirit cần dùng ?
Cho 4,35 g MnO2 tác dụng với dung dịch HCl đặc, dư. Dẫn khi thoát ra đi vào 300ml dung dịch NaOH có nồng độ 0,1 M (ở nhiệt độ thường).
a) Viết phương trình hoá học của các phản ứng xảy ra.
b) Xác định nồng độ mol của những chất có trong dung dịch sau phản ứng
Xem chi tiết
\(n_{MnO_2} = \dfrac{4,35}{87} = 0,05(mol)\)
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
0,05..................................0,05..................(mol)
\(n_{NaOH} = 0,3.0,1 = 0,03(mol)\)
2NaOH + Cl2 → NaCl + NaClO + H2O
0,03........0,05.....0,015.......0,015....................(mol)
Vậy :
\(C_{M_{NaCl}} = C_{M_{NaClO}} = \dfrac{0,015}{0,3} = 0,05M\)
Đúng 4
Bình luận (0)






















