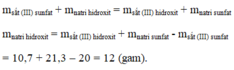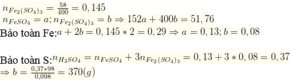Bài 1: Hòa tan 10,7 gam sắt(III) hidroxit Fe (OH)3 vào dung dịch chứa 14,7 gam axit sunfuric H2SO4 sau phản ứng thu được a gam muối sắt(III) sunfat Fe2(SO4)3 và 5,4 gam nước H2O
a. Viết công thức khối lượng của phản ứng xảy ra.
b. Khối lượng muối thu được bao nhiêu gam
Bài 2. Đốt cháy m g kim loại magie Mg trong không khí thu được 8g hợp chất magie oxit (MgO). Biết rằng khối lượng magie Mg tham gia bằng 1,5 lần khối lượng của oxi (không khí) tham gia phản ứng.
a. Viết phản ứng hóa học.
b. Tính khối lượng của Mg và oxi đã phản ứng.
Bài 3. Có các khí sau: Cl2, N2, HCl, H2S, H2
a. Những khí nào nặng hơn khí oxi (O2) và nặng hơn bao nhiêu lần?
b. Những khí nào nhẹ hơn không khí và nhẹ hơn bao nhiêu lần?
Bài 4. 16 g khí A có tỉ khối hơi đối với khí metan CH4 bằng 4.
a) Tính khối lượng mol của khí A.
b) Tính thể tích của khí A ở đktc.
Bài 5. Tính thành phần phần trăm theo khối lượng các nguyên tố hóa học có trong những hợp chất sau:
a. KClO3 b. Fe2(SO4)3
Bài 6. Xác định công thức hóa học của hợp chất X và Y biết:
a. Khối lượng mol phân tử X là 84g/mol. Thành phần theo khối lượng của X là: 28,57%Mg, 14,29%C và còn lại là O.
b. Y có thành phần % theo khối lượng như sau: Cu chiếm 40 %, S chiếm 20 % và O chiếm 40%
Bài 7. Tính số mol của
a. 3,36 lít khí CO2 (đktc)
b. 16 gam CuSO4
c. 40 gam Fe2(SO4)3
Bài 8. Tính thể tích ở đktc của
a. 0,75 mol khí H2
b. 6,8 gam khí H2S
c. Hỗn hợp gồm 3,2 gam khí O2 và 5,6 gam khí N2
Bài 9. Tính khối lượng của
a. 0,15 mol NaOH
b. 5,6 lít khí NH3 ở đktc
Bài 10. Hòa tan 14 gam kim loại Fe vào dung dịch axit clohiđric HCl, thu được sắt(II) clorua FeCl2 và khí hiđro H2
a. Tính khối lượng HCl đã dùng
b. Tính thể tích khí H2
Bài 11. PT nhiệt phân theo sơ đồ sau: KMnO4 --->K2MnO4 + MnO2 + O2
a) Tính thể tích khí oxi (đktc) thu được khi nhiệt phân 31,6 g KMnO4.
b) Tính khối lượng CuO được tạo thành khi cho lượng khí oxi sinh ra ở trên tác dụng hết với kim loiại Cu.
Bài 12. Đốt cháy hết 5,4 gam một kim loại M có hóa trị (III) trong oxi dư, thu được 10,2 gam oxit M2O3. Xác định kim loại M và viết CTHH của oxit.