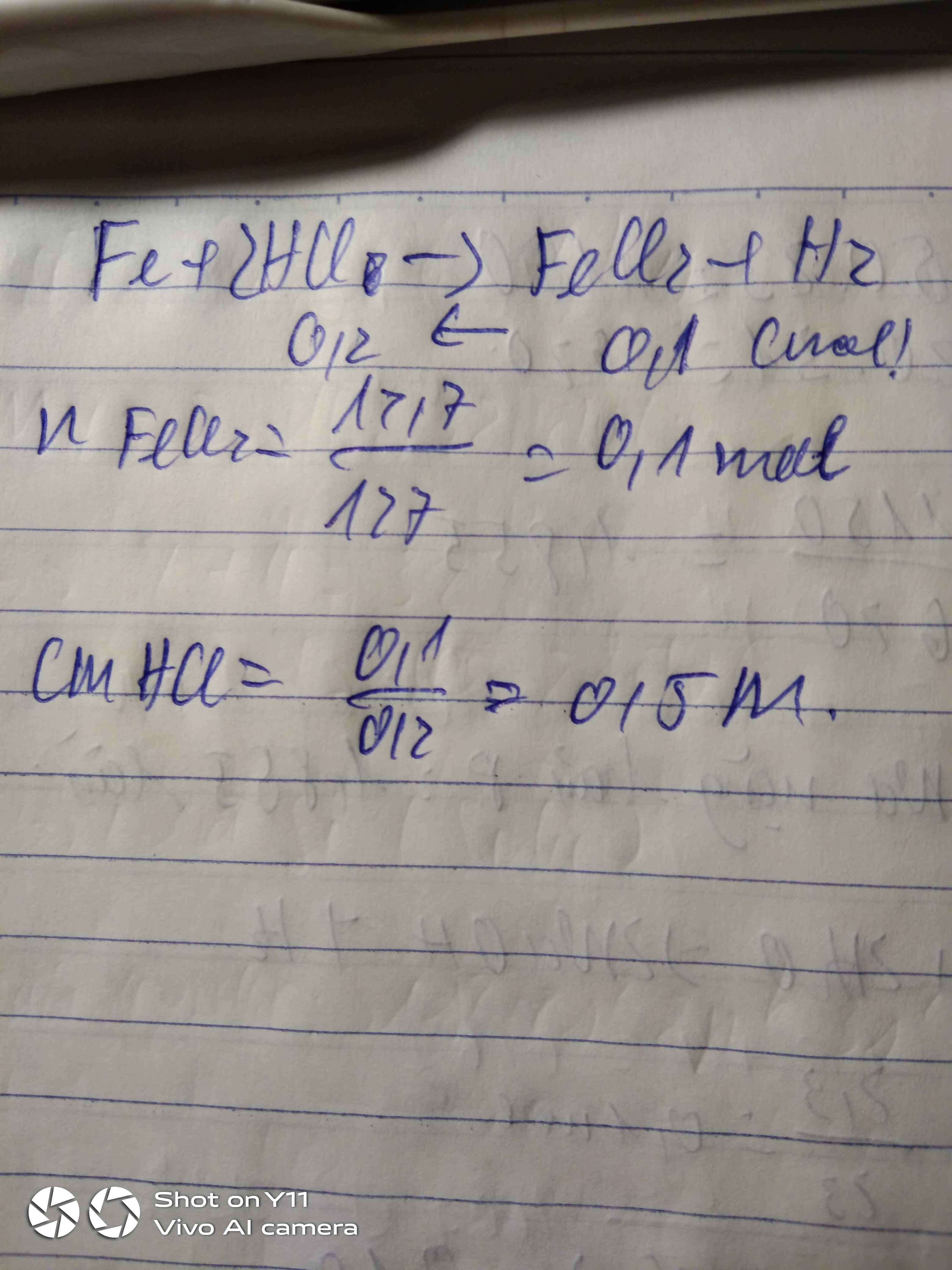Hòa tan 7,2 gam Magie trong 200 gam dd HCl vừa đủ. Tính nồng độ % dung dịch thu được và C% dung dịch HCl đã dùng.

Những câu hỏi liên quan
Bài 2: Hòa tan hoàn toàn m gam kim loại Mg cần dùng 200 gam dung dịch HCl vừa đủ được dung dịch A và 4,48 lit khí.
a. Tính m(khối lượng Mg) và C% của dung dịch HCl đã dùng.
b. Tính C% của chất tan trong dung dịch A thu được sau phản ứng.
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
a. PTHH: \(Mg+2HCl--->MgCl_2+H_2\)
Theo PT: \(n_{Mg}=n_{H_2}=0,2\left(mol\right)\)
=> \(m_{Mg}=0,2.24=4,8\left(g\right)\)
Theo PT: \(n_{HCl}=2.n_{Mg}=2.0,2=0,4\left(mol\right)\)
=> \(m_{HCl}=0,4.36.5=14,6\left(g\right)\)
=> \(C_{\%_{HCl}}=\dfrac{14,6}{200}.100\%=7,3\%\)
b. Ta có: \(m_{dd_{MgCl_2}}=4,8+200=204,8\left(g\right)\)
Theo PT: \(n_{MgCl_2}=n_{Mg}=0,2\left(mol\right)\)
=> \(m_{MgCl_2}=0,2.95=19\left(g\right)\)
=> \(C_{\%_{MgCl_2}}=\dfrac{19}{204,8}.100\%=9,28\%\)
Đúng 2
Bình luận (0)
Trộn 300 gam dd H2SO4 7,35% với 200 gam dd HCl 7,3% thu được dd X.
a) Tính nồng độ phần trăm của dung dịch X.
b) Cho 8,7 gam hỗn hợp gồm Mg và Fe hòa tan vừa đủ trong 250 gam dung dịch X trên tạo ra dung dịch Y và V lít khí hiđro. Tính V (ở đktc), tính khối lượng hỗn hợp muối có trong dung dịch Y và khối lượng của mỗi kim loại trong hỗn hợp ban đầu.
mH2SO4= \(\dfrac{300.7,35}{100}=22,05g\)
nH2SO4= \(\dfrac{22,05}{98}=0,225 mol\)
mHCl= \(\dfrac{200.7,3}{100}=14,6g\)
nHCl= \(\dfrac{14,6}{36,5}=0,4mol\)
H2SO4 + 2HCl → 2H2O + Cl2 ↑+ SO2 ↑
n trước pư 0,225 0,4
n pư 0,2 ← 0,4 → 0,4 → 0,2 → 0,2 mol
n sau pư dư 0,025 hết
a) mCl2= 0,2. 71= 14,2g
mSO2= 64. 0,2= 12,8g
mH2O= 18. 0,4=7,2g
mdd sau pư= 300 +200 -14,2 -12,8= 473g
C%dd H2O= \(\dfrac{7,2.100}{473}=1,52\)%
b) Mg + 2H2O → Mg(OH)2 + H2 ↑
x → 2x → x → x
Fe + 2H2O → Fe(OH)2 + H2↑
y → 2y → y → y
Gọi x,y lần lượt là số mol của Mg,Fe.
Ta có hệ phương trình:
24x + 56y = 8,7 x= \(\dfrac{5}{64}\)
⇒
2x + 2y = 0,4 y= \(\dfrac{39}{320}\)
VH2= 22,4. \((\dfrac{5}{64}+\dfrac{39}{320})\)= 4,48l
mhh MG(OH)2, Fe(OH)2= 8,7 +250 - 2.(\(\dfrac{5}{64}+\dfrac{39}{320}\)) = 2258,3g
mMg=24. \(\dfrac{5}{64}\)=1.875g
mFe= 8,7-1,875= 6,825g
Đúng 0
Bình luận (0)
Hòa tan một lượng sắt vừa đủ trong 200 ml dung dịch HCl thu được dung dịch chứa 12,7 gam chất tan và khí H2. Nồng độ mol của dung dịch HCl là
Ta có PT: Fe + 2HCl ---> FeCl2 + H2.
Ta có: \(n_{FeCl_2}=\dfrac{12,7}{127}=0,1\left(mol\right)\)
Theo PT: nHCl = \(2.n_{FeCl_2}=2.0,1=0,2\left(mol\right)\)
=> mHCl = 0,2 . 36,5 = 7,3(g)
Đổi 200ml = 0,2 lít
Ta có: \(C_{M_{HCl}}=\dfrac{7,3}{0,2}=36,5\)(g/mol)
Đúng 2
Bình luận (1)
1. (1,5 điểm) Hòa tan hết 36,1 gam hỗn hợp A gồm Fe và Al vào 200 mL dung dịch HCl (dùng vừa đủ).
Sau phản ứng thu được dung dịch B và 21,28 lít khí H2 (đktc). Hãy tính:
a. Khối lượng mỗi chất trong hỗn hợp A ban đầu.
b. Tính nồng độ dung dịch HCl đã dùng.
c. Tính nồng độ mol/l của chất tan trong dung dịch B.
a) PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a_____2a______a_____a (mol)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
b_____3b_______b_____\(\dfrac{3}{2}\)b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}56a+27b=36,1\\a+\dfrac{3}{2}b=\dfrac{21,28}{22,4}=0,95\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,5\\b=0,3\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,5\cdot56=28\left(g\right)\\m_{Al}=8,1\left(g\right)\end{matrix}\right.\)
b+c) Theo các PTHH: \(\left\{{}\begin{matrix}n_{HCl}=2a+3b=1,9\left(mol\right)\\n_{FeCl_2}=0,5\left(mol\right)\\n_{AlCl_3}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{HCl}}=\dfrac{1,9}{0,2}=9,5\left(M\right)\\C_{M_{FeCl_2}}=\dfrac{0,5}{0,2}=2,5\left(M\right)\\C_{M_{AlCl_3}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Hòa tan 13 gam Kẽm cần vừa đủ 500ml dung dịch HCL có nồng độ Cm a) tính nồng độ dung dịch HCL đã dùng b) tính khối lượng muối tạo thành và thể tích H2 sinh ra ở điều kiện tiêu chuẩn c) nếu cho lượng axít trên vào 200 gam dung dịch KOH 5,6% sau đó cho mẫu quỳ tím vào dung dịch thu được sau phản ứng thì màu của quỳ tím thế nào? giải thích
\(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{13}{65}=0,2mol\)
PTHH: Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
TL: 1 : 2 : 1 : 1
mol: 0,2 \(\rightarrow\) 0,1 \(\rightarrow\) 0,2 \(\rightarrow\) 0,2
đổi 500ml = 0,5 l
\(a.C_{M_{ddHCl}}=\dfrac{n_{HCl}}{V_{HCl}}=\dfrac{0,1}{0,5}=0,2M\)
\(b.m_{ZnCl_2}=n.M=0,2.136=27,2g\)
\(V_{H_2}=n.22,4=0,2.22,4=4,48l\)
c.
Màu của quỳ tím sẽ chuyển sang màu đỏ.
Giải thích:
- Phản ứng giữa axit HCl và bazơ KOH tạo ra muối KCl và nước: HCl + KOH → KCl + H2O
- Vì dung dịch KOH là bazơ, nên khi phản ứng với axit HCl thì sẽ tạo ra dung dịch muối KCl và nước.
- Muối KCl không có tính kiềm, nên dung dịch thu được sẽ có tính axit.
- Khi cho mẫu quỳ tím vào dung dịch axit, quỳ tím sẽ chuyển sang màu đỏ do tính axit của dung dịch.
Đúng 1
Bình luận (0)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2----->0,4------>0,2---->0,2
a) \(C_{MddHCl}=\dfrac{0,4}{0,5}=0,8M\)
b) \(m_{muối}=m_{ZnCl2}=0,2.136=27,2\left(g\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
c) \(n_{KOH}=\dfrac{5,6\%.200}{100\%.56}=0,2\left(mol\right)\)
Pt : \(KOH+HCl\rightarrow KCl+H_2O\)
0,2 0,4
Xét tỉ lệ : \(0,2< 0,4\Rightarrow HCldư\)
Khi cho quỳ tím vào dụng dịch sau phản ứng --> quỳ hóa đỏ (do HCl có tính axit)
Đúng 1
Bình luận (0)
Hòa tan 9,4 gam kali oxit(K2O)vào nước, thu được 200 ml dung dịch A. Hãy tính : a) Nồng độ mol của dung dịch A. b) Tính khối lượng dd HCl 10% cần dùng để trung hòa vừa đủ dd A. c) Tính thể tích khí CO2(đktc) tác dụng với dd A để thu được muối trung hòa
\(n_{K2O}=\dfrac{9,4}{94}=0,1\left(mol\right)\)
Pt : \(K_2O+H_2O\rightarrow2KOH|\)
1 1 2
0,1 0,2
a) \(n_{KOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
200ml = 0,2l
\(C_{M_{ddKOH}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
b) Pt : \(KOH+HCl\rightarrow KCl+H_2O|\)
1 1 1 1
0,1 0,1
\(n_{HCl}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{HCl}=0,1.36,5=3,65\left(g\right)\)
\(m_{ddHCl}=\dfrac{3,65.100}{10}=36,5\left(g\right)\)
c) \(CO_2+2KOH\rightarrow K_2CO_3+H_2O|\)
1 2 1 1
0,05 0,1
\(n_{CO2}=\dfrac{0,1.1}{2}=0,05\left(mol\right)\)
\(V_{CO2\left(dktc\right)}=0,05.22,4=1,12\left(l\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Hòa tan m (gam) kim loại Mg vào dung dịch hydrochloric acid HCl vừa đủ, thu được 9,916 L khí H2 (đkc).
a) Viết PTHH.
b) Tính m?
c)Tính khối lượng muối thu được.
d) Tính nồng độ mol của dd acid đã dùng.
a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b, \(n_{H_2}=\dfrac{9,916}{24,79}=0,4\left(mol\right)\)
Theo PT: \(n_{Mg}=n_{MgCl_2}=n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow m_{Mg}=0,4.24=9,6\left(g\right)\)
c, \(m_{MgCl_2}=0,4.95=38\left(g\right)\)
d, Bạn bổ sung thêm thể tích dd HCl nhé.
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 13 gam Zn cần dùng vừa đủ dung dịch axit HCl 7,3% thu được dung dịch muối X và thấy thoát ra V lít khí H2 (ở đktc) a. Tính giá trị của V? b. Tính khối lượng dung dịch axit HCl đã phản ứng? c. Tính nồng độ phần trăm của muối trong X?
a)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2-->0,4----->0,2--->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
b) mHCl = 0,4.36,5 = 14,6 (g)
=> \(m_{dd.HCl}=\dfrac{14,6.100}{7,3}=200\left(g\right)\)
c)
mdd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
mZnCl2 = 0,2.136 = 27,2 (g)
=> \(C\%=\dfrac{27,2}{212,6}.100\%=12,8\%\)
Đúng 2
Bình luận (0)
Hòa tan một lượng CaCO3 vào trong 200 gam dung dịch HCl 0.5 mol (phản ứng vừa đủ )thì sau phản ứng thu được một số dung dịch X và khí Y a) Tính khối lượng của CaCO3 đã dùng và thể tích khí Y Sinh ra ở (điều kiện tiêu chuẩn) b) tính nồng độ mol của muối trong dung dịch X