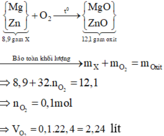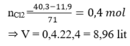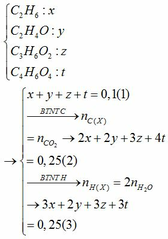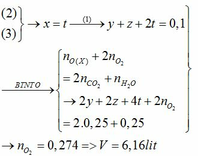Cho 50g hỗn hợp Al, Mg, Zn phản ứng hết với V lít khí O2 (đktc). Sau phản ứng thu được 74g hỗn hợp sản phẩm. Tính thể tích khí O2 đã tham gia phản ứng.

Những câu hỏi liên quan
Đốt cháy hoàn toàn 17,4 gam hỗn hợp Mg và Al trong bình kín chứa khí O2 (dư) thu được 30,2 gam hỗn hợp oxit. Thể tích khí oxi (đktc) đã tham gia phản ứng là
A. 17,92 lít
B. 4,48 lít
C. 11,20 lít
D. 8,96 lít
bài 2: Cho 5,2 g hỗn hợp gồm 3 kim loại Mg, Al ,Zn cháy hoàn toàn trong bình O2 dư 8,4 g hỗn hợp rắn .
a/viết các PTHH
b/ Tính V khí O2 đã tham gia phản ứng (đktc)
a)
$2Mg + O_2 \xrightarrow{t^o} 2MgO$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$2Zn + O_2 \xrightarrow{t^o} 2ZnO$
b)
Bảo toàn khối lượng :
$m_{O_2\ pư} = 8,4 - 5,2 = 3,2(gam)$
$n_{O_2\ pư} = \dfrac{3,2}{32} = 0,1(mol)$
$V_{O_2\ pư} = 0,1.22,4 = 2,24(lít)$
Đúng 2
Bình luận (1)
Đốt cháy hoàn toàn 3,36 lit hỗn hợp C2H4, C3H6 trong bình chứa O2 dư. Sau khi phản ứng kết thúc người ta thu được 17,6 gam khí CO2 và hơi nước
a. Tính %V mỗi khí trong hỗn hợp ban đầu
b.Tính thể tích khí O2 đã tham gia phản ứng. Các khí đo ở đktc
a) Gọi số mol C2H4, C3H6 là a, b (mol)
=> \(a+b=\dfrac{3,36}{22,4}=0,15\left(mol\right)\) (1)
\(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)\)
PTHH: C2H4 + 3O2 --to--> 2CO2 + 2H2O
a----->3a--------->2a
2C3H6 + 9O2 --to--> 6CO2 + 6H2O
b------>4,5b------->3b
=> 2a + 3b = 0,4 (2)
(1)(2) =>a = 0,05 (mol); b = 0,1 (mol)
\(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,05}{0,15}.100\%=33,33\%\\\%V_{C_3H_6}=\dfrac{0,1}{0,15}.100\%=66,67\%\end{matrix}\right.\)
b) nO2 = 3a + 4,5b = 0,6 (mol)
=> VO2 = 0,6.22,4 = 13,44 (l)
Đúng 3
Bình luận (1)
Gọi a (mol) và b (mol) lần lượt là số mol của C2H4 và C3H6, ta có:
Giả thiết: a+b=3,36/22,4=0,15 (1).
BT C: 2a+3b=17,6/44=0,4 (2).
Giải hệ phương trình gồm (1) và (2), ta suy ra a=0,05 (mol) và b=0,1 (mol).
a. %V\(C_2H_4\)=0,05/0,15.100%\(\approx\)33,33% \(\Rightarrow\) %V\(C_3H_6\)\(\approx\)100%-33,33%\(\approx\)66,67%.
b. nnước=0,5.(0,05.4+0,1.6)=0,4 (mol).
BTKL: m\(O_2\)=17,6+0,4.18-(0,05.28+0,1.42)=19,2 (g) \(\Rightarrow\) n\(O_2\)=19,2/32=0,6 (mol).
Thể tích cần tìm là 0,6.22,4=13,44 (lít).
Đúng 1
Bình luận (0)
Đốt cháy 12 gam hỗn hợp gồm Zn, Al trong khí O2 dư. Sau khi các phản ứng xảy ra hoàn toàn thu được 16 gam hỗn hợp oxit. Thể tích khí O2 đã phản ứng là
A. 2,80 lít
B. 4,2 lít
C. 3,36 lít
D. 5,6 lít
Đáp án A
12(g) Kim loại + ?O2 ® 16(g) Oxit.
Bảo toàn khối lượng: mO2 = 4(g) ⇒ nO2 = 0,125 mol.
||⇒ VO2 = 0,125 × 22,4 = 2,8 lít
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 8,9 gam hỗn hợp X gồm Mg và Zn bằng khí O2 (vừa đủ), thu được 12,1 gam hỗn hợp oxit. Thể tích oxi (đktc) tham gia phản ứng là : A. 6,72 lít. B. 5,6 lít. C. 4,48 lít. D. 2,24 lít.
Đọc tiếp
Đốt cháy hoàn toàn 8,9 gam hỗn hợp X gồm Mg và Zn bằng khí O2 (vừa đủ), thu được 12,1 gam hỗn hợp oxit. Thể tích oxi (đktc) tham gia phản ứng là :
A. 6,72 lít.
B. 5,6 lít.
C. 4,48 lít.
D. 2,24 lít.
Đốt cháy 11,9 gam hỗn hợp gồm Zn, Al trong khí
Cl
2
dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 40,3 gam hỗn hợp muối. Thể tích khí
Cl
2
(đktc) đã tham gia phản ứng là A, 8,96 lít B. 6,72 lít C. 17,92 lít D. 11,20 lít
Đọc tiếp
Đốt cháy 11,9 gam hỗn hợp gồm Zn, Al trong khí Cl 2 dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 40,3 gam hỗn hợp muối. Thể tích khí Cl 2 (đktc) đã tham gia phản ứng là
A, 8,96 lít
B. 6,72 lít
C. 17,92 lít
D. 11,20 lít
Đốt cháy 36g FeS2 với 13,44 lít khí O2 (đktc). Sau phản ứng thu được 28g hỗn hợp rắn X và V lít hỗn hợp khí Y. Tính hiệu suất phản ứng và thành phần % thể tích các khí trong Y ( các khí được đo cùng điều kiện)
$n_{FeS_2} = \dfrac{36}{120} = 0,3(mol)$
$n_{O_2} = \dfrac{13,44}{22,4} = 0,6(mol)$
$4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2$
Vì \(\dfrac{n_{FeS_2}}{4} = 0,075 > \dfrac{n_{O_2}}{11} = 0,0545\) nên $FeS_2$ dư
Gọi hiệu suất là a
\(n_{O_2\ pư} = 0,6a(mol)\\ n_{FeS_2} = \dfrac{4}{11}n_{O_2\ pư} = \dfrac{12a}{55}(mol)\\ n_{Fe_2O_3} = \dfrac{2}{11}n_{O_2\ pư} = \dfrac{6a}{55}(mol)\)
Suy ra :
120.(0,3 - 12a/55 )+ 160.6a/55 = 28
Suy ra a = 0,9167 = 91,67%
Sau phản ứng , khí gồm :
O2 dư : 0,6 - 0,6a = 0,05(mol)
SO2 : 0,4(mol)
Suy ra :
%V O2 = 0,05/(0,05 + 0,4) .100% = 11,11%
%V SO2 = 100% - 11,11% = 88,89%
Đúng 3
Bình luận (1)
Đốt cháy hoàn toàn 0,1 mol hỗn hợp gồm: C2H6, C2H4O2, C3H6O2 và C4H6O4 thu được 5,6 lít khí CO2 (đktc) và 4,5 gam H2O. Tính thể tích khí O2 (đktc) đã tham gia phản ứng.
Cho 7,8 gam hỗn hợp hai kim loại là Mg và Al tác dụng với dung dịch
H
2
SO
4
loãng, dư. Khi phản ứng kết thúc, người ta thu được 8,96 lít khí (đktc). Tính thể tích dung dịch
H
2
SO
4
2M đã tham gia các phản ứng.
Đọc tiếp
Cho 7,8 gam hỗn hợp hai kim loại là Mg và Al tác dụng với dung dịch H 2 SO 4 loãng, dư. Khi phản ứng kết thúc, người ta thu được 8,96 lít khí (đktc). Tính thể tích dung dịch H 2 SO 4 2M đã tham gia các phản ứng.
Thể tích dung dịch H 2 SO 4 tham gia phản ứng :
Số mol H 2 SO 4 tham gia (1) và (2) là :
0,1 + 0,3 = 0,4 (mol)
Thể tích dung dịch H 2 SO 4 là :
V H 2 SO 4 = 0,4/2 = 0,2 l
Đúng 0
Bình luận (0)