viết phương trình hóa học biểu diễn sự oxi hóa của các đơn chất: hidro,photpho,kẽm,chì ,sắt ,đồng
\(4K+O_2\underrightarrow{t^0}2K_2O\)
\(C+O_2\underrightarrow{t^0}CO_2\)
\(4Al+3O_2\underrightarrow{t^0}2Al_2O_3\)
\(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\)
\(2Cu+O_2\underrightarrow{t^0}2CuO\)
\(2Zn+O_2\underrightarrow{t^0}2ZnO\)
\(C_3H_8+5O_2\underrightarrow{t^0}3CO_2+4H_2O\)
\(C_5H_{10}+\dfrac{15}{2}O_2\underrightarrow{t^0}5CO_2+5H_2O\)
\(C_2H_5OH+3O_2\underrightarrow{t^0}2CO_2+3H_2O\)
Viết các phương trình hóa học biểu diễn sự cháy trong oxi của các đơn chất: cacbon, photpho, hidro, nhôm biết rằng sản phẩm lần lượt là những hợp chất có công thức hóa học: CO2, P2O5, H2O, Al2O3. Hãy gọi tên các sản phẩm.
\(C+O_2\underrightarrow{t^0}CO_2\) ( Cacbon dioxit)
\(4P+5O_2\underrightarrow{t^0}2P_2O_5\)( Diphotpho pentaoxit)
\(H_2+\dfrac{1}{2}O_2\underrightarrow{t^0}H_2O\) ( Nước hay dihidro monooxit)
\(4Al+3O_2\underrightarrow{t^0}2Al_2O_3\) ( Nhôm oxit)
C + O2 --to--> CO2 (Khí cacbonic)
4P + 5O2 --tO--> 2P2O5 (đi photpho pentaoxit)
H + O2 --to--> H2O (Nước)
4Al + 3O2 --to--> 2Al2O3 (Nhôm oxit)
Viết phương trình hóa học biểu diễn sự chấy của oxi với các đơn chất : Photpho P, đồng Cu, sắt Fe. Biết rằng sản phẩm là những hợp chất lần lượt là : P205,CuO, Fe3O4. Gọi tên các sản phẩm .
GIÚP MÌNH GẤP
4P+5O2➞(to)2P2O5
2Cu+O2➞(to)2CuO
3Fe+2O2➞(to)Fe3O4
P2O5:điphotphopentaoxit
CuO:đồng(II)oxit
Fe3O4:oxit sắt từ
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\\ 2Cu+O_2\underrightarrow{t^o}2CuO\\ 3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(4P+5O_2\xrightarrow[]{t^o}2P_2O_5\) : điphotpho pentaoxit
\(2Cu+O_2\xrightarrow[]{t^o}2CuO\) : đồng oxit
\(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\) : Oxit sắt từ
Viết các phương trình hóa học biểu diễn sự cháy trong oxi của các đơn chất: cacbon, photpho, hiđro, nhôm biết rằng sản phẩm là những hợp chất lần lượt có công thức hóa học là CO2, P2O5, H2O, Al2O3. Hãy gọi tên các chất tạo thành.
C + O2 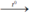 CO2. Cacbon đioxit.
CO2. Cacbon đioxit.
4P + 5O2 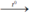 2P2O5. Điphotpho pentaoxit.
2P2O5. Điphotpho pentaoxit.
2H2 + O2 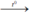 2H2O. Nước.
2H2O. Nước.
4Al + 3O2 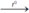 2Al2O3. Nhôm oxit.
2Al2O3. Nhôm oxit.
C1 viết phương trình hóa học biểu diễn sự chảy của sắt,photpho,lưu hình ,nhôm trong khí oxi
C2 dẫn 2,24 lít khí hidro(đktc) vào một ống chứa 12g CuO đã nung nóng đến một nhiệt độ thích hợp.Khối lượng nước tạo thành là:
C3 Cho chất Fe2O3
a) hợp chất Fe2O3 gồm mấy nguyên tố ? đó là nguyên tố nào?
b) Tính phần trăm về khối lượng của oxi
C1:
3Fe + 2O2 -> (t°) Fe3O4
4P + 5O2 -> (t°) 2P2O5
S + O2 -> (t°) SO2
C2:
nH2 = 2,24/22,4 = 0,1 (mol)
nCuO = 12/80 = = 0,15 (mol)
PTHH: CuO + H2 -> (t°) Cu + H2O
LTL 0,15 > 0,1 => CuO dư
nH2O = 0,1 (mol)
mH2O = 0,1 . 18 = 1,8 (g)
C3:
Fe2O3 gồm 2 nguyên tố: Fe và O
%Fe = 112/160 = 70%
%O = 100% - 70% = 30%
Câu 1: Photpho: 4P + 5O2 (to)-> 2P2O5
Lưu huỳnh: S + O2 (to)-> SO2
Nhôm: 4Al + 3O2 (to)-> Al2O3
Câu 2:
PTHH: \(CuO+H_2=>Cu+H_2O\)
\(nH_2=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(nCuO=\dfrac{12}{80}=0,15\left(mol\right)\)
\(=>CuOdư\)
\(nH_2O=nH_2=0,1\left(mol\right)\)
\(mH_2=0,1\text{×}18=1,8\left(gam\right)\)
Bài 1: Viết các phương trình hóa học biểu diễn sự cháy trong oxi của các đơn chất: cacbon, photpho, hiđro, nhôm biết rằng sản phẩm là những hợp chất lần lượt có công thức hóa học là CO2, P2O5, H2O, Al2O3. Hãy gọi tên các chất tạo thành.
Bài 8: Để chuẩn bị cho buổi thí nghiệm thực hành của lớp cần thu 20 lọ khí oxi, mỗi lọ có dung tích 100ml.
a) Tính khối lượng kali pemanganat phải dùng, giả sử khí oxi thu được ở điều kiện tiêu chuẩn và hao hụt 10%?
b) Nếu dùng kali clorat có thêm một lượng nhỏ MnO2 thì lượng kali clorat cần dùng là bao nhiêu? Viết phương trình phản ứng và chỉ rõ điều kiện phản ứng.
Bài 8:
\(V_{O_2}=20.100=2000\left(ml\right)=2\left(l\right)\\ a,PTHH:2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\\ n_{O_2}=\dfrac{2}{22,4}=\dfrac{5}{56}\left(mol\right)\\ n_{O_2\left(p.ứ\right)}=\dfrac{5}{56}.90\%=\dfrac{9}{112}\left(mol\right)\\ n_{KMnO_4\left(dùng\right)}=\dfrac{9}{112}.2=\dfrac{9}{56}\left(mol\right)\\ \Rightarrow m_{KMnO_4}=\dfrac{9}{56}.158=\dfrac{711}{28}\left(g\right)\\ b,2KClO_3\rightarrow\left(t^o,xt\right)2KCl+3O_2\\ n_{KClO_3}=\dfrac{2}{56}.\dfrac{2}{3}=\dfrac{1}{42}\left(mol\right)\\ m_{KClO_3}=122,5.\dfrac{1}{42}=\dfrac{35}{12}\left(g\right)\)
Bài 1:
\(C+O_2\rightarrow\left(t^o\right)CO_2\)
Tên sản phẩm: Cacbon dioxit/ Khí cacbonic
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
Tên sản phẩm: Điphotpho pentaoxit
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
Tên sản phẩm: Nước
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
Tên sản phẩm: Nhôm oxit
IV.12 Viết phương trình hoá học biểu diễn sự oxi hoá của các đơn chất : hiđro,
photpho, kem, chì, biết rằng sản phẩm là những hợp chất lần lượt có
công thức hoá học là H,O, P,03, ZnO, PbO.
\(H_2+O_2\rightarrow H_2O\)
\(P+O_2\underrightarrow{t^o}P_2O_5\)
\(Zn+O_2\underrightarrow{t^o}ZnO\)
\(Pb+O_2\underrightarrow{t^o}PbO\)
Viết phương trình hóa học biểu diễn sự cháy của các chất sau: sắt, đồng, chì, thủy ngân, cacbon, nhôm, photpho, kali, lưu huỳnh, khí hidro, magie, canxi, kẽm, natri
- 3Fe + 2O2 --> Fe3O4
- 2Cu + O2 --> 2CuO
- 2Pb + O2 --> 2PbO
- 2Hg + O2 --> 2HgO
- C + O2 --> CO2
- 4Al + 3O2 --> 2Al2O3
- 4P + 5O2 --> 2P2O5
- 4K + O2 --> 2K2O
- S + O2 --> SO2
- 2H2 + O2 --> 2H2O
- 2Mg + O2 --> 2MgO
- 2Ca + O2 --> 2CaO
- 2Zn + O2 --> 2ZnO
- Na + O2 --> Na2O
Bài 3 : Viết các phương trình hoá học biểu diễn sự oxi hoá cac bon, nhôm, sắt, photpho, metan CH4, khí đất đèn C2H4, cồn C2H6O.
DẠNG 2: Phân loại gọi tên oxit
Cho các oxit có công thức hóa học sau : SO3 ; N2O5 ; CO2 ; Fe2O3 ; CuO ; CaO ; SO2 MgO; H2O; Al2O3; ZnO
a- Gọi tên các oxit
b-Những chất nào thuộc oxit bazơ ? những chất nào thuộc loại oxit axit ?Dạng 3: Giải bài tập theo PTHH
Bài 1:Đốt cháy 24 (g) bột than (C) trong bình khí oxi.
a. Viết phương trình hóa học xảy ra
b.Tính thể tích khí oxi ở điều kiện tiêu chuẩn cần dùng để đốt cháy hết lượng Cacbon trên.
Bài 2 Đốt cháy hoàn toàn 5,4 gam Al trong không khí, thu được chất rắn là Al2O3
a. Viết phương trình phản ứng xảy ra và tính khối lượng Al2O3 tạo thành
b. Tính thể tích không khí cần dùng (biết rằng Oxi chiếm 20% không khí) (các thể tích đo ở đktc)
Bài 3: Đốt cháy hoàn toàn 1,86g sắt ở nhiệt độ cao .
a. Tính khối lượng oxit sắt thu được sau phản ứng.
b. Tính thề tích khí oxi cần dùng (đktc).
c. Tính thể tích không khí cần thiết để có đủ lượng oxi trên
Bài 4: Nung thuỷ ngân oxit thu được thuỷ ngân và oxi.
a. Viết PTHH của phản ứng
b. Phản ứng trên thuộc loại phản ứng nào
c. Nung 21,7 gam thuỷ ngân oxit. Tính thể tích oxi (đktc) và khối lượng thuỷ ngân thu được
Bài 5: Cho 11,2 g sắt tác dụng vừa đủ với HCl. Toàn bộ lượng Hiđro sinh ra cho tác dụng vừa đủ với m (g) CuO.
a-Tìm m
b-Tìm khối lượng FeCl2
Bài 6. Cho 13 gam Zn tác dụng với dung dịch có chứa 18,25 gam HCl.
a) Tính xem chất nào còn dư sau phản ứng và khối lượng dư là bao nhiêu ?
b) Tính khối lượng ZnCl2 tạo thành sau phản ứng.
c) Tính thể tích khí H2 thu được ở đktc.
Bài 1:Đốt cháy 24 (g) bột than (C) trong bình khí oxi.
a. Viết phương trình hóa học xảy ra
b.Tính thể tích khí oxi ở điều kiện tiêu chuẩn cần dùng để đốt cháy hết lượng Cacbon trên.
---
a) C + O2 -to-> CO2
nC=2(mol)
b)nO2=nC=2(mol)
=>V(O2,đktc)=2.22,4=44,8(l)
Bài 3:
C + O2 -to-> CO2
4Al +3 O2 -to-> 2 Al2O3
4P + 5 O2 -to-> 2 P2O5
3 Fe + 2 O2 -to-> Fe3O4
CH4 + 2 O2 -to-> CO2 + 2 H2O
2 C2H2 + 5 O2 -to-> 4 CO2 + 2 H2O
C2H4 + 3 O2 -to-> 2 CO2 + 2 H2O
C2H6O + 3 O2 -to-> 2 CO2 + 3 H2O
Dạng 2:
a) SO3: Lưu huỳnh trioxit
N2O5: Đinitơ pentaoxit
CO2: cacbon đioxit
Fe2O3: Sắt (III) oxit
CuO: Đồng (II) oxit
CaO: Canxi oxit
MgO: Magie oxit
SO2: Lưu huỳnh đioxit
ZnO: Kẽm oxit
Al2O3: Nhôm oxit
H2O: Nước
b) Oxit bazo: Fe2O3, MgO, Al2O3 (lớp 8 thì tạm phân loại vậy), ZnO, CaO, CuO.
Oxit axit: N2O5, SO3, SO2, CO2.