đốt chấy hoàn toàn m (g) hỗn hớp A cần dùng 11,2 lít khí oxi, thu được 8,8g CO2 và 5,4g H2O. Ở đktc 2,241l khí A có khói lượng 5,8g. Xác định CTP và CTCT cảu A

Những câu hỏi liên quan
đốt chấy hoàn toàn m (g) hỗn hớp A cần dùng 11,2 lít khí oxi, thu được 8,8g CO2 và 5,4g H2O. Ở đktc 2,241l khí A có khối lượng 5,8g. Xác định CTPT và CTCT của A
Đốt cháy hoàn toàn m gam hợp chất hữu cơ A cần dùng 11,2 gam khí oxi, thu được 8,8 gam
C
O
2
và 5,4 gam
H
2
O
. Ở đktc 2,24 lít khí A có khối lượng 3 gam. Xác định CTPT của A? A.
C
2
H
6
B.
C
2
H
4
C.
C...
Đọc tiếp
Đốt cháy hoàn toàn m gam hợp chất hữu cơ A cần dùng 11,2 gam khí oxi, thu được 8,8 gam C O 2 và 5,4 gam H 2 O . Ở đktc 2,24 lít khí A có khối lượng 3 gam. Xác định CTPT của A?
A. C 2 H 6
B. C 2 H 4
C. C 3 H 8
D. C 3 H 6
n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
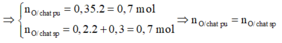
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
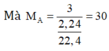
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.
Đúng 0
Bình luận (0)
đốt cháy hoàn toàn một hỗn hợp 20 hidrocacbon khác nhau thu được 8,8g co2 và 1,8g h2o thì số lít (đktc) khí oxi cần dùng là
\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\)
Bảo toàn O: \(n_{O_2}=\dfrac{0,2.2+0,1.1}{2}=0,25\left(mol\right)\)
=> \(V_{O_2}=0,25.22,4=5,6\left(l\right)\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 2,24l hidrocacbon A thể khí thu được 6,72l khí CO2 và 5,4g hơi nước.
1) Xác định công thức phân tử của hidrocacbon, biết rằng thể tích khí đo ở đktc.
2) Tính khối lượng khí Oxi cần dùng cho phản ứng trên.
1) \(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
=> nC = 0,3 (mol)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
=> nH = 0,6 (mol)
\(n_A=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Số nguyên tử C = \(\dfrac{0,3}{0,1}=3\) (nguyên tử)
Số nguyên tử H = \(\dfrac{0,6}{0,1}=6\) (nguyên tử)
CTHH: C3H6
2)
PTHH: 2C3H6 + 9O2 --to--> 6CO2 + 6H2O
0,1--->0,45
=> mO2 = 0,45.32 = 14,4 (g)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 7g hợp chất hữu cơ A thu được 11,2 l khí CO2 đo ở đktc và 9 g nước.
a, Xác định CTHH của A biết tỉ khối dA/CH4=1,75
b, Tính thể tích không khí cần dùng để đốt cháy hoàn toàn a biết oxi chiếm 20% không khí
Đốt cháy hoàn toàn m gam hợp chất hữu cơ À cần dùng 11,2 gam khí oxi , thu được 8,8gam Co2 và 5,4 gam H2O. Xác định CT PT của A biết 25
\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O
⇒ mA = 3 (g)
Ta có: mC + mH = 0,2.12 + 0,6.1 = 3 (g) = mA
→ A gồm C và H.
Gọi CTPT của A là CxHy.
⇒ x:y = 0,2:0,6 = 1:3
→ A có CTPT dạng (CH3)n ( n nguyên dương)
⇒ MA = 15n (g/mol)
Có: 25 < MA < 35
Với n = 1 ⇒ MA = 15 (loại)
n = 2 ⇒ MA = 30 (tm)
n = 3 ⇒ MA = 45 (loại)
Vậy: CTPT của A là C2H6.
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 5,8g chất hữu cơ A thu được 8,96 lít CO2 ở (đktc) và 9,0g H2O
a, Xác định cong thức phân tử của A. Biết MA = 58 g/mol
b, Viết công thức cấu tạo có thể có của A. Hãy cho mỗi CTCT đó thuộc loại mạch C nào?
nCO2 = 8.96/22.4 = 0.4 (mol)
nH2O = 9/18 = 0.5 (mol)
mO = mA - mC - mH = 5.8 - 0.4*12 - 0.5*2 = 0
nA = 5.8/58 = 0.1 (mol)
Số nguyên tử C : 0.4/0.1 = 4
Số nguyên tử H : 0.5*2/0.1 = 10
CT : C4H10
CTCT:
CH3 - CH2 - CH2 - CH3
CH3 - CH(CH3) - CH3
Đúng 1
Bình luận (0)
Câu 4: Đốt cháy một hỗn hợp gồm CH4 và C2H2 có thể tích là 33,6 lít (đktc) thu được 56 lít khí CO2 (đktc).a. Xác định thành phần % về thể tích các khí trong hỗn hợp?b. Tính khối lượng của oxi cần để đốt cháy hoàn toàn hỗn hợp khí trên?
Đọc tiếp
Câu 4: Đốt cháy một hỗn hợp gồm CH4 và C2H2 có thể tích là 33,6 lít (đktc) thu được 56 lít khí CO2 (đktc).
a. Xác định thành phần % về thể tích các khí trong hỗn hợp?
b. Tính khối lượng của oxi cần để đốt cháy hoàn toàn hỗn hợp khí trên?
a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\left(1\right)\)
Theo PT: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=\dfrac{56}{22,4}=2,5\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,5\left(mol\right)\\n_{C_2H_2}=1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,5.22,4}{33,6}.100\%\approx33,33\%\\\%V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=3,5\left(mol\right)\Rightarrow m_{O_2}=3,5.32=112\left(g\right)\)
Đúng 3
Bình luận (1)
Đốt cháy hoàn toàn hỗn hợp A gồm CH4, C2H4, C2H2 thu được 17,9g lít khí CO2 (đktc) và 18g H2O.
a) Viết các PTHH. b) Tính thể tích khí O2 (đktc) cần dùng và khối lượng hỗn hợp A.a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
b, Sửa đề: 17,9 (l) → 17,92 (l)
Ta có: \(n_{CO_2}=\dfrac{17,92}{22,4}=0,8\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{18}{18}=1\left(mol\right)\Rightarrow n_H=1.2=2\left(mol\right)\)
⇒ mA = mC + mH = 0,8.12 + 2.1 = 11,6 (g)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O
⇒ mO2 = 0,8.44 + 18 - 11,6 = 41,6 (g)
\(\Rightarrow n_{O_2}=\dfrac{41,6}{32}=1,3\left(mol\right)\Rightarrow V_{O_2}=1,3.22,4=29,12\left(l\right)\)
Đúng 2
Bình luận (0)















