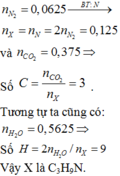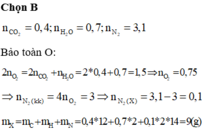Tìm công thức phân tử của 1 hidrocacbon mà sau khi đốt cháy thu 2,703 gam CO2 và 1,108 gam H2O ?

Những câu hỏi liên quan
Tìm công thức phân tử của 1 hiđrocacbon mà sau khi đốt cháy thu được 2,703 gam
C
O
2
và 1,108 gam
H
2
O
? A.
C
2
H
4
B.
C
2
H
6
C.
C
5
H
12
D. ...
Đọc tiếp
Tìm công thức phân tử của 1 hiđrocacbon mà sau khi đốt cháy thu được 2,703 gam C O 2 và 1,108 gam H 2 O ?
A. C 2 H 4
B. C 2 H 6
C. C 5 H 12
D. C 4 H 10
Đặt công thức tổng quát của hiđrocacbon là C x H y .
Ta có:
x : y = n C : n H = m C O 2 44 : m H 2 O 9 = 2,703 44 : 1,108 9 = 0,061 : 0,123 = 1 : 2
⇒ Chọn A.
Đúng 0
Bình luận (0)
Tìm công thức phân tử của một hiđrocacbon, mà sau khi đốt cháy thu được 2,703 gam CO2 và 1,108 gam H2O.
Ta có
\(n_{CO2}=\frac{2,703}{44}\approx0,06\left(mol\right)\)
\(\Rightarrow n_C=n_{CO2}=0,06\left(mol\right)\)
\(n_{H2O}=\frac{1,108}{18}\approx0,06\)
\(\Rightarrow n_H=2n_{H2O}=0,12\left(mol\right)\)
=>\(n_C:n_H=0,06:0,12=1:2\)
CTĐG: CH2
Gọi CTPT: (CH2)n
Do \(4n< 2n+1\)
=> n =2
=>CTPT:C2H4
Đốt cháy hoàn toàn 13,4 gam hợp chất hữu cơ X bằng không khí vừa đủ (chứa 80% N2 và 20% O2 về thể tích), thu được 22 gam CO2, 12,6 gam H2O và 69,44 lít N2 (đktc). Xác định công thức phân tử của X biết X có công thức phân tử trùng với công thức đơn giản nhất A. C5H14N2 B. C5H14O2N C. C5H14O2N2 D. C5H14ON2.
Đọc tiếp
Đốt cháy hoàn toàn 13,4 gam hợp chất hữu cơ X bằng không khí vừa đủ (chứa 80% N2 và 20% O2 về thể tích), thu được 22 gam CO2, 12,6 gam H2O và 69,44 lít N2 (đktc). Xác định công thức phân tử của X biết X có công thức phân tử trùng với công thức đơn giản nhất
A. C5H14N2
B. C5H14O2N
C. C5H14O2N2
D. C5H14ON2.
Khi đốt cháy hoàn toàn một amin đơn chức X, thu được 8,4 lít khí CO2; 1,4 lít khí N2 (các thể tích khí đo ở đktc) và 10,125 gam H2O. Công thức phân tử của X là A. C3H7N B. C2H7N C. C3H9N D. C4H9N
Đọc tiếp
Khi đốt cháy hoàn toàn một amin đơn chức X, thu được 8,4 lít khí CO2; 1,4 lít khí N2 (các thể tích khí đo ở đktc) và 10,125 gam H2O. Công thức phân tử của X là
A. C3H7N
B. C2H7N
C. C3H9N
D. C4H9N
Đốt cháy hỗn hợp hai hidrocacbon đồng đẳng kế tiếp nhau ta thu được 11,7 gam H2O và 17,6 gam CO2. Xác định công thức phân tử của hai hidrocacbon A. CH4 và C2H6 B. C3H8, C2H6 C. C3H8 và C4H10 D. Đáp án khác
Đọc tiếp
Đốt cháy hỗn hợp hai hidrocacbon đồng đẳng kế tiếp nhau ta thu được 11,7 gam H2O và 17,6 gam CO2. Xác định công thức phân tử của hai hidrocacbon
A. CH4 và C2H6
B. C3H8, C2H6
C. C3H8 và C4H10
D. Đáp án khác
nCO2 = 0,4 mol
nH2O = 0,65 mol
nH2O > nCO2 => ankan
CTB = 0,4/0,25 = 1,6 => CH4 và C2H6
Đúng 0
Bình luận (0)
Trộn a gam hỗn hợp X gồm 2 hidrocacbon C6H14 và C6H6 theo tỉ lệ mol (1:1) với b gam một hidrocacbon Y rồi đốt cháy hoàn toàn thì thu được
55
a
16
,
4
gam CO2 và
18
,
9
a
16
,
4...
Đọc tiếp
Trộn a gam hỗn hợp X gồm 2 hidrocacbon C6H14 và C6H6 theo tỉ lệ mol (1:1) với b gam một hidrocacbon Y rồi đốt cháy hoàn toàn thì thu được 55 a 16 , 4 gam CO2 và 18 , 9 a 16 , 4 gam H2O. Công thức phân tử của Y có dạng:
A. CnHn.
B. CmH2m-2.
C. CnH2n.
D. CnH2n+2.
Đáp án D
nCO2= 25/328mol
nH2O=21/328mol
=> nCO2 > nH2O
Dễ thấy đốt X thu được nCO2 < nH2O
=> Đốt Y phải thu được nCO2 > nH2O
=> X là ankan
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 35,2 gam este no, đơn chức thu được lượng CO2 lớn hơn H2O là 41,6 gam. CTPT của A là A. C4H8O2 B. C3H6O2 C. C4H6O2 D. C2H4O2
Đọc tiếp
Đốt cháy hoàn toàn 35,2 gam este no, đơn chức thu được lượng CO2 lớn hơn H2O là 41,6 gam. CTPT của A là A. C4H8O2 B. C3H6O2 C. C4H6O2 D. C2H4O2
Vì: este no, đơn chức ⇒ nCO2 = nH2O = x (mol)
Có: mCO2 - mH2O = 41,6
⇒ 44x - 18x = 41,6 ⇔ x = 1,6 (mol)
Gọi CTPT của este là CnH2nO2
\(\Rightarrow n_{C_nH_{2n}O_2}=\dfrac{1,6}{n}\left(mol\right)\)
\(\Rightarrow M_{C_nH_{2n}O_2}=\dfrac{35,2}{\dfrac{1,6}{n}}=22n\)
⇒ 14n + 32 = 22n ⇔ n = 4
Vậy: CTPT của este là C4H8O2.
→ Đáp án: A
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Đốt cháy amin X với không khí (
N
2
và
O
2
với tỉ lệ mol 4:1) vừa đủ, sau phản ứng thu được 17,6 gam
C
O
2
, 12,6 gam
H
2
O
và 69,44 lít
N
2
(đktc). Khối lượng của amin là: A. 9,2 gam B. 9 gam C. 11 gam D. 9,5 gam
Đọc tiếp
Đốt cháy amin X với không khí ( N 2 và O 2 với tỉ lệ mol 4:1) vừa đủ, sau phản ứng thu được 17,6 gam C O 2 , 12,6 gam H 2 O và 69,44 lít N 2 (đktc). Khối lượng của amin là:
A. 9,2 gam
B. 9 gam
C. 11 gam
D. 9,5 gam
Đốt cháy hoàn toàn 2,76 gam hỗn hợp X gồm CxHyCOOH, CxHyCOOCH3, CH3OH thu được 2,688 lít CO2 (đktc) và 1,8 gam H2O. Mặt khác, cho 2,76 gam X phản ứng vừa đủ với 30 ml dung dịch NaOH 1M, thu được 0,96 gam CH3OH. Công thức của CxHyCOOH là A. C2H5COOH. B. CH3COOH. C. C2H3COOH. D. C3H5COOH.
Đọc tiếp
Đốt cháy hoàn toàn 2,76 gam hỗn hợp X gồm CxHyCOOH, CxHyCOOCH3, CH3OH thu được 2,688 lít CO2 (đktc) và 1,8 gam H2O. Mặt khác, cho 2,76 gam X phản ứng vừa đủ với 30 ml dung dịch NaOH 1M, thu được 0,96 gam CH3OH. Công thức của CxHyCOOH là
A. C2H5COOH.
B. CH3COOH.
C. C2H3COOH.
D. C3H5COOH.
Đáp án C
► Đốt X: 2,76(g) X + ?O2 → t ° 0,12 mol CO2 + 0,1 mol H2O.
Bảo toàn khối lượng: mO2 = 4,32(g) ⇒ nO2 = 0,135 mol.
Bảo toàn nguyên tố Oxi: nO/X = 2 × 0,12 + 0,1 – 0,135 × 2 = 0,07 mol
● nCOO = nNaOH = 0,03 mol ⇒ nCH3OH/X = 0,07 – 0,03 × 2 = 0,01 mol.
nCH3OH = 0,03 mol ⇒ neste = 0,03 – 0,01 = 0,02 mol
⇒ naxit = 0,03 – 0,02 = 0,01 mol. Bảo toàn nguyên tố Cacbon và Hidro:
► x = 2; y = 3 ⇒ C2H3COOH
Đúng 0
Bình luận (0)