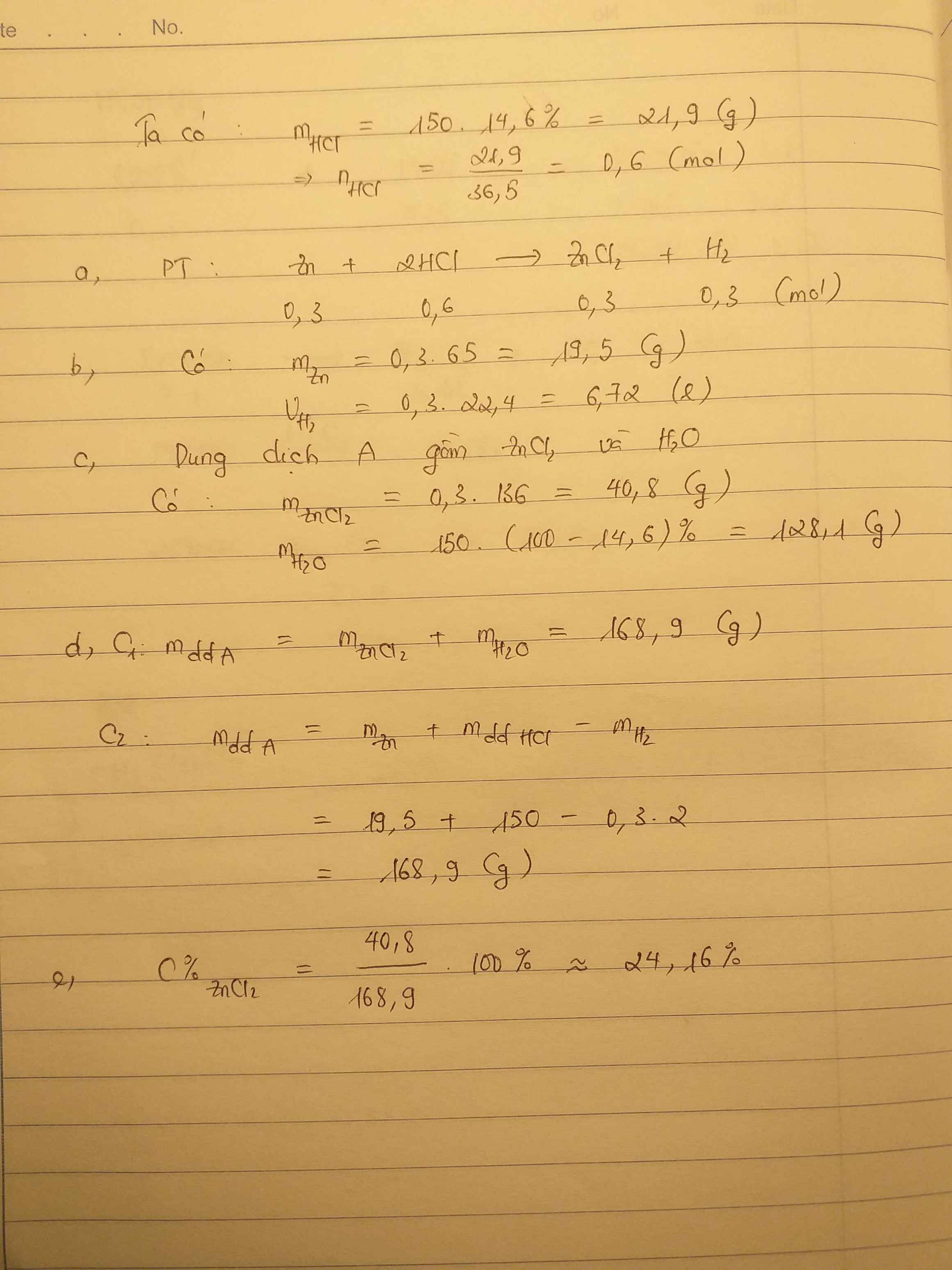Cho m gam kim loại m vào bình chứa 100ml dụng dịch HCl dư sau phản ứng thứ đc 1,792 lít khí H2 ở được đồng thời khối lượng bình tăng 1,76gam. Tính m và xác định kim loại

Những câu hỏi liên quan
Cho V lít khí CO đktc đi qua ống sứ chứa 2,32g oxit sắt kim loại nung nóng đến phản ứng hoàn toàn thu được m gam kim loại và hỗn hợp khí có tỉ khối so với H2 bằng 18.Dẫn toàn bộ lượng khí này vào bình chứa 2000ml dung dịch Ca(OH)2 0,015M.Kết thúc phản ứng thu được 2g kết tủa và dung dịch A.Lọc tách kết tủa rồi cho dung dịch Ba(OH)2 dư vào dung dịch A ta thu được p gam kết tủa.Cho toàn bộ lượng kim loại thi được ở trên vào bình chứa dung dịch HCl dư,phản ứng kết thúc ta thu được 0,672 lít khí H2...
Đọc tiếp
Cho V lít khí CO đktc đi qua ống sứ chứa 2,32g oxit sắt kim loại nung nóng đến phản ứng hoàn toàn thu được m gam kim loại và hỗn hợp khí có tỉ khối so với H2 bằng 18.Dẫn toàn bộ lượng khí này vào bình chứa 2000ml dung dịch Ca(OH)2 0,015M.Kết thúc phản ứng thu được 2g kết tủa và dung dịch A.Lọc tách kết tủa rồi cho dung dịch Ba(OH)2 dư vào dung dịch A ta thu được p gam kết tủa.Cho toàn bộ lượng kim loại thi được ở trên vào bình chứa dung dịch HCl dư,phản ứng kết thúc ta thu được 0,672 lít khí H2 đktc.Viết các PTHH xảy ra.Tính C,m,p và xác định CT của oxit kim loại
Cho m gam kim loại m vào bình chứa 100 ml dd HCl dư sau phản ứng thu đc 1,792 lít H2 ở đktc. Đồng thời khối lượng bình tăng 1,76 gam. Tính m và xđinh kim loại
đề có đúng không vậy bạn
cho 4,8 gam kim loại m tác dụng hết với dung dịch axit HCL Sau phản ứng thu được 4,48 lít khí H2 (đktc). xác định kim loại M và tính khối lượng muối thu được sau phản ứng
Giả sử KL có hóa trị n.
PT: \(2M+2nHCl\rightarrow2MCl_n+nH_2\)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_M=\dfrac{2}{n}nH_2=\dfrac{0,4}{n}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{4,8}{\dfrac{0,4}{n}}=12n\left(g/mol\right)\)
Với n = 2 thì MM = 24 (g/mol) là tm
Vậy: M là Mg.
Ta có: \(n_{MgCl_2}=n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(\Rightarrow m_{MgCl_2}=0,2.95=19\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 20,16 lít khí CO phản ứng với một lượng oxit MxOy nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được 25,2 gam kim loại M và hỗn hợp khí X. Cho toàn bộ lượng hỗn hợp khí X qua bình chứa dung dịch Ca(OH)2 dư tạo ra m gam kết tủa và có 6,72 lít khí thoát ra. Hòa tan hoàn toàn lượng kim loại trên trong dung dịch HCl dư, thấy thoát ra 10,08 lít khí H2. Xác định công thức oxit và tính m. Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Đọc tiếp
Cho 20,16 lít khí CO phản ứng với một lượng oxit MxOy nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được 25,2 gam kim loại M và hỗn hợp khí X. Cho toàn bộ lượng hỗn hợp khí X qua bình chứa dung dịch Ca(OH)2 dư tạo ra m gam kết tủa và có 6,72 lít khí thoát ra. Hòa tan hoàn toàn lượng kim loại trên trong dung dịch HCl dư, thấy thoát ra 10,08 lít khí H2. Xác định công thức oxit và tính m. Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.

Đúng 0
Bình luận (0)
Cho 4,8 gam kim loại M vào 50 gam dung dịch HCl nồng độ 36,5 % , phản ứng xong thu được 4,48 lít khí H2 , ( ở đktc ) và dung dịch X. Xác định kim loại M và tính nồng độ phần trăm các chất trong X.
PTHH: \(2M+2xHCl\rightarrow2MCl_x+xH_2\uparrow\) (x là hóa trị của M)
Tính theo sản phẩm
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow n_M=\dfrac{0,4}{x}\left(mol\right)\) \(\Rightarrow M=\dfrac{4,8}{\dfrac{0,4}{x}}=12x\)
Ta thấy với \(x=2\) thì \(M=24\) (Magie)
Mặt khác: \(n_{HCl}=\dfrac{50\cdot36,5\%}{36,5}=0,5\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{MgCl_2}=n_{H_2}=0,2\left(mol\right)\\n_{HCl\left(dư\right)}=0,1\left(mol\right)\end{matrix}\right.\)
Ta lại có: \(m_{dd\left(sau.p/ứ\right)}=m_{Mg}+m_{ddHCl}-m_{H_2}=4,8+50-0,2\cdot2=54,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{0,2\cdot95}{54,4}\cdot100\%\approx34,93\%\\C\%_{HCl\left(dư\right)}=\dfrac{0,1\cdot36,5}{54,4}\cdot100\%\approx6,71\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Bài 1:Cho sơ đồ phản ứng sau: Mg + HCl -MgCl2 + H2Nếu cho 2,4g Mg tác dụng với 3,65g HCl. Chất nào còn dư sau phản ứng? Tính khối lượng còn dư? Tính khối lượng MgCl2 tạo thành và thể tích khí H2 thu được (đktc)Bài 2:Cho sơ đồ phản ứng sau: Al + H2SO4 - Al2(SO4)3 + H2Nếu có 5,4g nhôm tác dụng với 14,7g H2SO4. Chất nào còn dư sau phản ứng? Tính khối lượng còn dư? Tính khối lượng Al2(SO4)3 tạo thành và thể tích khí H2 thu được (đktc)Bài 3: Hòa tan hoàn toàn 3,78g với kim loại M (hóa trị III) vào d...
Đọc tiếp
Bài 1:
Cho sơ đồ phản ứng sau: Mg + HCl ->MgCl2 + H2
Nếu cho 2,4g Mg tác dụng với 3,65g HCl. Chất nào còn dư sau phản ứng? Tính khối lượng còn dư? Tính khối lượng MgCl2 tạo thành và thể tích khí H2 thu được (đktc)
Bài 2:
Cho sơ đồ phản ứng sau: Al + H2SO4 -> Al2(SO4)3 + H2
Nếu có 5,4g nhôm tác dụng với 14,7g H2SO4. Chất nào còn dư sau phản ứng? Tính khối lượng còn dư? Tính khối lượng Al2(SO4)3 tạo thành và thể tích khí H2 thu được (đktc)
Bài 3:
Hòa tan hoàn toàn 3,78g với kim loại M (hóa trị III) vào dung dịch HCl thu được 4,704l khí H2 (đktc). Xác định kim loại M?
Bài 4:
Cho sơ đồ phản ứng sau: KMnO4 -> ..........+...........+O2
Tính thể tích Oxi (đktc) thu được khi nhiệt phân hủy hoàn toàn 0,4 mol KMnO4
Đốt cháy 6,2g photpho trong bình chứa lượng Oxi ở trên. Tính khối lượng điphotpho pentaoxit?
bạn từng câu lên sẽ dễ nhìn hơn
cho 3,79 g hỗn hợp 2 kim loại Zn và Al tác dụng với H2 SO4 loãng dư thu được 1,792 lít khí H2 ở điều kiện chuẩn a xác định thành phần phần trăm về khối lượng của kim loại tính khối lượng axit đã phản ứng giúp mình vs
\(n_{H_2\left(dktc\right)}=\dfrac{V}{22,4}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
đặt \(\left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
\(PTHH:Zn+H_2SO_4->ZnSO_4+H_2\)
tỉ lệ 1 : 1 : 1 : 1
n(mol) a---->a------------>a---------->a (1)
\(PTHH:2Al+3H_2SO_4->Al_2\left(SO_4\right)_3+3H_2\)
tỉ lệ 2 : 3 ; 1 : 3
n(mol) b-------->3/2b----->1/2b------------>3/2b (2)
Từ (1) và (2) ta có
\(\left\{{}\begin{matrix}65a+27b=3,79\\a+\dfrac{3}{2}b=0,08\end{matrix}\right.=>\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,02\left(mol\right)\end{matrix}\right.\)
\(=>\left\{{}\begin{matrix}m_{Zn}=n\cdot M=0,05\cdot65=3,25\left(g\right)\\m_{Al}=n\cdot M=0,02\cdot27=0,54\left(g\right)\end{matrix}\right.\)
\(=>\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{3,25\cdot100\%}{3,79}\approx85,75\%\\\%m_{Al}=100\%-85,75\approx14,25\%\end{matrix}\right.\)
với (1) thì
\(n_{H_2SO_4\left(1\right)}=a=0,05\left(mol\right)\)
với (2) thì
\(n_{H_2SO_4\left(2\right)}=\dfrac{3}{2}b=\dfrac{3}{2}\cdot0,02=0,03\left(mol\right)\)
\(=>m_{H_2SO_4}=\left(0,05+0,03\right)\cdot98=7,84\left(g\right)\)
Đúng 1
Bình luận (0)
1a, Cho 4,8g một kim loại hóa trị 2 phản ứng hết với dung dịch HCL dư, thu được 2,688lits H2(đktc). Xác định tên kim loại và khối lượng muối thu được sau phản ứng
1b, Cho 2,4g kim loại Mg tác dụng hết với đ HCL dư được V lít H2 ở đktc. Tính giá tri của V và khối lượng muối thu được sau phản ứng
1a)
nH2 = 2.688/22.4 = 0.12 (mol)
M + 2HCl => MCl2 + H2
0.12..............0.12......0.12
MM = 4.8/0.12 = 40
=> M là : Ca
mCaCl2 = 0.12 * 111 = 13.32 (g)
Đúng 1
Bình luận (0)
1b)
nMg = 2.4/24 = 0.1 (mol)
Mg + 2HCl => MgCl2 + H2
0.1....................0.1.........0.1
VH2 = 0.1*22.4 = 2.24 (l)
mMgCl2 = 0.1*95 = 9.5 (g)
Đúng 1
Bình luận (0)
1b)
nMg=0,2(mol)
PTHH: Mg + 2 HCl -> MgCl2 + H2
nH2=nMgCl2=nMg=0,2(mol)
=> nHCl=2.0,2=0,4(mol)
=> V=V(H2,đktc)=0,2.22,4=4,48(l)
mMgCl2=95. 0,2=19(g)
Đúng 0
Bình luận (2)
Cho m gam kim loại Zn phản ứng vừa đủ với 150 gam dung dịch HCl 14,6%. Sau phản ứng, thu được dung dịch A và V lít khí H2 ( ở đktc)
a) Viết PTHH
b) Tính giá trị của V và m?
c) Dung dịch A chứa những chất gì? tính khối lượng từng chất?
d) Tính khối lượng dung dịch A theo 2 cách?
e) Tính nồng độ % của dung dịch A?