Đốt cháy hoàn toàn 18 (g) hợp chất hữu cơ A cần vừa đủ 16,8 lít O2 ( đktc ) . Hỗn hợp sản phẩm cháy gồm CO2 và H2O theo tỉ lệ thể tích VCO2 : VH2O = 3 : 2 . Xác định CTPT của A biết dA/H2 = 36

Những câu hỏi liên quan
Để đốt cháy hoàn toàn 4,45 g hợp chất A cần dùng vừa hết 4,20 lít
O
2
. Sản phẩm cháy gồm có 3,15 g
H
2
O
và 3,92 lít hỗn hợp khí gồm
C
O
2
và
N
2
. Các thể tích ở đktc. Xác định công thức đơn giản nhất của chất A.
Đọc tiếp
Để đốt cháy hoàn toàn 4,45 g hợp chất A cần dùng vừa hết 4,20 lít O 2 . Sản phẩm cháy gồm có 3,15 g H 2 O và 3,92 lít hỗn hợp khí gồm C O 2 và N 2 . Các thể tích ở đktc. Xác định công thức đơn giản nhất của chất A.
Theo định luật bảo toàn khối lượng :
![]()
Đặt số mol C O 2 là a, số mol N2 là b, ta có :
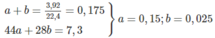
Khối lượng C: 0,150 x 12,0 = 1,80 (g).
Khối lượng H: 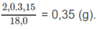
Khối lượng N: 0,0250 x 28,0 = 0,700 (g).
Khối lượng O: 4,48 - 1,80 - 0,35 - 0,700 = 1,60 (g).
Chất A có dạng C x H y N z O t
x : y ; z : t = 0,15 : 0,35 : 0,05 : 0,10 = 3 : 7 : 1 : 2
Công thức đơn giản nhất của A là C 3 H 7 N O 2
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 0,01 mol chất hữu cơ X cần vừa đủ 0,616 lít O2. Sau thí nghiệm thu đc 1,344 lít hỗn hợp sản phẩm Y gồm: CO2 , N2 và H2O . Làm lạnh để ngưng tụ hơi H2O chỉ còn 0,56 lít hỗn hợp khí Z ( có tỉ khối hơi với H2 là 20,4). Biết thể tích các khí đều đo ở đktc. CTPT của X là?
Xem chi tiết
Đốt cháy hoàn toàn 0,01 mol chất hữu cơ X cần vừa đủ 0,616 lít O2. Sau thí nghiệm thu được hỗn hợp sản phẩm Y gồm : CO2, N2 và hơi H2O. Làm lạnh để ngưng tụ hơi H2O chỉ còn 0,56 lít hỗn hợp khí Z (có tỉ khối hơi với H2 là 20,4). Biết thể tích các khí đều đo ở đktc. Công thức phân tử X là A. C2H5ON hoặc C2H7O2N B. C2H5O2N C. C2H7O2N D. C2H5ON
Đọc tiếp
Đốt cháy hoàn toàn 0,01 mol chất hữu cơ X cần vừa đủ 0,616 lít O2. Sau thí nghiệm thu được hỗn hợp sản phẩm Y gồm : CO2, N2 và hơi H2O. Làm lạnh để ngưng tụ hơi H2O chỉ còn 0,56 lít hỗn hợp khí Z (có tỉ khối hơi với H2 là 20,4). Biết thể tích các khí đều đo ở đktc. Công thức phân tử X là
A. C2H5ON hoặc C2H7O2N
B. C2H5O2N
C. C2H7O2N
D. C2H5ON
Đốt cháy hoàn toàn m gam hợp chất A hữu cơ cần dùng vừa đủ 13,44 lít khí O2 (ở ĐKTC) thu được sản phẩm là CO2 và H2O với tỉ lệ số mol lần lượt là 2:3. Xác định CTHH của A biết PTKA = 40
Trộn hỗn hợp khí A gồm 3 hidrocacbon với hỗn hợp khí B gồm khí oxi và ozon theo tỉ lệ thể tích VA:VB 3 : 6,4. Bật tia lửa điện để đốt cháy hoàn toàn thì hỗn hợp khí sau phản ứng chỉ gồm CO2 và H2O có VCO2:VH2O 2,6:2,4. Tính dA/H2 biết dB/H2 19? A. 6 B. 12 C. 8 D. 10
Đọc tiếp
Trộn hỗn hợp khí A gồm 3 hidrocacbon với hỗn hợp khí B gồm khí oxi và ozon theo tỉ lệ thể tích VA:VB = 3 : 6,4. Bật tia lửa điện để đốt cháy hoàn toàn thì hỗn hợp khí sau phản ứng chỉ gồm CO2 và H2O có VCO2:VH2O = 2,6:2,4. Tính dA/H2 biết dB/H2 = 19?
A. 6
B. 12
C. 8
D. 10
Đáp án B
Từ dB/H2 = 19 tính được nO2 : nO3 = 5 : 3
Giả sử nA =3; nB = 6,4 → nO2 = 4; nO3 = 2,4; → nO = 4.2+2,4.3=15,2
Đặt CTC 3 hidrocacbon là CxHy
CxHy + (2x+y/2)O → xCO2 + y/2H2O
Ta có 2x/y = 2,6/2,4 và 2x + y/2 = 15,2/3 → x = 26/15; y = 3,2
MA = 12.26/15 + 3,2 = 24; dA/H2 =12
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 2,82 gam chất hữu cơ A cần 2,856 lít khs O2 thu được khí CO2 và hơi nước theo tỉ lệ thể tích Vco2/Vh2o = 4/3 ( các khi đo ở điều kiện tiêu chuẩn ) . Hãy xác định công thức phân tử của A . Biết tỉ khối của A với không khí nhỏ hơn 7
Ta có: \(n_{O_2}=\dfrac{2,856}{22,4}=0,1275\left(mol\right)\)
\(\dfrac{V_{CO_2}}{V_{H_2O}}=\dfrac{4}{3}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{4}{3}\)
Gọi: nCO2 = 4x (mol) ⇒ nH2O = 3x (mol)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O
⇒ 2,82 + 0,1275.32 = 4x.44 + 3x.18
⇒ x = 0,03
⇒ nCO2 = 0,03.4 = 0,12 (mol) = nC
nH2O = 0,03.3 = 0,09 (mol) ⇒ nH = 0,09.2 = 0,18 (mol)
Ta có: mC + mH = 0,12.12 + 0,18.1 = 1,62 (g) < 2,82 (g)
→ A chứa C, H và O.
⇒ mO = 2,82 - 1,62 = 1,2 (g) \(\Rightarrow n_O=\dfrac{1,2}{16}=0,075\left(mol\right)\)
Gọi CTPT của A là CxHyOz
⇒ x:y:z = 0,12:0,18:0,075 = 8:12:5
→ CTPT của A có dạng là (C8H12O5)n (n nguyên dương)
Mà: \(M_A< 29.7=203\left(g/mol\right)\)
\(\Rightarrow\left(12.8+12.1+16.5\right)n< 203\)
⇒ n < 1,08 ⇒ n = 1
Vậy: CTPT của A là C8H12O5.
Đúng 1
Bình luận (2)
MỌI NGƯỜI GIÚP MIK TÝ NHA
đốt cháy hoàn toàn 8 g chất a cần vừa đủ 22,4 lít khí h2 hỗn hợp sản phẩm cháy gồm co2 và hơi h2o có tỷ lệ thể tích v co2 :v h2o +1:2 xác định công thức phân tử của a biết tỷ khối a/h2 =8
\(n_{O_2}=\frac{22,4}{22,4}=1mol\)
BT O: \(n_{CO_2}+0,5n_{H_2O}=n_{O_2}=1\)
Mà \(n_{CO_2}:n_{H_2O}=1:2\)
\(\rightarrow n_{CO_2}=0,5mol\) và \(n_{H_2O}=1mol\)
BT C và H: \(n_C=n_{CO_2}=0,5mol\) và \(n_H=2n_{H_2O}=2mol\)
Có \(m_C+m_H=0,5.12+2=8=m_A\)
Vậy A chỉ chứa C và H
\(\rightarrow n_C:n_H=0,5:2=1:4\)
Vậy CTPT của A có dạng là \(\left(CH_4\right)_n\)
Mà \(M_A=M_{H_2}.8=16\)
\(\rightarrow\left(12+4\right).n=16\)
\(\rightarrow n=1\)
Vậy CTPT của A là \(CH_4\)
Để đốt cháy hoàn toàn một lượng chất hữu cơ A phải dùng vừa hết 3,08 lít
O
2
. Sản phẩm thu được chỉ gồm có 1,80 g
H
2
O
và 2,24 lít
C
O
2
. Các thể tích khí đo ở đktc.1. Xác định công thức đơn giản nhất của A.2. Xác định công thức phân tử của A, biết rằng tỉ khối hơi của A đối với oxi là 2,25.3. Xác định công thức cấu tạo có thể có của chất A, ghi...
Đọc tiếp
Để đốt cháy hoàn toàn một lượng chất hữu cơ A phải dùng vừa hết 3,08 lít O 2 . Sản phẩm thu được chỉ gồm có 1,80 g H 2 O và 2,24 lít C O 2 . Các thể tích khí đo ở đktc.
1. Xác định công thức đơn giản nhất của A.
2. Xác định công thức phân tử của A, biết rằng tỉ khối hơi của A đối với oxi là 2,25.
3. Xác định công thức cấu tạo có thể có của chất A, ghi tên tương ứng, biết rằng A là hợp chất cacbonyl.
1. Theo định luật bảo toàn khối lượng:
m A = m C O 2 + m H 2 O − m O 2
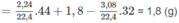
Khối lượng C trong 1,8 g A là: 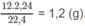
Khối lượng H trong 1,8 g A là: 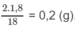
Khối lượng O trong 1,8 g A là : 1,8 - 1,2 - 0,2 = 0,4 (g).
Công thức chất A có dạng C x H y O z :
x : y : z = 0,1 : 0,2 : 0,025 = 4 : 8 : 1
CTĐGN là C 4 H 8 O
2. M A = 2,25.32 = 72 (g/mol)
⇒ CTPT trùng với CTĐGN: C 4 H 8 O .
3. Các hợp chất cacbonyl C 4 H 8 O :
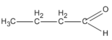 (butanal)
(butanal)
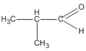 (2-metylpropanal)
(2-metylpropanal)
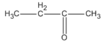 (butan-2-ol)
(butan-2-ol)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 0,3 mol hỗn hợp X gồm hiđrocacbon A và hợp chất hữu cơ B có công thức CxHyOz ( x ≥ 2 ), cần dùng vừa đủ 14,56 lít O2 (đktc), thu được 8,96 lít CO2 (đktc) và 9,9 gam H2O. Xác định công thức phân tử của A và B














