Sắt tác dụng ãit clohiđric
ta có PTHH sau: Fe+2HCl--->FeCl2+H2
Nếu 1,4g Fe tham gia phản ứng hết với lượng dung dịch axít trên
Hãy tính
a)KL axit Clohiđric cần dùng.(1,825)
b)V H2 thu đc đktc(0,56 lít)
Sắt tác dụng axit clohiđric : Ta có phương trình hóa học sau : Fe + 2HCl → FeCl2 + H2
Nếu 1,4g Fe tham gia phản ứng hết với lượng dung dịch axít trên. Hãy tính :
a) Khối lượng axit Clohiđric cần dùng .(1,825g)
b) Thể tích khí H2 thu được đktc .(0,56 lít)
\(n_{Fe}=\dfrac{1.4}{56}=0.025\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.025.....0.05...............0.025\)
\(m_{HCl}=0.05\cdot36.5=1.825\left(g\right)\)
\(V_{H_2}=0.025\cdot22.4=0.56\left(l\right)\)
Sắt tác dụng với axit clohiđric : Fe + 2HCl → FeCl2 + H2↑.
Nếu có 2,8g sắt tham gia phản ứng em hãy tìm:
a) Thể tích khí hiđro thu được ở đktc.
b) Khối lượng axit clohiđric cần dùng.
a) PTPU

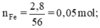
Theo pt: nH2 = nFe = 0,05 (mol)
VH2 = 22,4.n = 22,4.0,05 = 1,12 (l)
b) nHCl = 2.nFe = 2. 0,05 = 0,1 (mol)
mHCl = M.n = 0,1.36,5 = 3,65 (g)
Sắt tác dụng với axit clohiđric theo PTHH:
Fe + 2HCl -> FeCl2 + H2
Nếu có 2,8g Fe tham gia phản ứng, khối lượng khí H2 thu được là:
A. 0,3g H2
B. 0,2g H2
C. 1,0 g H2
D. 0,1g H2
\(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Fe}=0,05\left(mol\right)\)
\(\Rightarrow m_{H_2}=0,05.2=0,1\left(g\right)\)
Chọn D
Cho 14g fe tác dụng với axit Clohiđric (HCL) sau phản ứng thu được muối fe (II) clorua (feCl2) và khí H2 a) lập phương trình hóa học B) tính khối lượng axit Clohiđric tham gia phản ứng C) tính thể tích khí hiđro sinh ra ở ĐKTC Biết : fe=56 Clo=35,5
a)
$n_{Fe} = \dfrac{14}{56} = 0,25(mol)$
$Fe + 2HCl \to FeCl_2 + H_2$
b) $n_{HCl} = 2n_{Fe} = 0,5(mol) \Rightarrow m_{HCl} = 0,5.36,5 = 18,25(gam)$
c) $n_{H_2} = n_{Fe} = 0,25(mol) \Rightarrow V_{H_2} = 0,25.22,4 = 5,6(lít)$
Sắt tác dung với axit clohidric:
Ta có phương trình hóa học sau : Fe + 2HCl -----> \(FeCl_2+H_2\)
Nếu 1,4g Fe tham gia phản ứng hết với lượng dung dịch axit trên.
Hãy tính:
a,Khối lượng axit clohidric cần dùng.
b,Thể tích khí \(H_2\) thu được ở đktc.(0,56 lít)
![]()
a)
\(n_{Fe} = \dfrac{1,4}{56} = 0,025(mol)\)
Theo PTHH : \(n_{HCl} = 2n_{Fe} = 0,05(mol)\\ \Rightarrow m_{HCl} = 0,05.36,5 = 1,825(gam)\)
b)
Ta có :
\(n_{H_2} = n_{Fe} = 0,025(mol)\\ \Rightarrow V_{H_2} = 0,025.22,4 = 0,56(lít)\)
Sắt tác dụng với axit clohiđric:
Fe + 2HCl → FeCl2 + H2.
Nếu có 2,8 g sắt tham gia phản ứng, em hãy tìm:
a) Thể tích khí hiđro thu được ở đktc.
b) Khối lượng axit clohiđric cần dùng.
Số mol sắt tham gia phản ứng:
nFe = 0,05 mol
a) Thể tích khí hiđro thu được ở đktc:
Fe + 2HCl → FeCl2 + H2.
Theo phương trình hóa học, ta có: = nFe = 0,05 mol
Thể tích khí thu được ở đktc là: = 22,4 . n = 22,4 . 0,05 = 1,12 lít
b) Khối lượng axit clohiđric cần dùng
Theo phương trình hóa học, ta có:
nHCl = 2nFe = 2 . 0,05 = 0,1 mol
Khối lượng HCl cần dùng là: mHCl = M . n = 0,1 . 36,5 = 3,65 g
a) nFe = 2,8 / 56 = 0,05 mo
l Phương trình hoá học:
Fe + 2HCl -----> FeCl2 + H2
0, 05 mol 2.0,05 mol 0,05 mol
Theo phương trình trên ta có
nFe = nH = 0,05 VH2= 0,05 x 22,4 = 1,12 l.
b) nHCl = 2nFe = 2 x 0,05 = 0,1 mol
mHCl cần dùng: 0,1 x 36,5 = 3,65 g.
. Cho 5,6g Fe tác dụng với dung dịch axit clohiđric HCl tạo ra 12,7g sắt (II) clorua FeCl2 và 0,2g khí H2.
a. Viết phương trình hóa học của phản ứng trên
b. Tính khối lượng của axit HCl đã ph ản ứng
c. Tính V c ủa khí H2 ở đktc
(Cho:H=1, C=12; N=14; O=16; Al= 27; S=32; Cl= 35,5; Ca=40; Fe=56; Ba=137)
a) \(PTHH:Fe+HCL\) → \(FeCl_2+H_2\)
Cân bằng: \(Fe+2HCl\) → \(FeCl_2+H_2\)
b) \(n_{Fe}=\dfrac{m}{M}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(n_{HCl}=2.n_{Fe}=2.0,1=0,2\left(mol\right)\)
\(m_{HCl}=n.M=0,2.36,5=7,3\left(g\right)\)
c) \(n_{Fe}=n_{H_2}=0,1\left(mol\right)\)
\(V_{H_2\left(đktc\right)}=n.22,4=0,1.22,4=2,24\left(l\right)\)
sắt tác dụng với axit clohidric HCL theo sơ đồ phản ứng sau fe + HCL ---> FeCl2 +H2
nếu có 11,2 gam sắt tham gia phản ứng Hãy tính
a. khối lượng axit chohidric HCL cần dùng
b. thể tích khí hidro tạo thành ở đktc
( cho biết Fe = 56 ; Zn = 65 ; S=32; O = 16 ; K= 39; H=1 ; C=12; CL=35)
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
_____0,2_____0,4__________0,2 (mol)
a, \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
b, \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Fe + 2HCl -> FeCl2 + H2
Nếu có 2,8 g sắt tham gia phản ứng, em hãy tìm:
a) Thể tích khí hidro thu được ở đktc.
b) Khối lượng axit clohidric cần dùng.
chưa học tới đó ms học phần 2 ÙvÚ
a) PTPU
Tháy hình ko ạ , ko thấy = ib
a) Để tìm VH2 ,cần tìm n ( số mol chất)
m=2,8 ; M= 56
=> n= \(\frac{2,8}{56}\)
= 0.05 (mol)
n=0.05 =>V= n.22,4
= 0,05.22,4
=1,12(l)
Phần b) chưa học hihi sorry b