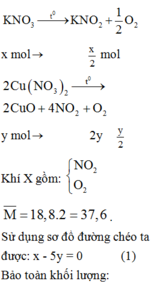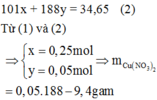Biết dX/H2=18,8.Tìm X

Những câu hỏi liên quan
Cho 5,6 lít hỗn hợp khí X gồm CO và CO2 (đktc). Biết X có tỉ khối so với H2 là 18,8. Tính số mol và % số mol mỗi khí trong hỗn hợp X.
Gọi $n_{CO} = a(mol) ; n_{CO_2} = b(mol)$
Ta có :
$n_X = a + b = 0,25(mol)$
$m_X = 28a + 44b = 18,8.2.0,25 = 9,4(gam)$
$\Rightarrow a = 0,1 ; b = 0,15
$\%n_{CO} = \dfrac{0,1}{0,25}.100\% = 40\%$
$\%n_{CO_2} = 100\% -40\% = 60\%$
Đúng 1
Bình luận (0)
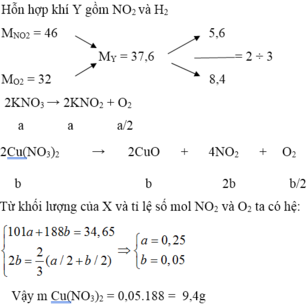
Nhiệt phân hết 34,65 gam X gồm KNO3 và Cu(NO3)2 được hỗn hợp khí Y, dY/H2 = 18,8. Tìm khối lượng của Cu(NO3)2 trong X :
A. 9,4g
B. 11,28g
C. 20,5g
D. 8,6g
tính % thể tích mỗi khí trong 0,02 mol hỗn hợp X gồm SO2 và CO2. biết dX/H2=28
Ta có: \(\overline{M}=28.2=56\)
Gọi %V của SO2 là x
Ta có:
\(x.M_{SO_2}+\left(1-x\right).M_{CO_2}=56\\ \Rightarrow64x+44-44x=56\\ \Rightarrow x=0,6\)
Vậy %SO2 = 60% và %CO2 = 40%
Đúng 3
Bình luận (0)
Cho 18,8 gam hỗn hợp M gồm C2H5OH và một ancol đồng đẳng X tác dụng với Na dư thu được 5,6 lít khí H2 (đktc). Oxi hóa 18,8 gam M bằng CuO, nung nóng thu được hỗn hợp Y gồm 2 anđehit (h100%). Cho Y tác dụng hết với dung dịch AgNO3 trong NH3 , thu được m gam Ag. Giá trị của m là: A. 86,4. B. 172,8. C. 108,0. D. 64,8.
Đọc tiếp
Cho 18,8 gam hỗn hợp M gồm C2H5OH và một ancol đồng đẳng X tác dụng với Na dư thu được 5,6 lít khí H2 (đktc). Oxi hóa 18,8 gam M bằng CuO, nung nóng thu được hỗn hợp Y gồm 2 anđehit (h=100%). Cho Y tác dụng hết với dung dịch AgNO3 trong NH3 , thu được m gam Ag. Giá trị của m là:
A. 86,4.
B. 172,8.
C. 108,0.
D. 64,8.
Đáp án : B
nH2 = 0,25 mol => n ancol = 0,5 mol
=> M tb = 18 , 8 0 , 5 = 37,6
=> Ancol còn lại là CH3OH. Gọi nCH3OH = x, nC2H5OH = y
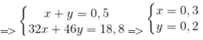
=> nAg = 4x + 2y = 1,6 mol => m = 1,6.108 = 172,8 g
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2, thu được hỗn hợp khí X (tỉ khối của X so với H2 là 18,8). Khối lượng của Cu(NO3)2 trong hỗn hợp là: A. 9,40 gam. B. 11,28 gam. C. 8,60 gam. D. 20,50 gam.
Đọc tiếp
Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2, thu được hỗn hợp khí X (tỉ khối của X so với H2 là 18,8). Khối lượng của Cu(NO3)2 trong hỗn hợp là:
A. 9,40 gam.
B. 11,28 gam.
C. 8,60 gam.
D. 20,50 gam.
Đốt cháy 5,6g hợp chất X thu được 8,96l khí CO2 (đktc) và 7,2 ml nước lỏng. Xác định CTHH của hợp chất X, biết dX/H2=14
Do đốt cháy A thu được sản phẩm chứa C, H ,O
=> A chứa C, H và có thể có O
\(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
=> nC = 0,4 (mol)
mH2O = 7,2.1 = 7,2 (g)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
=> nH = 0,8 (mol)
Xét mC + mH = 0,4.12 + 0,8.1 = 5,6 (g)
=> A chứa C, H
Xét nC : nH = 0,4 : 0,8 = 1 : 2
=> CTHH: (CH2)n
Mà MX = 14.2 = 28 (g/mol)
=> n = 2
=> CTHH: C2H4
Đúng 9
Bình luận (0)
Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2, thu được hỗn hợp khí X (tỉ khối của X so với khí H2 bằng 18,8). Khối lượng Cu(NO3)2 trong hỗn hợp ban đầu là: A. 8,6 gam. B. 20,5 gam. C. 11,28 gam. D. 9,4 gam.
Đọc tiếp
Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2, thu được hỗn hợp khí X (tỉ khối của X so với khí H2 bằng 18,8). Khối lượng Cu(NO3)2 trong hỗn hợp ban đầu là:
A. 8,6 gam.
B. 20,5 gam.
C. 11,28 gam.
D. 9,4 gam.
Gọi n K N O 3 = x và n C u ( N O 3 ) 2 = y
Hỗn hợp khí X thu được gồm khí O2 và khí NO2.
Ta có M = 18,8 . 2 = 37,6
Các phản ứng xảy ra như sau:
K N O 3 → t 0 K N O 2 + 1 2 O 2
Mol x x 2
C u ( N O 3 ) 2 → t 0 C u O + 2 N O 2 + 1 2 O 2
Mol y 2y y 2
Đến đây, ta có thể sử dụng 2 cách:
Cách 1: Sơ đồ đường chéo
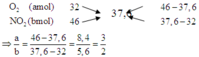
Cách 2: Tính toán thông thường:
Gọi X là tỉ lệ số mol của O2 với tổng số mol hỗn hợp
Suy ra tỉ lệ mol của NO2 với tổng số mol hỗn hợp là (1 – X).
Khi đó M = 32X + 46(1-X) = 37,6 ⇔ X = 0,6
Suy ra, tỉ lệ số mol của NO2 so với tổng số mol khí là 0,4
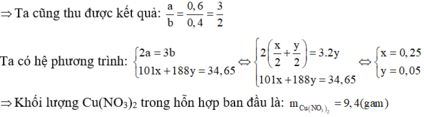
Đáp án D.
Đúng 0
Bình luận (0)
cho dx/h2=8,5 và dx/y =0,5 tìm khối lượng mol cua khi x va khí y
\(d_{\dfrac{X}{H_2}}=8,5\\ M_{H_2}=2\\ \Rightarrow M_X=d_{\dfrac{X}{H_2}}.M_{H_2}=8,5.2=17\left(g\right)\)
\(d_{\dfrac{X}{Y}}=0,5\\ \Rightarrow d_{\dfrac{Y}{X}}=2\\ M_X=17\\ \Rightarrow M_Y=d_{\dfrac{Y}{X}}.M_X=2.17=34\left(\dfrac{g}{mol}\right)\)
Đúng 1
Bình luận (0)
Ta có: dx/h2 = 8,5
=> Mx = 8,5 . 2 = 17 (g/mol)
dx/y = 0,5
=> My = \(\dfrac{17}{0,5}\) = 34 (g/mol)
Vậy Mx = 17 (g/mol)
My = 34 (g/mol)
Đúng 0
Bình luận (0)
Tính số mol của mỗi khí trong 3,36(l) (đktc) hỗn hợp khí X gồm N2O , biết dX/H2 = 18,5