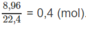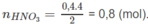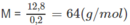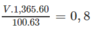1. Hòa tan 12,8g kim loại hóa trị 2 trong 1 lượng vừa đủ dung dịch HNO3 60% D=1,365g/ml thu được 8,96l khí màu nâu đỏ . Xác định kim loại
2. Cho 2,16 g kim loại hóa trị 3 td với dd HNO3 loãng dư thu được 0,27mol hỗn hợp khí N2O và N2 có tỉ khối so với H2 là 18,45 .tìm kim loại
3. Dung dịch của chất nào sau đây có khả năng dẫn điện
A. NaCl
B. C2H5OH
C. HCHO
D. C6H12O6
4. Nguyên nhân tính dẫn điện của dung dịch các chất điện li là
A. Phân tử các chất hòa tan
B. Các ion trong dung dịch
C. Các anion trong dung dịch
D. Các cation trong dung dịch
5. Chất điện li là
A. Chất tan được trong nước hoặc có thể nóng chảy
B. Chất dẫn điện
C. Chất phân li thành các cation tan trong nước hoặc ở trạng thái nóng chảy
D. Chất không tan trong nước và không thể nóng chảy
6. Chất nào sau đây không là chất điện li
A. CH3 COOH
B. CH3COONa
C. CH3COONH4
D. C2H5OH