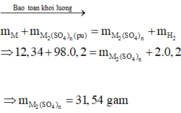Trung hòa hết 5.6g một hiđroxit của kim loại nhóm IA cần dùng hết 100ml dung dịch HCL 1M. Kim loại nhóm IA đó là?

Những câu hỏi liên quan
7. Trung hòa dung dịch có chứa 1,12 gam một hiđroxit của kim loại kiềm R (R thuộc nhóm IA trong bảng tuần hoàn các nguyên tố hóa học) cần vừa đủ 200 ml dung dịch axit clohiđric 0,1M.
a. Xác định tên kim loại kiềm R?
b. Tính khối lượng muối thu được khi cô cạn dung dịch thu được sau phản ứng?
hòa tan 4,8g hỗn hợp 2 kim loại A,B thuộc 2 chu kì liên tiếp của nhóm IA tác dụng với dd HCl 1M dư thu được 1,792 lít khí ở dktc a) Xác định tên 2 kim loại kiềm b) Tính thể tích dung dịch HCl đã dùng biết đã lấy dư 25% so với lượng cần dùng cho p/ư
a) \(n_{H_2}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
2A + 2HCl --> 2ACl + H2
2B + 2HCl --> 2BCl2 + H2
=> nA + nB = 2.nH2 = 0,16
=> \(\overline{M}_{hh}=\dfrac{4,8}{0,16}=30\)
Mà A, B thuộc 2 chu kì liên tiếp nhóm IA
=> A, B là Na, K
b)
Gọi số mol Na, K là a,b
=> 23a + 39b = 4,8
2Na + 2HCl --> 2NaCl + H2
_a----->a-------------->0,5a
2K + 2HCl --> 2KCl + H2
_b--->b-------------->0,5b
=> 0,5a + 0,5b = 0,08
=> a = 0,09; b = 0,07
nHCl(PTHH) = a + b = 0,16
=> nHCl(thực tế) = 0,16.125% = 0,2(mol)
=> \(V_{ddHCl}=\dfrac{0,2}{1}=0,2\left(l\right)\)
Đúng 0
Bình luận (0)
Để trung hòa hết 16g một hiđroxit của 1 kim loại nhóm IA cần dùng hết 500ml dung dịch HCl 0,8M. Tìm công thức của hiđroxit trên.
MOH+HCl--->MCl+H2O
Ta có
n HCl=0,5.0,8=0,4(mol)
Theo pthh
n MOH=n HCl=0,4(mol)
M\(_{MOH}=\frac{16}{0,4}=40\)
M\(_M=40-17=23\)
Vậy M là Na
CTHH:NaOH
Chúc bạn học tốt
giúp em không biết làm hòa tan 2,3 gram kim loại a vào nước thu được dung dịch kiềm để trung hòa hết lượng kiềm trên phải dùng 100ml dung dịch hcl 1M kim loại a là gì
\(n_{HCl}=0,1.1=0,1\left(mol\right)\)
PTHH: \(2A+2xH_2O\rightarrow2A\left(OH\right)_x+xH_2\)
\(2A\left(OH\right)_x+2xHCl\rightarrow2ACl_x+2xH_2O\)
=> \(n_A=\dfrac{0,1}{x}\left(mol\right)\Rightarrow M_A=\dfrac{2,3}{\dfrac{0,1}{x}}=23x\left(g/mol\right)\)
Xét x = 1 => MA = 23(Na)
Đúng 3
Bình luận (0)
\(n_{HCl}=0.1\cdot1=0.1\left(mol\right)\)
\(A+H_2O\rightarrow AOH+\dfrac{1}{2}H_2\)
\(AOH+HCl\rightarrow ACl+H_2O\)
\(n_A=n_{AOH}=n_{HCl}=0.1\left(mol\right)\)
\(M_A=\dfrac{2.3}{0.1}=23\left(g\text{/}mol\right)\)
\(A:Na\)
Đúng 0
Bình luận (0)
Cho 7,2 gam hỗn hợp hai kim loại nhóm IA, thuộc hai chu kỳ liên tiếp, tác dụng hết với dung dịch HCl dư thu được 4,48 lít khí hiđro (đktc). Hai kim loại đó là
Gọi CTTQ hai kim loại kiềm là R
$n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$2R + 2HCl \to 2RCl + H_2$
$n_R = 2n_{H_2} = 0,2.2 = 0,4(mol)$
$\Rightarrow M_R = \dfrac{7,2}{0,4} = 18(g/mol)$
Ta thấy : $M_{Liti} = 7 < 18 < M_{Natri} = 23$
Do đó hai kim loại đó là Liti và Natri
Đúng 2
Bình luận (0)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ \text{Đ}\text{ặt}-chung-2kl:A\\ A+HCl\rightarrow ACl+\dfrac{1}{2}H_2\\ n_A=2.0,2=0,4\left(mol\right)\\ M_A=\dfrac{7,2}{0,4}=18\left(\dfrac{g}{mol}\right)\\ \Rightarrow2KL:Liti\left(Li\right),Natri\left(Na\right)\)
Đúng 1
Bình luận (0)
Hòa tan 19,5 gam kim loại trong nhóm IA trong Vml dung dịch HCl 0,1M thu được 5,6 lít khí ( đktc). Xác định tên kim loại
A. K
B. Li
C. Na
D. Ca
Đáp án A
2R + 2HCl → 2RCl + H2
Ta có: nH2 = 0,25 mol => nR =0,25 .2 = 0,05 mol
=> MR=19,5/0,5 = 39
Vậy R là nguyên tố K
Đúng 0
Bình luận (0)
Hòa tan hết 1,29g 1 kim loại X thuộc nhóm 2A bằng dung dịch HCL 0,5M thu đc 1,2395 lít khí ( đkc ). Thể tích dung dịch HCL cần dùng là?
Ta có: \(n_{H_2}=\dfrac{1,2395}{24,79}=0,05\left(mol\right)\)
BTNT H, có: nHCl = 2nH2 = 0,1 (mol)
\(\Rightarrow V_{ddHCl}=\dfrac{0,1}{0,5}=0,2\left(l\right)\)
Đúng 3
Bình luận (0)
Hòa tan 1,7 gam hỗn hợp kim loại A và Zn vào dung dịch HCl thu được 0,672 lít khí ở điều kiện tiêu chuẩn và dung dịch B. Mặt khác để hòa tan 1,9 gam kim loại A thì cần không hết 200ml dung dịch HCl 0,5M. A thuộc phân nhóm chính nhóm II. Kim loại M là: A. Ca B. Cu C. Mg D. Sr
Đọc tiếp
Hòa tan 1,7 gam hỗn hợp kim loại A và Zn vào dung dịch HCl thu được 0,672 lít khí ở điều kiện tiêu chuẩn và dung dịch B. Mặt khác để hòa tan 1,9 gam kim loại A thì cần không hết 200ml dung dịch HCl 0,5M. A thuộc phân nhóm chính nhóm II. Kim loại M là:
A. Ca
B. Cu
C. Mg
D. Sr
Đáp án A
Vì A và Z đều có hóa trị II khi tác dụng với dung dịch HCl nên gọi công thức chung

Đúng 1
Bình luận (0)
Hòa tan hết 12.34 gam hỗn hợp kim loại X gồm 3 kim loại thuộc nhóm IA và IIA tác dụng với lượng dư dung dịch
H
2
SO
4
loãng thu được 4,48 lít khí
H
2
(đktc) và m gam hỗn hợp muối. Giá trị của m là A. 31,54. B. 30,50. C. 28,14. D. 45,00.
Đọc tiếp
Hòa tan hết 12.34 gam hỗn hợp kim loại X gồm 3 kim loại thuộc nhóm IA và IIA tác dụng với lượng dư dung dịch H 2 SO 4 loãng thu được 4,48 lít khí H 2 (đktc) và m gam hỗn hợp muối. Giá trị của m là
A. 31,54.
B. 30,50.
C. 28,14.
D. 45,00.