Tính thể tích etlen cần thiết để tổng hợp 280 PE
Trong công nghiệp polietilen (PE) được điều chế từ metan theo sơ đồ
C H 4 → H 2 - 80 % C 2 H 2 → H 2 - 80 % C 2 H 4 → H 2 - 80 % P E
Để tổng hợp 5,376 kg PE theo sơ đồ trên cần V m3 khí thiên nhiên (đktc, chứa 75% metan theo thể tích). Giá trị của V là
A. 11,2
B. 22,4
C. 28,0
D. 16,8
Trong công nghiệp polietilen (PE) được điều chế từ metan theo sơ đồ:
C H 4 → H 2 = 80 % C 2 H 2 → H 2 = 80 % C 2 H 4 → H 2 = 80 % P E
Để tổng hợp 5,376 kg PE theo sơ đồ trên cần V m 3 khí thiên nhiên (đktc, chứa 75% metan theo thể tích). Giá trị của V là
A. 11,2
B. 22,4
C. 28,0
D. 16,8
Trong công nghiệp polietilen (PE) được điều chế từ metan theo sơ đồ
CH 4 → H 2 = 80 % C 2 H 2 → H 2 = 80 % C 2 H 4 → H 2 = 80 % P E
Để tổng hợp 5,376 kg PE theo sơ đồ trên cần V m3 khí thiên nhiên (đktc, chứa 75% metan theo thể tích). Giá trị của V là
A. 11,2
B. 22,4
C. 28,0
D. 16,8
Trong công nghiệp polietilen (PE) được điều chế từ metan theo sơ đồ:
C H 4 → H 1 = 80 % C 2 H 2 → H 2 = 80 % C 2 H 4 → H 3 = 80 % P E
Để tổng hợp 5,376 kg PE theo sơ đồ trên cần V m 3 khí thiên nhiên (đktc, chứa 75% metan theo thể tích). Giá trị của V là
A. 11,2
B. 22,4
C. 28,0
D. 16,8
Dung dịch A chứa 8g NaoH
a/ Tính thể tích dd H2SO4 0,5M cần dùng để hoà tan A
b/ Tính Thể tích SO2 cần thiết để khi tác dụng với dd A tạo ra hỗn hợp muối axit và muối trung hoà theo tỉ lệ mol tương ứng là 2:1
nNaOH=0,2mol
a) PTHH: 2NaOH+H2SO4=> Na2SO4+2H2O
0,2=>0,1
=> V H2SO4=0,1:0,5=0,2l=200ml
b) 2NaOH+SO2=>Na2SO3+H2O
2/15=>1/15
NaOH+SO2=>NaHSO3
1/15=>1/15
=> VSO2=2.1/15.22,4=2,98l
Đốt cháy hoàn toàn m gam nhôm trong không khí thu được 20,4g nhôm oxit
a. Tính m?
b. Tính thể tích khí O2 ở đktc cần thiết để đốt cháy hết lượng nhôm trên( 2 cách)
c. Tính thể tích kk ở đktc cần thiết để đốt cháy hết lượng nhôm trên, biết thể tích oxi chiếm khoảng 20% thể tích kk?
a) \(n_{Al_2O_3}=\dfrac{20,4}{102}=0,2\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,4<--0,3<---------0,2
=> mAl = 0,4.27 = 10,8(g)
b) C1: VO2 = 0,3.22,4 = 6,72(l)
C2: Theo ĐLBTKL: mO2 = 20,4 - 10,8 = 9,6(g)
=> \(n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)=>V_{O_2}=0,3.22,4=6,72\left(l\right)\)
c) Vkk = 6,72 : 20% = 33,6(l)
Tính thể tích khí oxi và thể tích không khí (đktc) cần thiết để đốt cháy: 1,5mol photpho
Cho biết oxi chiếm 20% thể tích không khí.
Phương trình hóa học khi đốt cháy photpho:
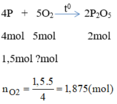
Thể tích của oxi cần: V O 2 = n O 2 .22,4 = 1,875.22,4 = 42(l)
Thể tích của không khí cần dùng là: V k k = 5 V O 2 = 5.42=210(l)
Tính thể tích khí oxi và thể tích không khí (đktc) cần thiết để đốt cháy: 1mol cacbon
Cho biết oxi chiếm 20% thể tích không khí.
Phương trình phản ứng khi đốt cháy cacbon:
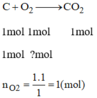
V O 2 = n O 2 .22,4 = 1.22,4 = 22,4(l)
→ V k k = 5 V O 2 = 5.22,4 = 112(l)
a) PTHH: \(S+O_2\underrightarrow{t^o}SO_2\)
Ta có: \(n_{O_2}=n_S=\dfrac{3,2}{32}=0,1\left(mol\right)\) \(\Rightarrow V_{O_2}=0,1\cdot22,4=2,24\left(l\right)\)
b) PTHH: \(C+O_2\underrightarrow{t^o}CO_2\)
Ta có: \(n_{O_2}=n_C=\dfrac{6}{12}=0,5\left(mol\right)\) \(\Rightarrow V_{O_2}=0,5\cdot22,4=11,2\left(l\right)\)
a/
Áp dụng công thức \(m=n.M=>n=\dfrac{m}{M}\)
\(=>n_S=\dfrac{m_S}{M_S}=\dfrac{3.2}{32}=0.1\left(mol\right)\)
PTHH
\(S+O_2\underrightarrow{t^o}SO_2\)
1 1
0.1 x
=>\(x=0.1\cdot1:1=0.1=n_{O_2}\)
\(=>V_{O_2}=0.1\cdot22,4=2.24\left(l\right)\)
a. PT: S + O2 ---> SO2.
Ta có: nS=3,2/32=0,1(mol)
Theo PT, ta có: nS=nO=0,1(mol)
=> VO=0,1.22,4=2,24(l)
=> Vkk=5.VO=5.2,24=11,2(l)
b. PT: C + O2 ---> CO2.
Ta có: nC=6/12=0,5(mol)
Theo PT, ta có: nC=nO=0,5(mol)
=> VO=0,5.22,4=11,2(l)
=> => Vkk=5.VO=5.11,2=56(l)