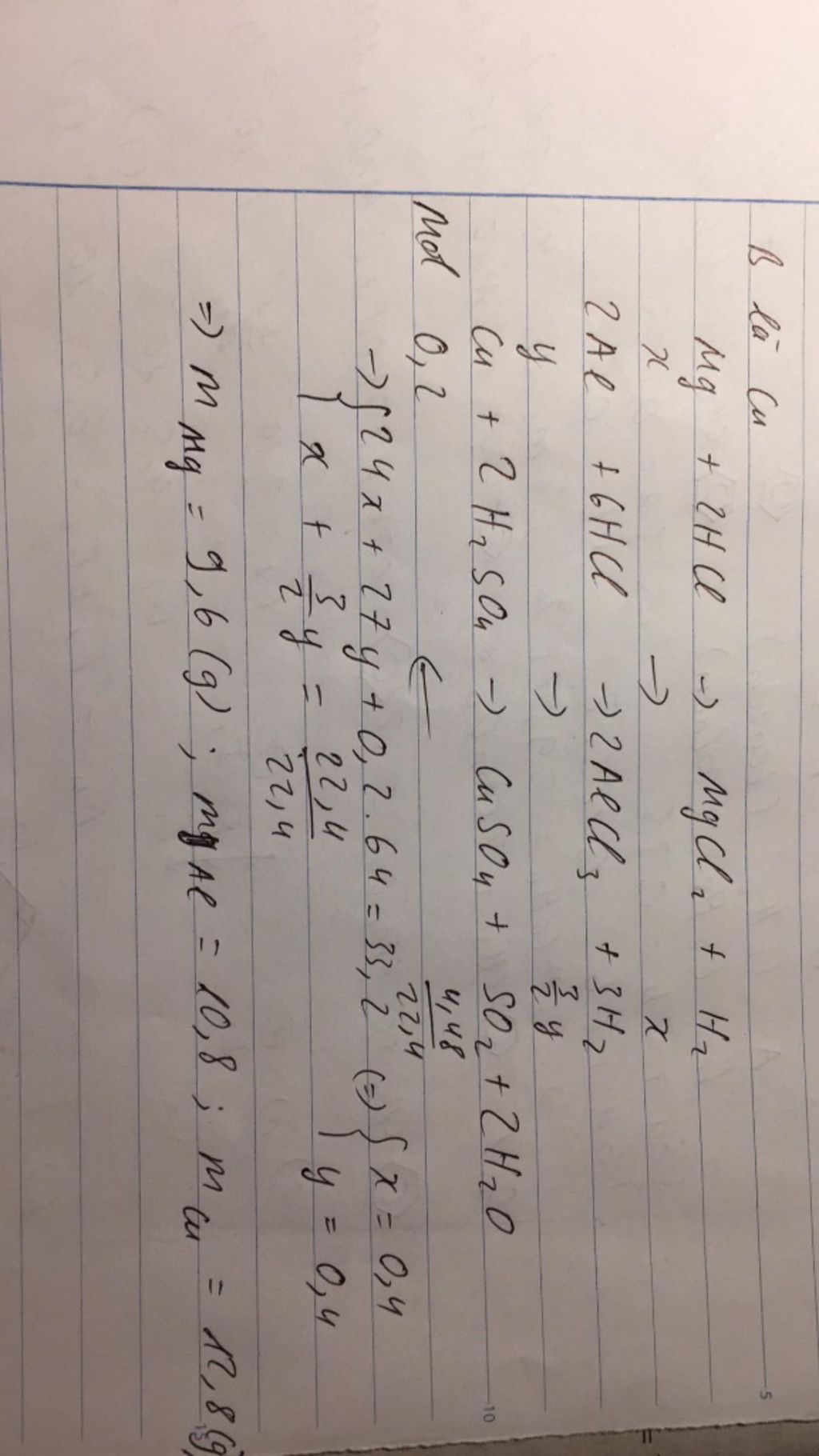Ko viết pthh, áp dụng định luật bảo toàn electron giải
5. Cho 2,4g Mg tác dụng vừa đủ với dung dịch H2SO4 98% nóng thu đc V lít SO2( đktc. Tính V
6. Cho mg Al tác dụng vs dd H2SO4 98% nóng thu đc 10,08 lít H2S( đktc). Tính mg?

Những câu hỏi liên quan
Cho 33,2 g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch HCl thu được V lít khí ở đktc và chất rắn không tan Y. Cho Y hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2 (đktc). Phần trăm khối lượng của Cu trong hỗn hợp X là A. 57,83%. B. 33,33%. C. 19,28%. D. 38,55%.
Đọc tiếp
Cho 33,2 g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch HCl thu được V lít khí ở đktc và chất rắn không tan Y. Cho Y hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2 (đktc). Phần trăm khối lượng của Cu trong hỗn hợp X là
A. 57,83%.
B. 33,33%.
C. 19,28%.
D. 38,55%.
cho 16,8 gam Fe tác dụng vừa đủ với dung dịch H2SO4 đặc nóng, thu được dung dịch A và V lít khí SO2(đktc) A) Tính V B) Cho dung dịch A tác dụng hoàn toàn với dung dịch NaOH thu được m gam kết tủa. Tính m
a, \(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
BT e, có: 3nFe = 2nSO2 ⇒ nSO2 = 0,45 (mol)
⇒ VSO2 = 0,45.22,4 = 10,08 (l)
b, BTNT Fe, có: nFe(OH)3 = nFe = 0,3 (mol)
⇒ mFe(OH)3 = 0,3.107 = 32,1 (g)
Đúng 1
Bình luận (0)
Cho 33,2g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hợp X lần lượt là: A. 13,8;7,6;11,8 B. 11,8;9,6;11,8 C. 12,8;9,6;10,8 D. kết quả khác
Đọc tiếp
Cho 33,2g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hợp X lần lượt là:
A. 13,8;7,6;11,8
B. 11,8;9,6;11,8
C. 12,8;9,6;10,8
D. kết quả khác
Đáp án C.
Kim loại không phản ứng với H2SO4 loãng là Cu.
Gọi nCu = x, nMg = y, nAl = z
Ta có:
64x + 24y + 27z = 33,2 (1)
Bảo toàn e:
2nMg + 3nAl = 2nH2
=> 2y + 3z = 2.1 (2)
2nCu = 2nSO2 => x = 0.2 (mol) (3)
Từ 1, 2, 3 => x = 0,2; y = z = 0,4 (mol)
mCu = 0,2.64 = 12,8 (g)
mMg = 0,4.24 = 9,6 (g)
mAl = 10,8 (g)
Đúng 0
Bình luận (0)
Tính khối lượng dd sau phản ứng. a, cho 12.3 g hỗn hợp al mg zn tác dụng với vừa đủ dd h2so4 9% thu được 7.84 lít khí h2 đktc B, cho 16.2 g hỗn hợp gồm mg al fe tác dụng với vừa đủ dd h2so4 25% thu được 12.32 lít khí h2 đktc
a) Sửa đề: dd H2SO4 9,8%
Ta có: \(n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\) \(\Rightarrow m_{H_2}=0,35\cdot2=0,7\left(g\right)\)
Bảo toàn nguyên tố: \(n_{H_2SO_4}=n_{H_2}=0,35\left(mol\right)\) \(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,35\cdot98}{9,8\%}=350\left(g\right)\)
\(\Rightarrow m_{dd}=m_{KL}+m_{H_2SO_4}-m_{H_2}=361,6\left(g\right)\)
b) Tương tự câu a
Đúng 1
Bình luận (0)
Cho 21,6 gam hỗn hợp X gồm Fe và MgSO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, sau phản ứng thu được 6,72 l hỗn hợp khí (đktc)a) Xác định khối lượng các chất trong Xb) Cho toàn bộ lượng X trên tác dụng với H2SO4 đặc, nóng dư thu được V lít khí SO2 (sản phẩm khử duy nhất ở đktc). Tính Vc) Tính số mol KOH tối thiểu để hấp thụ hết V lít SO2 trênd) Cho 0,03 mol Ba(OH)2 tác dụng hoàn toàn với 0,1 V lít SO2 trên. Tính khối lượng kết tủa thu được
Đọc tiếp
Cho 21,6 gam hỗn hợp X gồm Fe và MgSO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, sau phản ứng thu được 6,72 l hỗn hợp khí (đktc)
a) Xác định khối lượng các chất trong X
b) Cho toàn bộ lượng X trên tác dụng với H2SO4 đặc, nóng dư thu được V lít khí SO2 (sản phẩm khử duy nhất ở đktc). Tính V
c) Tính số mol KOH tối thiểu để hấp thụ hết V lít SO2 trên
d) Cho 0,03 mol Ba(OH)2 tác dụng hoàn toàn với 0,1 V lít SO2 trên. Tính khối lượng kết tủa thu được
Chia m(g) hỗn hợp Fe , FeO, Fe3O4,Fe2O3 thành hai phần bằng nhau. Phần 1 : tác dụng vừa đủ vs 350ml dd H2SO4 loãng 1M giải phóng 3,36 lít khí H2 (đktc). Phần 2 tác dụng với dung dịch H2SO4 đặc, nóng, dư thu được 5,6 lít khí SO2 (đktc). Tính phần trăm khối lượng của Fe trong hỗn hợp.
1/2m hỗn hợp= 39,2
m muối tăng= mSO4-mCl
do nso4(2-)=1/2ncl-(bảo toàn điện tích hoặc có thể viết pt ra là thấy)
83,95-77,7=96.1/2.ncl-35,5ncl
ncl bị thay thế là 0,5
có ở phần 77,7. có btkluong 39,2+36,5.2.a=77.7+18a(a là n h20)
a=0,7 ----- tổng ncl = 1,4
n kloai là 77,7-1,4.35.5=28 ----- nfeo là x fe2o3 y (ở nửa phần) có 56x+112y=28......72x+160y=39,2
x=0,1 y=0,2
%feo=18,36...... fe203=81,64%
b, ncl còn lại=nhcl=1,4-0,5=0,9
nso4=1/2ncl=0.25=nh2so4
CM=(0,25+0,9)/0,5=2,3
Đúng 0
Bình luận (0)
Giúp mk với ạ: Cho 33,2g hỗn hưp X gồm Cu, Mg, Al tác dông vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hựp X lần lượt là: A. 13,8g; 7,6; 11,8 B. 11,8; 9,6; 11,8 C.12,8; 9,6; 10,8 D. kết quả khác
\(n_{SO_2}=0.2\left(mol\right)\)
Bảo toàn e :
\(n_{Cu}=n_{SO_2}=0.2\left(mol\right)\)
\(m_{Cu}=0.2\cdot64=12.8\left(g\right)\)
\(m_{Mg}+m_{Al}=24x+27y=33.2-12.8=20.4\left(g\right)\left(1\right)\)
\(n_{H_2}=x+1.5y=1\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):x=y=0.4\)
\(m_{Mg}=0.4\cdot24=9.6\left(g\right)\)
\(m_{Al}=10.8\left(g\right)\)
=> C
Đúng 0
Bình luận (0)
Cho 27,25 gam hỗn hợp X gồm Mg, Al, Fe, Cu tác dụng với O2 thu được m gam hỗn hợp chất rắn Y. Cho toàn bộ Y tác dụng với dung dịch H2SO4 đặc, nóng, thu được dung dịch Z (chứa 5 muối, với tổng khối lượng muối là 96,85 (gam) và 10,64 lít (đktc) khí SO2 duy nhất. Giá trị của m là A. 38,85. B. 31,25. C. 34,85. D. 20,45.
Đọc tiếp
Cho 27,25 gam hỗn hợp X gồm Mg, Al, Fe, Cu tác dụng với O2 thu được m gam hỗn hợp chất rắn Y. Cho toàn bộ Y tác dụng với dung dịch H2SO4 đặc, nóng, thu được dung dịch Z (chứa 5 muối, với tổng khối lượng muối là 96,85 (gam) và 10,64 lít (đktc) khí SO2 duy nhất. Giá trị của m là
A. 38,85.
B. 31,25.
C. 34,85.
D. 20,45.
Câu 1: Cho 2,58 gam hỗn hợp Mg, Al tác dụng vừa đủ với V dung dịch H2SO4 0,5M loãng thu được 2,91362 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị VCâu 2: Cho 4,96 gam hỗn hợp Fe, Mg tác dụng vừa đủ với 200 gam dung dịch H2SO4 loãng a% thu được 3,136 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị aCâu 3: Cho 3,94 gam hỗn hợp Ba, Mg tác dụng vừa đủ với 100ml dung dịch H2SO4 xM loãng thu được 1,568 lít khí H2 (đktc). Tính khối lượng mỗi...
Đọc tiếp
Câu 1: Cho 2,58 gam hỗn hợp Mg, Al tác dụng vừa đủ với V dung dịch H2SO4 0,5M loãng thu được 2,91362 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị V
Câu 2: Cho 4,96 gam hỗn hợp Fe, Mg tác dụng vừa đủ với 200 gam dung dịch H2SO4 loãng a% thu được 3,136 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị a
Câu 3: Cho 3,94 gam hỗn hợp Ba, Mg tác dụng vừa đủ với 100ml dung dịch H2SO4 xM loãng thu được 1,568 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị x
Câu 1:
\(n_{H_2}=\dfrac{2.91362}{22.4}=0.13mol\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a a a a
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
2b 3b b 3b
Ta có: \(\left\{{}\begin{matrix}24a+54b=2.58\\a+3b=0.13\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0.04\\b=0.03\end{matrix}\right.\)
\(m_{Mg}=0.04\times24=0.96g\)
\(m_{Al}=0.03\times2\times27=1.62g\)
\(V_{H_2SO_4}=\dfrac{0.04+3\times0.03}{0.5}=0.26l\)
Câu 2:
\(n_{H_2}=\dfrac{3.136}{22.4}=0.14mol\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a a a a
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b b b b
Ta có: \(\left\{{}\begin{matrix}24a+56b=4.96\\a+b=0.14\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0.09\\b=0.05\end{matrix}\right.\)
\(m_{Mg}=0.09\times24=2.16g\)
\(m_{Fe}=0.05\times56=2.8g\)
\(C\%_{H_2SO_4}=\dfrac{0.14\times98\times100}{200}=6.86\%\)
Đúng 0
Bình luận (0)
Câu 3:
\(n_{H_2}=\dfrac{1.568}{22.4}=0.07mol\)
\(Ba+H_2SO_4\rightarrow BaSO_4+H_2\)
a a a a
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
b b b b
Ta có: \(\left\{{}\begin{matrix}137a+24b=3.94\\a+b=0.07\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0.02\\b=0.05\end{matrix}\right.\)
\(m_{Ba}=0.02\times137=2.74g\)
\(m_{Mg}=0.05\times24=1.2g\)
\(CM_{H_2SO_4}=\dfrac{0.07}{0.1}=0.7M\)
Đúng 0
Bình luận (0)