Nguyên tử R có 2 đồng vị X và Y. Tổng số các loại hạt của 2 đồng vị là 106. Số nowtron của Y hơn X 2 hạt. Ở trạng thái cơ bản R có 1 e độc thân . Xđ R và số khối mỗi đồng vị.
Biết X có số nguyên tử nhiều hơn Y là 50%. Xđ %m X trong FeR3
Nguyên tố kali có hai đồng vị là X và Y. Biết nguyên tử đồng vị X có điện tích hạt nhân là 19+ và có tổng số hạt cơ bản là 58. Đồng vị Y chiếm 9,5% số nguyên tử, hạt nhân của Y có số nơtron nhiều hơn hạt nhân của X một hạt.
a. Tính số khối mỗi đồng vị?
b. Tính nguyên tử khối trung bình của kali.
c. Tính phần trăm khối lượng của X trong K3PO4 (Cho nguyên tử khối: P = 31, O = 16).
Một nguyên tố R có 3 đồng vị X, Y ,Z; biết tổng số các hạt cơ bản (n, p, e) trong 3 đồng vị bằng 129, số nơtron đồng vị X hơn đồng vị Y một hạt. Đồng vị Z có số proton bằng số nơtron. Số khối của X, Y, Z lần lượt là
A. 26, 27, 29
B. 30, 29,28
C. 28, 29, 30
D. 27, 28, 26
Đáp án B
• Giả sử số hạt nơtron trong X, Y, Z lần lượt là NX, NY, NZ
Vì X, Y, Z là đồng vị nên chúng đều có số p = số e = Z
Ta có hpt:
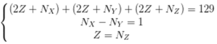
→ 7Z + NY = 128.
• TH1: Z = 13.
→ NZ = 13, NX = 19,5; NY = 18,5 → loại.
• TH2: Z = 14
→ NZ = 14, NX = 16, NY = 15
→ Số khối của X, Y, Z lần lượt là 30, 29, 28
Nguyên tố R có 3 đồng vị là X, Y, Z. Tổng số hạt cơ bản của ba đồng vị là 129. Số notron của X nhiều hơn của Y là 1. Đồng vị Z có số proton bằng số notron. Xác định số hiệu nguyên tử của nguyên tố R
A. 11
B. 12
C. 14
D. 16
Trong tự nhiên, nguyên tố R có 2 đồng vị bền. Tổng số các hạt p, n và e trong đồng vị thứ nhất là 60, ít hơn tổng số hạt p, n và e trong đồng vị thứ hai là 2 hạt. Biết rằng các loại hạt trong đồng vị thứ nhất bằng nhau và nguyên tử khối trung bình của nguyên tố R là 40,08. Tính % khối lượng của đồng vị thứ nhất trong hợp chất RSO4?
Số nguyên tố X trong thiên nhiên gồm 2 loại đồng vị. Hạt nhân nguyên tử R gồm có 17 proton. Đồng vị 1 có 20 notron. Đồng vị 2 ít hơn đồng vị 1 hai notron. Biết số nguyên tử của đồng vị 1 và 2 có tỉ lệ là 1 : 3. Khối lượng nguyên tử trung bình của X là:
A. 35,06 B. 35,6 C. 35,5 D. 36,5
Các hạt X, Y, Z có thành phần cấu tạo như sau:
Phát biểu nào sau đây là đúng?
A. X và Y cùng một nguyên tố hóa học
B. X và Y có cùng số khối
C. X và Z có cùng số khối
D. X và Z cùng một nguyên tố hóa học
Cho nguyên tử X ,ở trạng thái cơ bản 17 electron thuộc các phân lớp P.X có đồng vị hơn kém nhau hai notron .trong đồng vị số khối ,số hạt mang điện bằng số hạt ko mang điện . Xác định số e trong X Số e lớp ngoài cùng của X X có tính kim loại hay phi kim
Nguyên tố R có 2 đồng vị X và Y. Tổng số các loại hạt trong đồng vị Y là 54. Ở trạng thái cơ bản R có 1 e độc thân. Đòng vị X hơn đồng vị Y là 2 n
Theo đề ta có:
\(2P+N_Y=54\)
Mà \(1.5\ge\frac{N}{P}\ge1\)\(\Leftrightarrow\frac{54}{3}\ge P\ge\frac{54}{3.5}\)
\(\Rightarrow P=\left\{16;17;18\right\}\)
Mặt khác ở trạng thái cơ bản R có 1 e độc thân tức : R là Cl
một nguyên tử nguyên tố R có tổng số hạt là 92. Biết rằng số hạt không mang điện nhiều hơn số hạt mang điện 5 hạt. Hỏi: a. viết kí hiệu nguyên tử R b. biết nguyên tố R có 2 đồng vị. tìm đồng vị còn lại của R biết nó chiểm 27% và nguyên tử khối trung bình của R là 63,54
Đề này thiếu rồi em, hơn 5 hạt là trong hạt nhân hay hơn hạt mang điện dương?điện âm?
Nguyên tố R có hai đồng vị X và Y, trong đó X chiếm 75% số nguyên tử. Nguyên tử X có 29 proton và 34 nơtron, hạt nhân nguyên tử Y nhiều hơn X 2 nơtron. Tính nguyên tử khối của R
% số nguyên tử của Y là 100% - 75% = 25%
Số khối của X = 29 + 34 = 63
Số hạt notron của Y là 34 + 2 = 36
Số khối của Y là 29 + 36 = 65
Suy ra: NTK của R = $63.75\% + 65.25\% = 63,5(đvC)$