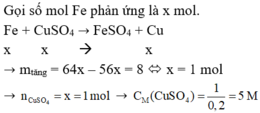Ngâm lá nhôm 13,5g vào 200ml dd gồm CuSO4 0,1M và FeSO4 đến pư kết thúc thấy mAl=17,4g. Tính nồng độ 2 muối ban đâuf

Những câu hỏi liên quan
Nhúng 1 lá nhôm vào dd 200ml CuSO4 . Sau một thời gian lấy lá nhôm ra khỏi dd làm khô rồi cân thì thấy khối lượng lá nhôm tăng 1,38g
a) Tính khối lượng đồng tạo thành
b) Tính nồng độ mol CuSO4 đã phản ứng
\(a,\) Đặt \(n_{CuSO_4}=x(mol)\)
\(PTHH:2Al+3CuSO_4\to Al_2(SO_4)_3+3Cu\\ \dfrac{2}{3}x.....x......\dfrac{1}{3}x.....x(mol)\\ \Rightarrow \Delta m_{Al\uparrow}=m_{Cu}-m_{Al}=64x-\dfrac{2}{3}.27x=1,38\\ \Rightarrow x=0,03\\ \Rightarrow m_{Cu}=0,03.64=1,92(g)\\ b,n_{CuSO_4}=0,03(mol)\\ \Rightarrow C_{M_{CuSO_4}}=\dfrac{0,03}{0,2}=0,15M\)
Đúng 0
Bình luận (0)
Gọi khối lượng Al ban đầu là a gam
khối lượng Al pư là x gam
PTHH: 2Al+3CuSO4→Al2(SO4)3+3Cu
a, vì khối lượng của nhôm sau pư tăng 1,38g, nên ta có PT:
(a-x) + 192x/54 = a + 1,38
⇒ x= 0,54
⇒ a= 0,54 + 1,38 = 1,92g
b, nAl=0,54/27 = 0,02 mol
theo PTHH có nCuSO4=2/3 .nAl = 0,03 mol
⇒CMCuSO4=0,03/0,2=0,15M
Chúc bạn học tốt nha!
Đúng 0
Bình luận (0)
Bt2. Hòa tan 6,45 g hh bột X gồm Al và Mg vào 200ml dd chứa CuSO4 1M và FeSO4 1M. Sau khi các phản ứng xảy ra hoàn toàn thu đc dd Y gồm ba muối và m gam chất rắn Z. Cho Y tác dụng với lượng dư dd Ba(OH)2, sau khi kết thúc các pư thu đc 105,75 gam chất kết tủa . a. Tính phần trăm khối lượng mỗi kl trong Xb. Tính m
Đọc tiếp
Bt2. Hòa tan 6,45 g hh bột X gồm Al và Mg vào 200ml dd chứa CuSO4 1M và FeSO4 1M. Sau khi các phản ứng xảy ra hoàn toàn thu đc dd Y gồm ba muối và m gam chất rắn Z. Cho Y tác dụng với lượng dư dd Ba(OH)2, sau khi kết thúc các pư thu đc 105,75 gam chất kết tủa .
a. Tính phần trăm khối lượng mỗi kl trong X
b. Tính m
Nhúng một lá nhôm vào 200ml dung dịch
C
u
S
O
4
, đến khi dung dịch mất màu xanh, lấy lá nhôm ra cân thấy nặng hơn so với ban đầu là 1,38 gam. Nồng độ của dung dịch
C
u
S
O
4
đã dùng là: A. 0,05 M B. 0,15 M C.0,2 M D. 0,25 M
Đọc tiếp
Nhúng một lá nhôm vào 200ml dung dịch C u S O 4 , đến khi dung dịch mất màu xanh, lấy lá nhôm ra cân thấy nặng hơn so với ban đầu là 1,38 gam. Nồng độ của dung dịch C u S O 4 đã dùng là:
A. 0,05 M
B. 0,15 M
C.0,2 M
D. 0,25 M
2 A l + 3 C u S O 4 → A l 2 S O 4 3 + 3 C u
2x……3x…….x…3x (Mol)
Theo bài ta có:
m C u b á m v à o - m A l tan = m A l t ă n g
⇔ 3x.64 -2x.27 = 1,38 ⇔ 138x = 1,38
⇔ x = 0,01 mol
⇒ n C u S O 4 = 3x = 3.0,01 = 0,03 mol
⇒ C M C u S O 4 = 0,03/0,2 = 0,15 mol
⇒ Chọn B.
Đúng 0
Bình luận (0)
Bài 1: Nhúng một lá nhôm vào 200ml dung dịch CuSO4, đến khi dung dịch mất màu xanh, lấy lá nhôm ra cân thấy nặng hơn so với ban đầu là 1,38 gam. Nồng độ của dung dịch CuSO4 đã dùng là?
2x……3x…….x…3x (Mol)
Theo bài ta có:
⇔ 3x.64 -2x.27 = 1,38 ⇔ 138x = 1,38
⇔ x = 0,01 mol
⇒ = 3x = 3.0,01 = 0,03 mol
⇒ = 0,03/0,2 = 0,15 mol
Đúng 2
Bình luận (0)
Ngâm đinh sắt sạch trong 200 ml dd CuSO4. Sau phản ứng kết thúc lấy đinh sắt ra rửa nhẹ và làm khô thấy khối lượng đinh sắt tăng 8 gam. Nồng độ CuSO4 ban đầu là: A. 0,52 M B. 0,5 M C. 5 M D. 0,25 M
Đọc tiếp
Ngâm đinh sắt sạch trong 200 ml dd CuSO4. Sau phản ứng kết thúc lấy đinh sắt ra rửa nhẹ và làm khô thấy khối lượng đinh sắt tăng 8 gam. Nồng độ CuSO4 ban đầu là:
A. 0,52 M
B. 0,5 M
C. 5 M
D. 0,25 M
Hoà tan hoàn toàn 11,2g bột sắt vào một lượng vừa đủ dd CuSO4 có nồng độ 0,1M
a. Tính thể tích dd CuSO4
b. Nếu cho 11,2g bột sắt vào 2,5 lít dd CuSO4 có nồng độ 0,1M. Xác định nồng độ mol các chất có trong dd sau có phản ứng kết thúc. (Giả thiết rằng thể tích của dd sau phản ứng thấy đổi không đáng kể)
Xem chi tiết
a)
\(Fe + CuSO_4 \to FeSO_4 + Cu\)
Theo PTHH :
\(n_{CuSO_4} = n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)\\ \Rightarrow V_{dd\ CuSO_4} = \dfrac{0,2}{0,1} = 2(lít)\)
b)
\(n_{CuSO_4} = 0,1.2,5 = 0,25(mol) > n_{Fe}= 0,2\) nên \(CuSO_4\) dư.
Ta có :
\(n_{CuSO_4\ pư} = n_{FeSO_4} = n_{Fe} = 0,2(mol)\\ \Rightarrow n_{CuSO_4\ dư} = 0,25 - 0,2 = 0,05(mol)\)
Vậy :
\(C_{M_{CuSO_4}} = \dfrac{0,05}{2,5} = 0,02M\\ C_{M_{FeSO_4}} = \dfrac{0,2}{2,5} = 0,08M\)
Đúng 1
Bình luận (0)
Ngâm 1 lá nhôm vào 200g dung dịch H2SO4 loãng nồng độ a%.Đến khi lá nhôm không còn tan được nữa,người ta thu được dung dịch muối nồng độ 10%.Tính a?
Xem chi tiết
PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
2x 3x x 3x (mol)
Ta có: \(m_{ddsaup/ứ}=m_{Al}+m_{ddH_2SO_4}-m_{H_2}=54x+200-6x\left(g\right)\)
Dung dịch muối có nồng độ 10%
\(\Rightarrow\dfrac{342x}{54x+200-6x}=0,1\) \(\Rightarrow x=\dfrac{50}{843}\left(mol\right)\)
\(\Rightarrow C\%_{H_2SO_4}=a\%=\dfrac{\dfrac{50}{243}\cdot98}{200}\cdot100\%\approx10,08\%\)
Đúng 2
Bình luận (0)
Cho a(g) kim loại Zn vào 200ml dung dịch CuCl2 2M, sau khi pư kết thúc thu được dung dịch muối kẽm clorua và kim loại đồnga) Viết PTHH của pưb) Tính a
c) Lấy toàn bộ lượng kim loại đồng sinh ra ở pư trên cho vào 100g dd H2SO4 đặc , nóng có nồng độ 98% .Tính nồng độ phần trăm các chất có trong dung dịch sau khi pư kết thúc
a) PTHH: \(Zn+CuCl_2\rightarrow ZnCl_2+Cu\)
b) Ta có: \(n_{CuCl_2}=0,2\cdot2=0,4\left(mol\right)=n_{Zn}\) \(\Rightarrow m_{Zn}=0,4\cdot65=26\left(g\right)\)
c) PTHH: \(Cu+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}CuSO_4+SO_2\uparrow+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Cu}=n_{Zn}=0,4mol\\n_{H_2SO_4}=\dfrac{100\cdot98\%}{98}=1\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,4}{1}< \dfrac{1}{2}\) \(\Rightarrow\) H2SO4 còn dư, Cu phản ứng hết
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2SO_4\left(dư\right)}=0,2mol\\n_{CuSO_4}=n_{SO_2}=n_{Cu}=0,4mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{H_2SO_4\left(dư\right)}=0,2\cdot98=19,6\left(g\right)\\m_{CuSO_4}=0,4\cdot160=64\left(g\right)\\m_{SO_2}=0,4\cdot64=25,6\left(g\right)\\m_{Cu}=0,4\cdot64=25,6\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd\left(saup/ứ\right)}=m_{Cu}+m_{ddH_2SO_4}-m_{SO_2}=100\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{CuSO_4}=\dfrac{64}{100}\cdot100\%=64\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{19,6}{100}\cdot100\%=19,6\%\end{matrix}\right.\)
Đúng 1
Bình luận (2)
Ngâm 1 lá nhôm vào 200g dung dịch H2SO4 loãng nồng độ a%.Đến khi lá nhôm không còn tan được nữa,người ta thu được dung dịch muối nồng độ 10%.Tính a?