1,Cho hai dung dịch Ba(OH)2 có nồng độ 2M và 4M. Hãy xác định thể tích của từng dung dịch để pha chế được 300ml Ba(OH)2 có nồng độ 3M.

Những câu hỏi liên quan
Cho hai dung dịch Ba(OH)2 có nồng độ 2M và 4M. Hãy xác định thể tích của từng dung dịch để pha chế được 300ml Ba(OH)2 có nồng độ 3M.
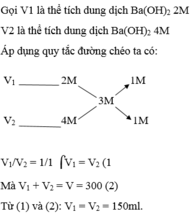
Áp dụng sơ đồ đường chéo:
\(\dfrac{V_{Ba\left(OH\right)_2\left(2M\right)}}{V_{Ba\left(OH\right)_2\left(4M\right)}}=\dfrac{4-3}{3-2}=\dfrac{1}{1}\)
=> \(V_{Ba\left(OH\right)_2\left(2M\right)}=V_{Ba\left(OH\right)_2\left(4M\right)}=\dfrac{300}{2}=150\left(ml\right)\)
Đúng 3
Bình luận (0)
II-Tự luận
Cho hai dung dịch B a ( O H ) 2 có nồng độ 2M và 4M. Hãy xác định thể tích của từng dung dịch để pha chế được 300ml B a ( O H ) 2 có nồng độ 3M.
Cho hai dung dịch Ba(OH)2 có nồng độ 2M và 4M. Hãy xác định thể tích của từng dung dịch để pha chế được 300ml Ba(OH)2 có nồng độ 3M.
Gọi thể tích dung dịch Ba(OH)2 nồng độ 2M là V (ml)
ð Thể tích dung dịch Ba(OH)2 nồng độ 4M là 300- V
Theo quy tắc đường chéo ta có:
\(\Rightarrow\frac{V}{300-V}=\frac{1}{1}\)
=>V = 150ml
Vậy thể tích dung dịch Ba(OH)2 nồng độ 2M là 150 (ml)
Thể tích dung dịch Ba(OH)2 nồng độ 4M là 300
Đúng 0
Bình luận (0)
Ta có
n\(_{BaOH}=\)0,3.3=0,9(mol)
=> V\(_{Ba\left(OH\right)2\left(2M\right)}=\frac{0,9}{2}=0,45\left(l\right)\)
V\(_{Ba\left(OH\right)2\left(3m\right)}=\frac{0,9}{4}=0,225\left(l\right)\)
chúc bạn học tốt
Đúng 0
Bình luận (0)
Câu 1. Có 2 dung dịch HCl có nồng độ 2M và 12M tính thể tích dung dịch cần lấy để pha chế được 400ml dung dịch HCl có nồng độ 10M
Câu 2. Trộn 600ml dung dịch KOH 2M và 400ml dung dịch KOH 3M. Hãy tính nồng độ mol của dung dịch này
Cho 200ml dung dịch Ba(OH)2 0,5M tác dụng với 300ml dung dịch H2SO4 0,4M. a. Viết phương trình hóa học xảy ra. b. Tính nồng độ mol và nồng độ phần trăm của dung dịch thu được sau phản ứng. Giả sử khối lượng riêng của hai dung dịch Ba(OH)2 và H2SO4 lần lượt bằng 2,3g/cm3 và 1,6g/cm3.
\(n_{Ba\left(OH\right)_2}=0,5.0,2=0,1\left(mol\right);n_{H_2SO_4}=0,3.0,4=0,12\left(mol\right)\)
PTHH: Ba(OH)2 + H2SO4 → BaSO4↓ + 2H2O
Mol: 0,1 0,1 0,1
Ta có: \(\dfrac{0,1}{1}< \dfrac{0,12}{1}\) ⇒ Ba(OH)2 hết, H2SO4 dư
\(C_{M_{H_2SO_4dư}}=\dfrac{0,12-0,1}{0,2+0,3}=0,04M\)
mdd sau pứ = 200.2,3+300.1,6-0,1.233 = 916,7 (g)
\(C\%_{H_2SO_4dư}=\dfrac{0,02.98.100\%}{916,7}=0,21\%\)
Đúng 0
Bình luận (0)
Cần dùng bao nhiêu gam Ba(OH)2 nguyên chất để pha vào 800g dung dịch Ba(OH)2 5% thu được dung dịch Ba(OH)2 có nồng độ 12%
Gọi: mBa(OH)2 thêm vào = a (g)
Ta có: \(m_{Ba\left(OH\right)_2\left(bđ\right)}=800.5\%=40\left(g\right)\)
\(\Rightarrow\dfrac{a+40}{a+800}=0,12\)
\(\Rightarrow a\approx63,64\left(g\right)\)
Đúng 1
Bình luận (0)
Có 190 ml đ chứa đồng thời KOH và Ba(OH)2 có nồng độ 3M và 4M . Tính thể tích dung dich chứa đồng thời HCl 1.98M và H2SO41.1M đủ để trung hòa lượng dung dịch trên. Tính m kết tủa
Ta có : \(n_{OH}=2C_{MBa\left(OH\right)2}V+C_{MKOH}V=2,09\left(mol\right)\)
\(BTNT\left(O\right):n_{H2O}=n_{OH}=2,09\left(mol\right)\)
\(BTNT\left(H\right):n_H=n_{H2O}=2,09\left(mol\right)\)
Mà \(n_H=2,09=1,98V+2,2V=4,18V\)
\(\Rightarrow V=0,5\left(l\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Ba\left(OH\right)2}=0,76\\n_{H2SO4}=0,55\end{matrix}\right.\) ( mol )
\(PTHH:H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2H_2O\)
Thấy ; \(0,55< 0,76\)
\(\Rightarrow n_{BaSO4}=0,55\left(mol\right)\)
\(\Rightarrow m_{kt}=128,15g\)
Đúng 1
Bình luận (0)
Pha loãng 200ml dung dịch Ba(OH)2 bằng 1,3 lít nước thu được dung dịch có pH13. Tính nồng độ mol ban đầu của dung dịch Ba(OH)2? A. 0,375M B. 0,325M C. 0,300M D. 0,425M
Đọc tiếp
Pha loãng 200ml dung dịch Ba(OH)2 bằng 1,3 lít nước thu được dung dịch có pH=13. Tính nồng độ mol ban đầu của dung dịch Ba(OH)2?
A. 0,375M
B. 0,325M
C. 0,300M
D. 0,425M
Đáp án A
Gọi nồng độ ban đầu của Ba(OH)2 là xM
nOH-= 0,2.2x = 0,4 x mol; [OH-] = 10-14/10-13 = 10-1M
[OH-] = 0,4x/ 1,5 = 10-1 suy ra x = 0,375 M
Đúng 0
Bình luận (0)
hoà tan 40g so3 vào 1l dung dịch h2so4 4,5% (d=1,099g/ml) thu được dung dịch a trộn dung dịch a với dung dịch h2so4 nồng độ 2M thu được dung dịch b dùng 100mldung dịch b tác dụng với dung dịch ba(oh)2 dư cho ra 32,62g kết tủa xác định tỉ lệ pha trộn giữa 2 dung dịch biết rằng so3 với dung dịch h2so4 và sự pha trộn không làm thay đổi thể tích dung dịch