Dẫn luồng khi hidro 28g hỗn hợp gồm Fe2O3 và CuO nung nóng để phản ứng hoàn toàn thu đc 9,6g kim loại đồng
a, Tính khối lượng từng oxit ban đầu
(Giúp mình vs )
Cho luồng khí CO dư đi qua 36,4g hỗn hợp Al2O3 và Fe2O3 nung nóng sau phản ứng để nguội cân lại thấy khối lượng hỗn hợp còn lại 86,813% so với ban đầu (phản ứng xảy ra hoàn toàn)
a) Phương trình phản ứng và tính khối lượng kim loại thu được
\(Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe + 3CO_2\)
Gọi \(n_{Fe_2O_3\ pư} = a(mol)\)
Theo PTHH : \(n_{Fe} = 2n_{Fe_2O_3} = 2a(mol)\)
Ta có :
\(m_{hỗn\ hợp} = m_{Al_2O_3} + 160a(gam)\)
\(m_{rắn\ sau\ phản\ ứng} = m_{Al_2O_3} + m_{Fe} = m_{Al_2O_3} + 112a(gam)\)
Ta có :
\(m_{giảm} = 160a - 112a = 36,4(100\% - 86,813\%)\)
Suy ra : a = 0,1
Vậy : \(m_{Fe} = 0,1.2.56 = 11,2(gam)\)
Al2O3+3CO→2Al+3CO2
Fe2O3+3CO→2Fe+3CO2
m kim loại=36,4x86,813%=31,6 g
Dẫn luồng khí CO dư đi qua 2,4 gam hỗn hợp CuO và Fe2O3 nung nóng đến phản ứng xảy ra hoàn toàn, thu được 1,76 gam chất rắn. Phần trăm khối lượng CuO có trong hỗn hợp ban đầu là ?
A. 45,72%.
B. 55,28%.
C. 66,67%.
D. 33,33%.
Đáp án D
Gọi nCuO = x ; nFe2O3 = y
=> Sau phản ứng : nCu = x ; nFe = 2y
=> mhh đầu = 80x + 160y = 2,4 và mhh sau = 64x + 112y = 1,76
=> x = y = 0,01 mol
=> %mCuO(hh đầu) = 33,33%
=>D
Dẫn luồng khí CO dư đi qua 2,4 gam hỗn hợp CuO và Fe2O3 nung nóng đến phản ứng xảy ra hoàn toàn, thu được 1,76 gam chất rắn. Phần trăm khối lượng CuO có trong hỗn hợp ban đầu là:
A. 45,72%.
B. 55,28%.
C. 66,67%.
D. 33,33%.
Dẫn luồng khí CO dư đi qua 2,4 gam hỗn hợp CuO và Fe2O3 nung nóng đến phản ứng xảy ra hoàn toàn, thu được 1,76 gam chất rắn. Phần trăm khối lượng CuO có trong hỗn hợp ban đầu là:
A. 45,72%
B. 55,28%
C. 66,67%
D.33,33%
Bài 3: Dẫn hidro đi qua 36g hỗn hợp gồm CuO và Fe2O3 nung nóng thu được hỗn hợp kim loại có khối lượng đồng gấp 4 lần khối lượng của sắt.
a) Tính khối lượng mỗi chất trong hh ban đầu. b) Thể tích hidro đã pư.
c) Khối lượng dd HCl 10,95% đủ để pư với lượng kim loại tạo ra ở trên.
Bài 4: Cho 1,95g kẽm tác dụng vừa đủ với 120g dd axit clohiđric, ta thu được dd A và khí B .
a) Viết phương trình phản ứng ? Tính thể tích khí B sinh ra ( đktc)
b) Tính nồng độ phần trăm của dung dịch axit clohidric và dd A thu được sau phản ứng ?
Bài 3 :
\(a) n_{CuO} = a(mol) ; n_{Fe_2O_3} = b(mol)\\ \Rightarrow 80a + 160b = 36(1)\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + H_2O\\ n_{Cu} = n_{CuO} = a(mol)\\ n_{Fe} = 2n_{Fe_2O_3} = 2b(mol)\\ \Rightarrow 64a = 4.2b.56(2)\\ (1)(2) \Rightarrow a = 0,35 ; b = 0,05\\ m_{CuO} = 0,35.80 = 28(gam)\\ m_{Fe_2O_3} = 0,05.160 = 8(gam)\\ b) n_{H_2} = a + 3b = 0,5(mol) \Rightarrow V_{H_2} = 0,5.22,4 = 11,2(lít)\)
\(c) Fe + 2HCl \to FeCl_2 + H_2\\ n_{HCl} = 2n_{Fe} = 0,1.2 = 0,2(mol)\\ \Rightarrow m_{dd\ HCl} = \dfrac{0,2.36,5}{10,95\%} = 66,67(gam)\)
Bài 4 :
\(a) Zn + 2HCl \to ZnCl_2 + H_2\\ n_{H_2} = n_{Zn} = \dfrac{1,95}{65} = 0,03(mol)\\ V_{H_2} = 0,03.22,4= 0,672(lít)\\ b) n_{HCl} =2 n_{H_2} = 0,06(mol)\\ \Rightarrow C\%_{HCl} = \dfrac{0,06.36,5}{120}.100\% = 1,825\%\\ m_{dd\ sau\ pư} = 1,95 + 120 - 0,03.2 = 121,89(gam)\\ \Rightarrow C\%_{ZnCl_2} = \dfrac{0,03.136}{121,89}.100\% = 3,35\%\)
Dẫn luồng khí H 2 dư đi qua 16 g hỗn hợp hai oxit CuO và F e 2 O 3 . nung nóng. Sau phản ứng để nguội, cân lại thấy khối lượng hỗnn hợp giảm 25%. Tính phần trăm khối lượng của mỗi oxit trong hỗn hợp ban đầu.
Phương trình hóa học:
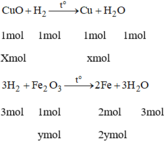
Gọi x là số mol của CuO
y là số mol của F e 2 O 3 .
Ta có: 80x + 160y = 16 (1)
Khối lượng hỗn hợp giảm do oxit tạo thành kim loại:
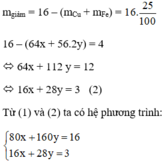
Giải hệ phương trình ta được:
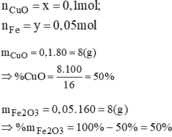
Cho bột than dư vào hỗn hợp 2 oxit Fe2O3 và CuO đun nóng để phản ứng hoàn toàn, thu được 4 gam hỗn hợp kim loại và 1,68 lít khí (đktc). Khối lượng hỗn hợp hai oxit ban đầu là
A. 5 g
B. 5,1 g
C. 5,2 g
D. 5,3 g
Cho 9,6g hỗn hợp A gồm Mg và Fe tác dungkk vừa đủ với 2,8 lít khí õi. Sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp gồm 2 oxit là MgO và Fe3O4.
a. Tính khối lượng của từng kim loại trong hỗn hợp ban đầu
b. Tính khối lượng của hỗ hợp oxit thu được
\(a) n_{Mg} = a(mol) ; n_{Fe} = b(mol)\\ \Rightarrow 24a + 56b = 9,6(1)\\ 2Mg + O_2 \xrightarrow{t^o} 2MgO\\ 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ n_{O_2} = 0,5a + \dfrac{2}{3}b = \dfrac{2,8}{22,4} = 0,125(2)\\ (1)(2)\Rightarrow a = 0,05 ; b = 0,15\\ m_{Mg} = 0,05.24 = 1,2(gam) ; m_{Fe} = 0,15.56 = 8,4(gam)\\ b) m_{oxit} = m_A + m_{O_2} = 9,6 + 0,125.32 = 13,6(gam)\)
Một hỗn hợp A gồm các oxit MgO, CuO, Fe2O3. Fe có khối lượng bằng m. Dẫn luồng khí CO dư đi qua A nung nóng đến khi phản ứng xảy ra hoàn toàn thu được chất rắn B có khối lượng là 6,8g và hỗn hợp khí C. Cho C vào dung dịch Ca(OH)2 dư thì xảy ra phản ứng. Sau phản ứng thu được 20 gam kết tủa. Tìm m
\(Ca(OH)_2 + CO_2 \to CaCO_3 + H_2O\\ n_{CO_2} = n_{CaCO_3} = \dfrac{20}{100} = 0,2(mol)\\ CO + O_{oxit} \to CO_2\\ n_{O(oxit)} = n_{CO_2} = 0,2(mol)\\ \Rightarrow m = m_B + m_{O(pư)} = 6,8 + 0,2.16 = 10(gam)\)