Câu 9: Hoàn tan 7,02g muối clorua của kim loại hóa trị I vào dd AgNO3 dư thu được dd muối nitrat và 17,22g kết tủa bạc clorua. Xác định kim loại hóa trị I và CTHH của muối, tên gọi?

Những câu hỏi liên quan
Hòa tan 3,33g muối clorua kim loại M có hóa trị II bằng dung dịch AgNO3 vừa đủ sau phản ứng hoàn toàn thu được dung dịch A và ết tủa B.Lọc bỏ hết kết tủa,cô cạn dung dịch thu được một lượng muối có khối lượng khác khối lượng muối clorua ban đầu là 1,59g.Xác định CT của muối clorua kim loại M
PTHH: MCl2 + 2AgNO3 → M(NO3)2 + 2AgCl ↓
Theo pt: Số mol MCl2 = Số mol M(NO3)2
Mà: Khối lượng mol của MCl2 < Khối lượng mol của M(NO3)2 => Khối lượng muối M(NO3)2 hơn khối lượng muối ban đầu là 1,59(gam).
Khối lượng muối M(NO3)2 sau phản ứng là:
3,33 + 1,59 = 4,92 (gam)
Số mol MCl2 tính theo khối lượng là:
3,33 / MM + 71
Số mol M(NO3)2 tính theo khối lượng là:
4,92 / MM + 124
Mà: Số mol của 2 muối là bằng nhau
=> 3,33 / MM + 71 = 4,92 / MM + 124
=> MM = 40 ( Canxi )
=> Công thức hoá học của muối Clorua kim loại M là: CaCl2
Đúng 0
Bình luận (0)
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nướ...
Đọc tiếp
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nước ở điều kiện thường ,muối clorua của M tan hoàn toàn trong nước,kim loại M hoạt động hóa học hơn Cu.
a)Viết các pthh và xác định kim loại M
b)Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp Q
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nướ...
Đọc tiếp
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nước ở điều kiện thường ,muối clorua của M tan hoàn toàn trong nước,kim loại M hoạt động hóa học hơn Cu.
a)Viết các pthh và xác định kim loại M
b)Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp Q
Khi lấy 14,25g muối clorua của một kim loại chỉ có hóa trị II và một lượng muối nitrat của kim loại đó có số mol bằng số mol muối clorua thì thấy khác nhau 7,95g . Xác định tên kim loại
Gọi kim loại cần tìm là M, có hóa trị là n
Công thức muối clorua là MCln
Công thức muối nitrat là M(NO3)n. Có số mol là x
Theo bài ra ta có hệ phương trình :
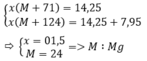
Đúng 0
Bình luận (0)
Khi lấy 14,25g muối clorua của một kim loại chỉ có hóa trị II và một lượng muối nitrat của kim loại đó có số mol bằng số mol muối clorua thì thấy khác nhau 7,95g . Xác định tên kim loại.
Gọi số mol của muối MCl2 là x, ta có:
(M + 124).x – (M + 71).x = 7,95
⇒ x = 0,15
MMCl2= \(\dfrac{14,25}{0,15}\) = 95 (g/mol)
⇒ MM = 95 – 71 = 24 (g/mol)
Kim loại M là Mg.
Vậy hai muối là MgCl2 và Mg(NO3)2.
Đúng 0
Bình luận (0)
thêm dd KOH dư vào 27g muối clorua của kim loại A (hóa trị 2 k đổi) rồi lọc kết tủa đem nung được oxit . Dẫn luồng h2 dư đi quâ lượng oxit trên thu được 12,8 kim loại . xác đinh A
Cho 416g dd bacl2 12% tác dụng vừa đủ với dd chứa 27,36g muối sunfat kim loại A.Sau khi lọc bỏ kết tủa thu được 800ml dd 0,2M của muối clorua kim loại A.Tìm hóa trị A, tên A , công thức sunfat
ta có mBaCl2=49,92g=>nBaCl2=0,24mol
n AClx=0.2*0.8=0.16mol
pt: xBaCl2 + A2(SO4)x->xBaSO4 + 2 AClx
mol 0.24 0.08 0.16
=>0.24*2=0.16x=>x=3=> A có hóa tri 3
=>M A2(SO4)3=27.36/0.08=342=>A=27
=>A là nhôm (Al) và công thức của muối là Al2(SO4)3
Đúng 0
Bình luận (0)
Hòa tan hết 2,019g hỗn hợp gồm muối clorua của kim loại A chỉ có hóa trị 1, muối clorua cảu kim loại B chỉ cso hóa trị 2 trong mọi hợp chất vào nước được dung dịch X. cho 50ml dung dịch AgNO3 1M vào dung dịch X, sau khi xảy ra phản ứng hoàn toàn thu được 5,74g kết tủa. lọc kết tủa, cô cạn dung dịch nước lọc thu được a g muối khan,a/ Tìm ab/ xác định KL A,B biết rằng MBMA+1
Đọc tiếp
Hòa tan hết 2,019g hỗn hợp gồm muối clorua của kim loại A chỉ có hóa trị 1, muối clorua cảu kim loại B chỉ cso hóa trị 2 trong mọi hợp chất vào nước được dung dịch X. cho 50ml dung dịch AgNO3 1M vào dung dịch X, sau khi xảy ra phản ứng hoàn toàn thu được 5,74g kết tủa. lọc kết tủa, cô cạn dung dịch nước lọc thu được a g muối khan,
a/ Tìm a
b/ xác định KL A,B biết rằng MB=MA+1
Jòa tan hoàn toàn 12,6g muối carbonate kim loại hóa trị II (RCO3) bằng 150 ml dd HCl (d=1,08g/ml), sau phản ứng thu được ddA và 3,7185 lít khí (đkc).
a. Xác định kim loại R.
b. Tính nồng độ phần trăm muối trong dd A.
c. Cho dd AgNO3 dư vào dd A thu được 53,8125 g kết tủa. Tính nồng độ mol/lít của dd HCl đem dùng.
\(m_{dd.HCl}=1,08.150=162\left(g\right)\)
\(n_{CO_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
\(RCO_3+2HCl\rightarrow RCl_2+H_2O+CO_2\)
0,15<----------------0,15<-----------0,15
Có: \(R+60=\dfrac{12,6}{0,15}\Rightarrow R=24\left(g/mol\right)\)
a. Kim loại R là Magie (Mg)
b. \(C\%_{MgCl_2}=\dfrac{0,15.95.100\%}{12,6+162-0,15.44}=8,48\%\)
c. \(n_{AgCl}=\dfrac{53,8125}{143,5}=0,375\left(mol\right)\)
\(MgCl_2+2AgNO_3\rightarrow2AgCl+Mg\left(NO_3\right)_2\)
0,15-------------------->0,3
Vì \(n_{AgCl}=0,3\left(mol\right)< 0,375\left(mol\right)_{theo.đề}\) \(\Rightarrow\) HCl dư
\(HCl+AgNO_3\rightarrow AgCl+HNO_3\)
0,075<------------0,075
\(CM_{HCl.đem.dùng}=\dfrac{0,075}{0,15}=0,5M\)
Đúng 1
Bình luận (0)


















