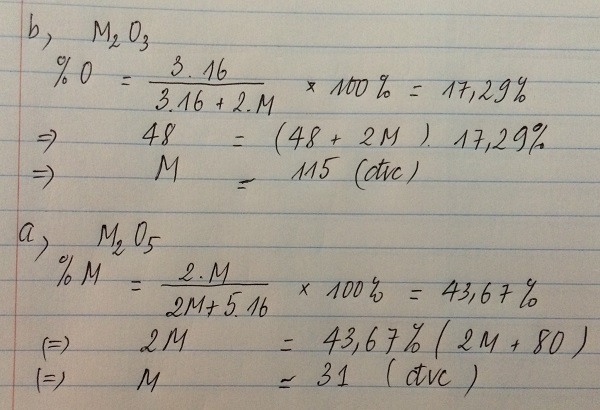Một oxit hóa trị III chứa 30% oxi. Tìm CTHH của oxit

Những câu hỏi liên quan
Bài 1: oxit của một nguyên tố hóa trị V chứa 25,9% nguyên tố đó. Xác định CTHH của oxit?a) Oxit của một nguyên tố hóa trị III chứa 23,08%O. Xác định CTHH của oxit đó?b) Oxit của một nguyên tố hóa trị IV chứa 53,33% khối lượng ôxi. Xác định CTHH của oxit?c) Trong hợp chất của nguyên tố A hóa trị III với H chứa 17,65% khối lượng H. Xác định A và CT hợp chất.d) Trong hợp chất của nguyên tố B hóa trị II với H chứa 94,12% khối lượng B. Xác định A và CT hợp chất.(mọi người ơi mình cần gấp)
Đọc tiếp
Bài 1: oxit của một nguyên tố hóa trị V chứa 25,9% nguyên tố đó. Xác định CTHH của oxit?
a) Oxit của một nguyên tố hóa trị III chứa 23,08%O. Xác định CTHH của oxit đó?
b) Oxit của một nguyên tố hóa trị IV chứa 53,33% khối lượng ôxi. Xác định CTHH của oxit?
c) Trong hợp chất của nguyên tố A hóa trị III với H chứa 17,65% khối lượng H. Xác định A và CT hợp chất.
d) Trong hợp chất của nguyên tố B hóa trị II với H chứa 94,12% khối lượng B. Xác định A và CT hợp chất.(mọi người ơi mình cần gấp)
Oxi hóa hết 22,4 g kim loại A (hóa trị III) thu đc 32g Oxit kim loại.Lập CTHH của oxit kim loại đó
\(4A+3O_2\rightarrow\left(t^o\right)2A_2O_3\\ m_{O_2}=32-22,4=9,6\left(g\right)\\ \Rightarrow n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\\ \Rightarrow n_A=\dfrac{4}{3}.0,3=0,4\left(mol\right)\\ \Rightarrow M_A=\dfrac{22,4}{0,4}=56\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Sắt\left(Fe=56\right)\)
Đúng 6
Bình luận (0)
-PTHH:\(4A+3O_2\rightarrow^{t^0}2A_2O_3\).
-Theo định luật bảo toàn khối lượng, ta có:
\(m_A+m_{O_2}=m_{A_2O_3}\)
\(\Rightarrow m_{O_2}=m_{A_2O_3}-m_A=32-22,4=9,6\left(g\right)\)
\(\Rightarrow n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\).
-Theo PTHH ở trên, ta có:
\(n_{A_2O_3}=\dfrac{0,3}{3}.2=0,2\left(mol\right)\)
\(\Rightarrow M_{A_2O_3}=\dfrac{m}{n}=\dfrac{32}{0,2}=160\) (g/mol).
\(\Rightarrow2.M_A+3.16=160\)
\(\Rightarrow M_A=\dfrac{160-3.16}{2}=56\) (g/mol).
\(\Rightarrow A\) là Fe (Iron).
Đúng 1
Bình luận (0)
Oxit của kim loại hóa trị III có chứa 70% oxi về khối lượng tìm công thức hóa học của oxit nói trên
Sửa đề : 70% kim loại
\(CT:A_2O_3\)
\(\%A=\dfrac{2A}{2A+16\cdot3}\cdot100\%=70\%\)
\(\Leftrightarrow A=56\)
\(CT:Fe_2O_3\)
Đúng 6
Bình luận (0)
Gọi CTHH của oxit là M2O3
Ta có %mM = 70%
=> \(\dfrac{2.M_M}{2.M_M+3.16}.100\%=70\%\Rightarrow M_M=56\left(Fe\right)\)
Vậy cthh của oxit là Fe2O3
Bài này phải là 30% oxi về khối lượng thì đúng hơn
Đúng 2
Bình luận (0)
Một oxit của một nguyên tố Y ( Y có hóa trị III ) chứa 30% nguyên tố oxi. Xác định nguyên tử khối của nguyên tố Y.
gọi công thức oxit là Y2O3 ta có:
%O=30%
=> M Y2O3=\(\frac{16.3}{30}.100=160\)g/mol
=> M Y2=160-16.3=112
=>My=112:2=56
vậy nguyên tử khối của Y là 56
Đúng 0
Bình luận (1)
a. Oxit của một nguyên tố hóa trị V chứa 43,67% nguyên tố đó. Xác định CTHH
b. Oxit của một nguyên tố hóa trị III chứa 17,29% O . Xác địnhCTHH
c. Oxit của một nguyên tố hóa trị IV chứa 13,4% khối lượng oxi. Xác định CTHH
Làm lại nhé
Câu a: Gọi công thức oxit là A2O5 (Kí hiệu A trùng với nguyên tử khối ở dưới nhé)
Theo đề ra ta có:
\(\frac{2.A}{2.A+16.5}=\frac{43,67}{100}\). Giải phương trình ta được A = 31
=> CTHH là \(P_2O_5\)
Ủng hộ mình nha
Đúng 0
Bình luận (0)
a) Gọi A là nguyên tố hóa trị V
CTTQ: A2O5
Ta có: %(m)O = 100 - 43,67 = 56,33 (%)
Ta lại có: \(\frac{m_A}{m_O}=\frac{\%m_A}{\%m_O}\) ⇔ \(\frac{2A}{5.16}\) = \(\frac{43,67}{56,33}\)
⇔ 2A = \(\frac{80.43,67}{56,33}\) \(\approx\) 62 ⇒ A = 31 (đvC)
Vậy nguyên tố A là Photpho (P)
CTHH: P2O5
b) Gọi B là nguyên tố hóa trị III
CTTQ: B2O3
Ta có: %(m)B = 100 - 17,29 = 82,71 (%)
Ta lại có: \(\frac{m_B}{m_O}\) = \(\frac{\%m_B}{\%m_O}\) ⇔ \(\frac{2B}{48}\) = \(\frac{82,71}{17,29}\)
⇔ 2B = \(\frac{48.82,71}{17,29}\) \(\approx\) 230 ⇒ B = 115 (đvC)
Vậy B là nguyên tố Indium (Indi)
CTHH: Indi2O3
Continute
Chúc bạn học tốt!!!
Vậy nguyên tố A là Photpho (P)
Đúng 0
Bình luận (0)
Oxit của một nguyên tố hóa trị III chứa 0% oxi về khối lượng. Công thức hóa học của oxit đó là :A. Cl2O3B. Fe2O3C. Cr2O3D. Al2O3
Xem chi tiết
Sửa đề : chứa 30% oxi về khối lượng :
Oxit : \(R_2O_3\)
\(\%O = \dfrac{16.3}{2R + 16.3}.100\% = 30\%\\ \Rightarrow R = 56(Fe)\)
Vậy Oxit cần tìm : Fe2O3
Đáp án : B
Đúng 3
Bình luận (3)
Oxit của một nguyên tố hóa trị III có chưa 47,06% khối lượng oxi.
a) Tìm CTHH của oxit đã cho.
b) Viết PTHH tạo ra oxit từ các đơn chất.
\(a,CTTQ:A_2O_3\\ Ta.c\text{ó}:\dfrac{M_A.2}{M_O.3}=\dfrac{100\%-47,06\%}{47,06\%}\\ \Leftrightarrow94,12\%M_A=158,82\%.16\\ \Leftrightarrow M_A\approx27\left(\dfrac{g}{mol}\right)\\ \Rightarrow CTHH:Al_2O_3\\ b,4Al+3O_2\rightarrow\left(t^o\right)Al_2O_3\)
Đúng 5
Bình luận (0)
a,CTTQ:A2O3
Ta.có:MA.2MO.3=100%−47,06%47,06%⇔94,12%MA=158,82%.16⇔MA≈27(gmol)⇒CTHH:Al2O3b,4Al+3O2→(to)Al2O3 . Mình ko ghi đc dấu gạch
Đúng 0
Bình luận (1)
Một oxit của kim lạo có hóa trị III trong đó oxit chiếm 31.578%
a/ Xác định CTHH của oxit trên
b/ Tính thể tích H2 ( ĐKTC) cần dùng để điều chế 20.8 kim loại trong oxit trên
c/ Tính khối lượng của oxit kim loại đem dùng . Biết trong oxit này có chứa 5% tạp chất
a, Gọi CTHH: AxIIIOyII ⇒ A2O3 (Theo quy tắc hóa trị)
Ta có: %O = \(\dfrac{16.2}{16.2+2Ma}\).100%=31,578%
⇒ 0,31517(2MA + 48) =48 ⇒ 0,63156MA = 32,84256
⇒ MA ≈ 52 (Cr) (Cr có hóa trị III)
⇒ CT Oxit là: Cr2O3
Đúng 0
Bình luận (0)
b, nCr = 20,8/52 = 0,4 mol
PTPƯ: Cr2O3 + 3H2 ---> 2Cr + 3H2O
Ta có: 0,4 mol Cr ----> 0,6 mol H2
⇒ VH2 = 0,6 . 22,4 = 13,44 (l)
Vậy ...
Đúng 0
Bình luận (0)
c, M oxit đem dùng là: 95/100 . 152 =144,4 (g) (Trừ 5% tạp chất)
(Nếu dùng dữ kiện câu b, )
mCr2O3 = 152 . 0,2 = 30,4 (g)
M oxit đem dùng là: 95/100 . 30,4 = 28,88 (g)
Vậy ...
Đúng 0
Bình luận (0)
Oxit có của 1 nguyên tố có hóa trị III chứa 43,66% oxi về khối lượng. Xđ CTHH của oxit đó
CTHH: \(X_2O_3\)
Ta có: \(\frac{2.M_X}{3.M_O}=\frac{56,34\%}{43,66\%}\)
=> \(\frac{2.M_X}{48}=\frac{2817}{2183}\)
=> \(M_X=31\) (g/mol)
=> X là P (photpho)
=> CTHH: P2O3