nguyên tử của kim loại M có số proton ít hơn số nơtron là 1 và số hạt mang điện nhiều hơn số hạt không mang điện là 10. xác định số khối của M

Những câu hỏi liên quan
Bài 8. Nguyên tử của kim loại M có số proton ít hơn số nơtron là 1 và số hạt mang điện nhiều hơn
số hạt không mang điện là 10. Xác định Z, A, viết kí hiệu nguyên tử M
Ta có: \(\left\{{}\begin{matrix}n-p=1\\n=10\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=9\\n=10\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=z=9\\n=10\end{matrix}\right.\)
\(\Rightarrow A=z+n=9+10=19\left(u\right)\)
\(KHNT:^{19}_9F\)
Đúng 0
Bình luận (0)
Nguyên tử M có số nơtron nhiều hơn số proton là 1 và số hạt mang điện nhiều hơn số hạt không mang điện là 10.
a) Xác định số proton trong hạt nhân (điện tích hạt nhân) của M.
b) Biết proton và nơtron có cùng khối lượng và bằng 1đvC. Tính khối lượng nguyên tử của X.
c) Vẽ sơ đồ đơn giản của nguyên tử nguyên tố M. X là nguyên tố nào? Kí hiệu hoá học của M.
Nguyên tử M có số notron nhiều hơn số proton là 1 => nM - pM = 1 => - pM+nM=1 (1) Số hạt ko mang điện nhiều hơn số hạt mang điện là 10 => 2pM-nM = 10 (2) Giai (!) (2) suy ra : pM=3 (Li) X là Li. Bài dễ mà bạn :P chi tiết rồi đó
Đúng 0
Bình luận (0)
Nguyên tử M có số nơtron nhiều hơn số proton là 1 và số hạt mang điện nhiều hơn số hạt không mang điện là 10. Xác định cấu tạo nguyên tử , và xác định M là nguyên tố nào?
Gọi số proton , notron , electron của nguyên tử M lần lượt là p , n , e ( p,n,e ϵ N*)
Ta có :
n - p = 1 => n = p+1 (*)
Do trong nguyên tử M số hạt mang điện lớn hơn số hạt không mang điện là 10 hạt
=> (p+e) - n = 10
=> 2p - n = 10 (vì nguyên tử trung hòa về điện)
kết hợp (*) ta được
2p - (p+1) = 10
=> 2p - p - 1 =10
=> p = 11
=> e = 11 (hạt)
=> M là nguyên tố Natri
Đúng 3
Bình luận (1)
Nguyên tử M có số nơtron nhiều hơn số proton là 1 và số hạt mang điện nhiều hơn số hạt không mang điện là 10. Xác định cấu tạo nguyên tử
Ta có:
\(\left\{{}\begin{matrix}p=e\\n-p=1\\p+e-n=10\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}n-p=1\\2p-n=10\end{matrix}\right.\\ \Rightarrow p=e=11;n=12\)
Vậy M là Na
Cấu tạo ngtử:
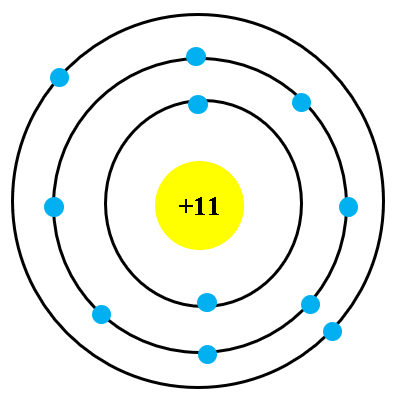
Đúng 2
Bình luận (0)
Ta có số proton=số electron
Ta có số nơtron nhiều hơn số proton là 1, ta có
2n-2p=2(1)
Ta có số hạt mang điện nhiều hơn số hạt không mang điện, ta có
2p-n=10 (2)
(1)+(2)= 2n-2p+2p-n=n=12
=>p=11
Vậy M là nguyên tố Boron(B)
Đúng 1
Bình luận (0)
Bài 6. Tổng số hạt proton, nơtron, electron trong hai nguyên tử kim loại A và B là 142, trong đó tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 42. Số hạt mang điện của nguyên tử B nhiều hơn của A là 12. Xác định hai kim loại A, B.
Giải:
p1 + n1 + e1 + p2 + n2 + e2 = 142
Mà ( p = e )
<=> 2p1 + 2p2 + n1 + n2 = 142 (1)
Mặt khác:
2p1 + 2p2 - n1 + n2 = 142
Cộng (1) và (2)
=> 4p1 + 4p2 = 184 (3)
Mà: 2p2 - 2p1 = 12
<=> -2p1 + 2p2 = 12 (4)
Giải (3) và (4):
p1 = 20 ( Ca )
p2 = 26 ( Fe )
ĐÁNH GIÁ CHO MÌNH NHÉ
Đúng 0
Bình luận (0)
Tổng số hạt proton, nơtron, electron trong 2 nguyên tử kim loại X và Y là 142, trong đó tổng số hạt mang điện nhiều hơn tổng sô hạt không mang điện là 42. Số hạt mang điện của nguyên tử Y nhiều hơn của X là 12.Xác định hai kim loại X và Y.
Kí hiệu : P X , P Y và N X , N Y lần lượt là số proton và số nơtron của nguyên tử X và Y.
Theo đề bài ta lập được hệ phương trình đại số :
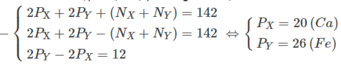
Đúng 1
Bình luận (1)
: Tổng số hạt proton, nơtron, electron trong 2 nguyên tử kim loại M và X là 94, trong đó tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 30. Số hạt mang điện của nguyên tử X nhiều hơn của M là 18. Hai kim loại M và X lần lượt là :
2pM + nM + 2pX + nX = 94
2pM + 2pX - nM - nX = 30
2pX - 2pM = 18
=> \(\left\{{}\begin{matrix}p_M=11\\p_X=20\end{matrix}\right.\)
=> M, X lần lượt là Na, Ca
Đúng 2
Bình luận (0)
Nguyên tử M có số nơtron nhiều hơn số proton là 1 và số hạt mang điện nhiều hơn số hạt không mang điện là 10. Hãy xác định số hạt mỗi loại ?
trình bày bài giải rõ dàng hộ mk nhé!!
vì nguyên tử M có số notron nhiều hơn số proton là 1
=> n= p+1 (1)
vì số hạt mang điện nhiều hơn số hạt không mang điện là 10
=> p+e=n+10
=> 2p = n+10 (vì số p = số e) (2)
thay (1) vào (2) ta được : 2p = p +1+10
=> 2p-p =11
=> p=11
mà p =e => e=11
lại có n=p+1=> n =11+1=12
Vậy nguyên tử M có 11 hạt proton ,11 hạt electron và 12 hạt notron
Đúng 0
Bình luận (0)
Theo đề bài ta có
n=p+1 (1)
P+e=n+10 hay 2p=n+10 (2)
Từ 1 và 2
Suy ra 2p=p+1+10
Suy ra 2p-p=11
Vậy p=11
Đúng 0
Bình luận (0)
nguyên tử m có số nơtron nhiều hơn số proton là 1 và số hạt mang điện nhiều hơn số hạt không mang điện là 10 hãy xác định m là nguyên tố nào
hóa lớp 8 đó
Số notron nhiều hơn số proton là 1: N - P = 1 (1)
Số hạt mang điện nhiều hơn số hạt không mang điện là 10: 2P - N = 10 (2)
Giải hệ (1) và (2): P = 11 và N = 12
Đó là nguyên tố Na.
Đúng 0
Bình luận (4)
gọi số notron là x
số proton,electron là y (số proton=số electron)
theo bài ra:
x-y=1
2y=x+10
=>y=11
<=>số electron = 11
=> m là Natri
Đúng 0
Bình luận (0)
Số notron nhiều hơn số proton là 1: N - P = 1 (1)
Số hạt mang điện nhiều hơn số hạt không mang điện là 10: 2P - N = 10 (2)
Giải hệ (1) và (2): P = 11 và N = 12
Đó là nguyên tố Na.
Đúng 0
Bình luận (0)
Xem thêm câu trả lời




























