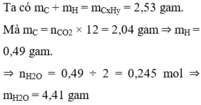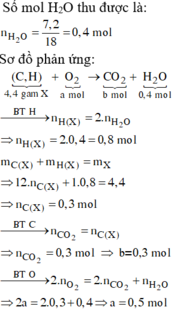Đốt cháy hết 1,6 gam CH4 trong bình chứa 9,6 gam oxi thu được 4,4 gam CO2 và m gam H2O giá trị của m là

Những câu hỏi liên quan
Đốt cháy hoàn toàn 1,6 gam CH4 trong khí oxi dư, sau phản ứng thu được V lít khí CO2 và m gam H2O. Giá trị của V và m lần lượt là
\(n_{CH_4}=\dfrac{1,6}{16}=0,1\left(mol\right)\)
PTHH: \(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
0,1--->0,2----->0,1---->0,2
\(\Rightarrow\left\{{}\begin{matrix}V=V_{CO_2}=0,1.22,4=2,24\left(l\right)\\m=m_{H_2O}=0,2.18=3,6\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn m (g) gồm CH4 ; C3H6 ; C4H10 thu được 4,4 gam CO2 và 2,52 gam H2O. Giá trị của m là?
Ta có: \(n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{2,52}{18}=0,14\left(mol\right)\Rightarrow n_H=0,14.2=0,28\left(mol\right)\)
\(\Rightarrow m=m_C+m_H=0,1.12+0,28.1=1,48\left(g\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
1.Đốt cháy hết m gam chất A cần dùng 3,36 lít oxi ở đktc, thu được 4,4 gam CO2 và 1,8 gam H2O. Giá trị đúng của m là bao nhiêu?
2.Cho 1,2 gam magie tác dụng với dung dịch axit sunfuric H2SO4 loãng, dư. Thể tích khí hiđro (đktc) thu được là bao nhiêu?
1) \(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo ĐLBTKL: m = 4,4 + 1,8 - 0,15.32 = 1,4 (g)
2)
\(n_{Mg}=\dfrac{1,2}{24}=0,05\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,05------------------------->0,05
=> VH2 = 0,05.22,4 = 1,12 (l)
Đúng 4
Bình luận (0)
mO2 = ( 3,36 : 22,4 ) . 32 = 4,8 (g)
ADDLBTKL ta co :
mA + mO2 = mCO2 + mH2O
=> mA = mCO2 + mH2O - mO2
= 4,4 + 1,8 - 4,8 = 1,4 (g)
=> m= 1,4 (g)
2
nMg = 1,2 : 24 = 0,05 (mol)
pthh : Mg +H2SO4 ---> MgSO4 + H2
0,05--------------------------->0,05(mol)
=> VH2 = 0,05 .22,4 = 1,12 (l)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 2,53 gam hỗn hợp
CH
4
,
C
2
H
6
và
C
4
H
10
thu được 7,48 gam
CO
2
và m gam
H
2
O...
Đọc tiếp
Đốt cháy hoàn toàn 2,53 gam hỗn hợp CH 4 , C 2 H 6 và C 4 H 10 thu được 7,48 gam CO 2 và m gam H 2 O . Giá trị của m là
A. 4,08.
B. 4,05.
C. 4,59.
D. 4,41.
Đốt cháy hoàn toàn 2,53 gam hỗn hợp CH4, C2H6 và C4H10 thu được 7,48 gam CO2 và m gam H2O. Giá trị của m là
A. 4,08.
B. 4,05.
C. 4,59.
D. 4,41.
Đáp án D
Ta có mC + mH = mCxHy = 2,53 gam.
Mà mC = nCO2 × 12 = 2,04 gam ⇒ mH = 0,49 gam.
⇒ nH2O = 0,49 ÷ 2 = 0,245 mol ⇒ mH2O = 4,41 gam
Đúng 0
Bình luận (0)
Đốt cháy 4,4 gam hỗn hợp
CH
4
,
C
2
H
4
,
C
3
H
6
,
C
4
H
10...
Đọc tiếp
Đốt cháy 4,4 gam hỗn hợp CH 4 , C 2 H 4 , C 3 H 6 , C 4 H 10 cần a mol O 2 thu được b mol CO 2 và 7,2 gam H 2 O . Giá trị a, b lần lượt là
A. 0,5 và 0,3
B. 0,6 và 0,3
C. 0,5 và 0,8
D. 0,5 và 0,4
Đáp án là A
Quy hỗn hợp ban đầu thành nguyên tố C và H
![]()
(bảo toàn nguyên tố H)
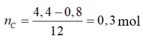
![]()
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn một lượng methane CH4 cần 6,4 gam O2 thu được H2O và 4,4 gam CO2. Khối lượng nguyên tố oxygen O có trong chất nước H2O ở sản phẫm là:
a) 1,6 gam
b) 1,8 gam
c) 3,2 gam
d) 2 gam
Đốt cháy hoàn toàn hỗn hợp gồm CH4, C3H8 , C4H10 , C3H4 Cần m gam khí oxi, thu được 13,2 g CO2 và 4,32 g H2O . Giá trị của m là
\(n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)\)
=> nC = 0,3 (mol)
\(n_{H_2O}=\dfrac{4,32}{18}=0,24\left(mol\right)\)
=> nH = 0,48 (mol)
m = mC + mH = 0,3.12 + 0,48.1 = 4,08 (g)
Đúng 2
Bình luận (0)
Đốt cháy 4,4 gam hỗn hợp X gồm CH4, C2H4, C3H6, C4H10 cần a mol O2 thu được b mol CO2 và 7,2 gam H2O. Giá trị a, b lần lượt là: A.0,5 và 0,3. B.0,6 và 0,3. C.0,5 và 0,8. D.0,5 và 0,4.
Đọc tiếp
Đốt cháy 4,4 gam hỗn hợp X gồm CH4, C2H4, C3H6, C4H10 cần a mol O2 thu được b mol CO2 và 7,2 gam H2O. Giá trị a, b lần lượt là:
A.0,5 và 0,3.
B.0,6 và 0,3.
C.0,5 và 0,8.
D.0,5 và 0,4.