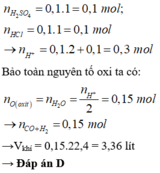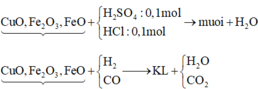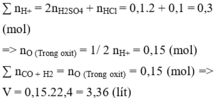Câu 1 : Dùng khí H2 để khử 40g CuO thu được 16g Cu .Tính thể tích H2 cần dùng ở ĐKTC ? Câu 2:Cho m gam kim loại Fe tác dụng với dung dịch H2SO4 loãng có chứa 12,25g H2SO4 tạo ra khí hidro và 15,2g sắt II sunfat FeSO4 .Tính M?

Những câu hỏi liên quan
Cho 5,6g Fe tác dụng với dung dịch H2SO4 tạo ra muối Fe(SO4) và khí H2 a) tính thể tích h2 sinh ra (ở đktc) b) tính khối lượng muối thu được c) dùng toàn bộ khí sinh ra tác dụng với 12g CuO.tính khối lượng kim loại sinh ra * em cần gấp ạ 12h em đi thi r
Số mol của 5,6 g Fe:
\(n_{Fe}=\dfrac{m}{M}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
1 :1 : 1 : 1
0,1-> 0,1 : 0,1 : 0,1(mol)
a) thể tích của 0,1 mol H2:
\(V_{H_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
b) khối lượng 0,1 mol FeSO4:
\(m_{FeSO_4}=n.M=0,1.152=15,2\left(g\right)\)
c) PTHH: \(H_2+CuO\underrightarrow{t^o}Cu+H_2O\)
1 : 1 : 1 : 1
0,1 -> 0,1 : 0,1 : 0,1(mol)
khối lượng 0,1 mol Cu:
\(m_{Cu}=n.M=0,1.64=6,4\left(g\right)\)
Đúng 2
Bình luận (0)
a) Ta sử dụng định luật Avogadro để tính thể tích H2 sinh ra:
1 mol khí ở đktc có thể tích là 22,4 LTính số mol H2 sinh ra:Fe + H2SO4 → FeSO4 + H2
Fe + H2SO4 → FeSO4 + H2
Số mol H2 = số mol Fe = m/FeMM = 5,6/56 = 0,1 molThể tích H2 ở đktc = số mol H2 x 22,4 L/mol = 0,1 x 22,4 = 2,24 L
Vậy thể tích H2 sinh ra là 2,24 L (ở đktc).
b) Tính khối lượng muối thu được:
Viết phương trình phản ứng:Fe + H2SO4 → FeSO4 + H2Tính số mol FeSO4 thu được:
Fe : FeSO4 = 1 : 1
n(FeSO4) = n(Fe) = 0,1 molTính khối lượng muối thu được:
m(FeSO4) = n(FeSO4) x M(FeSO4) = 0,1 x (56 + 32x4) = 27,2 g
Vậy khối lượng muối thu được là 27,2 g.
c) Dùng toàn bộ H2 sinh ra tác dụng với CuO, ta có phương trình phản ứng:
CuO + H2 → Cu + H2O
n(CuO) = m/M = 12/64 = 0,1875 molTính số mol H2 cần dùng:
Theo phương trình phản ứng ta biết: 1 mol CuO cần 1 mol H2
n(H2) = n(CuO) = 0,1875 molTính khối lượng Cu sinh ra:
Theo phương trình phản ứng ta biết: 1 mol Cu cần 1 mol H2
m(Cu) = n(Cu) x M(Cu) = 0,1875 x 63,5 = 11,90625 g
Vậy khối lượng kim loại Cu sinh ra là 11,90625 g.
Đúng 0
Bình luận (0)
\(a)n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ Fe+H_2SO_4\xrightarrow[]{}FeSO_4+H_2\\ \Rightarrow n_{Fe}=n_{H_2}=n_{FeSO_4}=0,1mol\\ V_{H_2}=0,1.22,4=2,24\left(l\right)\\ b)m_{FeSO_4}=0,1.152=15,2\left(g\right)\\ c)n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\\ CuO+H_2\xrightarrow[]{t^0}Cu+H_2\)
Theo pt: \(\dfrac{0,15}{1}>\dfrac{0,1}{1}\Rightarrow Cu\) \(dư\)
\(CuO+H_2\xrightarrow[]{t^0}Cu+H_2O\\ \Rightarrow n_{H_2}=n_{Cu}=0,1mol\\ m_{Cu}=0,1.64=6,4\left(g\right)\)
Đúng 0
Bình luận (0)
Câu 6: Cho 13g Kẽm tác dụng hoàn toàn với dung dịch axit clohidric
a/ Tính thể tích khí H2 sinh ra (ở đktc)? b/ Tính khối lượng ZnCl2 thu được?
c/ Dùng toàn bộ khí H2 ở trên để khử Sắt (III) oxit. Tính số gam sắt thu được?
Zn+2Hcl->ZnCl2+H2
0,2---0,4----0,2----0,2
n Zn=0,2 mol
=>VH2 =0,2.22,4=4,48l
mZncl2=0,2.136=27,2g
3H2+Fe2O3-to>2Fe+3H2O
0,2---------------------2\15
->m Fe=2\15.56=7,467g
Đúng 1
Bình luận (0)
nZn= 13/65=0,2(mol)
a) PTHH: Zn + 2 HCl -> ZnCl2 + H2
b) nH2=nZnCl2=nZn=0,2(mol)
=>V(H2,đktc)=0,2 x 22,4= 4,48(l)
c) khối lượng muối sau phản ứng chứ nhỉ?
mZnCl2=136.0,2=27,2(g)
Khử 0,8g đồng (II) oxit bằng khí hiđro. (Cho Cu = 64; H = 1; O = 16; Cl = 35,5).Hãy: a/Tính số gam đồng kim loại thu được? b/Tính thể tích khí hiđro (đktc) cần dùng? c/Để có lượng H2 đó phải lấy bao nhiêu gam Fe cho tác dụng vừa đủ với bao nhiêu gam dd axit HCl 20
`n_[CuO]=[0,8]/80=0,01(mol)`
`H_2 + CuO` $\xrightarrow{t^o}$ `Cu + H_2 O`
`0,01` `0,01` `0,01` `(mol)`
`a)m_[Cu]=0,01.64=0,64(g)`
`b)V_[H_2]=0,01.22,4=0,224(l)`
`c)`
`Fe + 2HCl -> FeCl_2 + H_2`
`0,01` `0,02` `0,01` `(mol)`
`@m_[Fe]=0,01.56=0,56(g)`
`@m_[dd HCl]=[0,02.36,5]/20 . 100=3,65(g)`
Đúng 4
Bình luận (0)
Cho 5,6 gam kim loại Fe tác dụng với 150 ml dung dịch HCl. Sau phản ứng thu được muối sắt (II) clorua (FeCl2) và khí H2. a. Tính nồng độ mol dung dịch HCl đã phản ứng và thể tích khí H2 (ở đktc) sau phản ứng? b. Cần dùng bao nhiêu lít dung dịch NaOH 2M để phản ứng hết với muối sắt (II) clorua (FeCl2) thu được ở trên
Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
____0,1______0,2_____0,1____0,1 (mol)
a, \(C_{M_{HCl}}=\dfrac{0,2}{0,15}=\dfrac{4}{3}\left(M\right)\)
\(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
b, \(FeCl_2+2NaOH\rightarrow2NaCl+Fe\left(OH\right)_2\)
Theo PT: \(n_{NaOH}=2n_{FeCl_2}=0,2\left(mol\right)\)
\(\Rightarrow V_{NaOH}=\dfrac{0,2}{2}=0,1\left(l\right)\)
Đúng 5
Bình luận (0)
Cho kim loại 14 gam Fe tác dụng với dung dịch axit HCl, thu được dung dịch muối FeCl2và khí H2a) Viết CTHH xảy ra.b) Tính khối lượng axit HCl đã dùng. c) Tính thể tích khí H2 sinh ra ở đktc.
Đọc tiếp
Cho kim loại 14 gam Fe tác dụng với dung dịch axit HCl, thu được dung dịch muối FeCl2và khí H2
a) Viết CTHH xảy ra.
b) Tính khối lượng axit HCl đã dùng.
c) Tính thể tích khí H2 sinh ra ở đktc.
a, PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b, Ta có: \(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Fe}=0,5\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,25.36,5=18,25\left(g\right)\)
c, Theo PT: \(n_{H_2}=n_{Fe}=0,25\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,25.22,4=5,6\left(l\right)\)
Đúng 3
Bình luận (0)
Cho 16,25 gam kim loại Zn tác dụng vừa đủ với 300 ml dung dịch H2SO4 thu được
muối kẽm sunfat (ZnSO4) và khí hiđrô (H2) .
a) Tính thể tích khí hiđro sinh ra ở đktc?
b) Tính nồng độ mol/lit của axit đã dùng?
c) Nếu lấy lượng H2 cho phản ứng với 32 gam Fe2O3 đun nóng thì thu được m ( gam) chất rắn Tính m ?
Sửa:
`Zn + H_2 SO_4 -> ZnSO_4 + H_2`
`0,25` `0,25` `0,25` `(mol)`
`n_[Zn]=[16,25]/65=0,25(mol)`
`a)V_[H_2]=0,25.22,4=5,6(l)`
`b)C_[M_[H_2 SO_4]]=[0,25]/[0,3]~~0,8(M)`
`c)`
`3H_2 + Fe_2 O_3` $\xrightarrow{t^o}$ `2Fe + 3H_2 O`
`0,25` `1/12` `1/6` `(mol)`
`n_[Fe_2 O_3]=32/160=0,2(mol)`
Ta có:`[0,25]/3 < [0,2]/1`
`=>Fe_2 O_3` dư
`=>m_[Fe]=1/6 . 56~~9,3(g)`
Đúng 0
Bình luận (0)
`Zn + H_2 SO_4 -> ZnSO_4 + H_2`
`0,25` `0,25` `0,25` `(mol)`
`n_[Zn]=[16,25]/65=0,25(mol)`
`a)V_[H_2]=0,25.22,4=5,6(l)`
`b)C_[M_[H_2 SO_4]]=[0,25]/[0,3]~~0,8(M)`
`c)`
`H_2 + 3Fe_2 O_3` $\xrightarrow{t^o}$ `2Fe_3 O_4 + H_2 O`
`1/15` `0,2` `2/15` `(mol)`
`n_[Fe_2 O_3]=32/160=0,2(mol)`
Ta có:`[0,25]/1 > [0,2]/3`
`=>H_2` dư
`=>m_[Fe_3 O_4]=2/15 . 232~~30,93(g)`
Đúng 0
Bình luận (7)
Cho m gam hỗn hợp X gồm CuO, Fe2O3, FeO tác dụng vừa đủ với 100 ml dung dịch chứa H2SO4 1M và HCl 1M. Thể tích (ở đktc) hỗn hợp khí CO và H2 tối thiểu cần dùng để khử hoàn toàn m gam hỗn hợp X là A. 1,12 lít B. 6,72 lít C. 4,48 lít D. 3,36 lít
Đọc tiếp
Cho m gam hỗn hợp X gồm CuO, Fe2O3, FeO tác dụng vừa đủ với 100 ml dung dịch chứa H2SO4 1M và HCl 1M. Thể tích (ở đktc) hỗn hợp khí CO và H2 tối thiểu cần dùng để khử hoàn toàn m gam hỗn hợp X là
A. 1,12 lít
B. 6,72 lít
C. 4,48 lít
D. 3,36 lít
Cho m gam hỗn hợp X gồm CuO,
Fe
2
O
3
, FeO tác dụng vừa đủ với 100ml dung dịch chứa
H
2
SO
4
1M và HCl 1M. Thể tích (ở đktc) hỗn hợp khí CO và
H
2
tối thiểu cần dùng để khử hoàn toàn m gam hỗn hợp X là A. 3,36 lít. B. 6,72 lít...
Đọc tiếp
Cho m gam hỗn hợp X gồm CuO, Fe 2 O 3 , FeO tác dụng vừa đủ với 100ml dung dịch chứa H 2 SO 4 1M và HCl 1M. Thể tích (ở đktc) hỗn hợp khí CO và H 2 tối thiểu cần dùng để khử hoàn toàn m gam hỗn hợp X là
A. 3,36 lít.
B. 6,72 lít.
C. 1,12 lít.
D. 4,48 lít.
Cho m gam hỗn hợp X gồm CuO, Fe2O3, FeO tác dụng vừa đủ với 100 ml dung dịch chứa H2SO4 1M và HCl 1M. Thể tích (ở đktc) hỗn hợp khí CO và H2 tối thiểu cần dùng để khử hoàn toàn m gam hỗn hợp X là A. 1,12 lít. B. 6,72 lít. C. 4,48 lít. D. 3,36 lít.
Đọc tiếp
Cho m gam hỗn hợp X gồm CuO, Fe2O3, FeO tác dụng vừa đủ với 100 ml dung dịch chứa H2SO4 1M và HCl 1M. Thể tích (ở đktc) hỗn hợp khí CO và H2 tối thiểu cần dùng để khử hoàn toàn m gam hỗn hợp X là
A. 1,12 lít.
B. 6,72 lít.
C. 4,48 lít.
D. 3,36 lít.