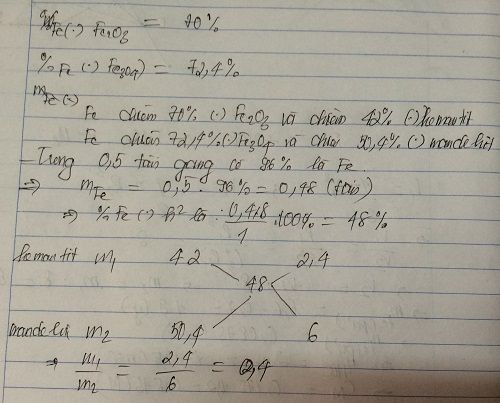1. Tính khối lượng sắt có trong:
a. 100 tấn quăng hematit chứa 60% Fe2O3
b. 100 tấn quặng manhetit chứa 69,6% Fe3O4
2. Cần trộn 2 loại quặng trên theo tỉ lệ nào để từ 1 tấn quặng đã trộn người ta điều chế được 0,5 tấn gang( chứa 96% sắt và 4% cacbon)?