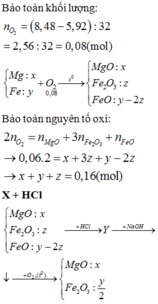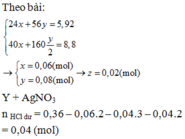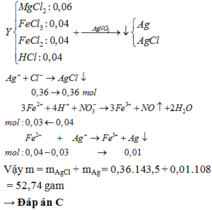Đốt cháy hoàn toàn 2,46 gam hỗn hợp lim loại X gồm al, Mg, Fe thì cần 896 ml khí O2, thu được m gam hỗn hợp Y gồm oxit. Hòa tan m gam Y thì cần 50 gam dung dịch HCl. Viết các pthh và tính nồng độ % đung dịch HCl. Tính giá trị m

Những câu hỏi liên quan
Nung 16 gam hỗn hợp X gồm Al, Mg, Zn, Cu trong bình đựng oxi dư thu được m gam hỗn hợp các oxit Y. Hòa tan hoàn toàn m gam Y thì cần 160 ml dung dịch HCl 3,5M. Tính m.
\(n_{HCl}=0,16.3,5=0,56\left(mol\right)\)
=> \(n_{H_2O}=\dfrac{0,56}{2}=0,28\left(mol\right)\)
=> nO = 0,28 (mol)
=> m = 16 + 0,28.16 = 20,48 (g)
Đúng 1
Bình luận (0)
\(n_{HCl}=0,16.3,5=0,56\left(mol\right)\\ n_{O\left(trong.oxit\right)}=n_{H_2O}=\dfrac{n_{HCl}}{2}=\dfrac{0,56}{2}=0,28\left(mol\right)\\ m=m_{hh.oxit}=m_{hhX}+0,28.16=16+4,48=20,48\left(g\right)\)
Đúng 0
Bình luận (0)
Đốt cháy 5,92 gam hỗn hợp gồm Mg và Fe trong khí
O
2
, thu được 8,48 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong 180 mL dung dịch HCl 2M, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, lọc kết tủa và đem nung trong không khí đến khối lượng không đổi, thu được 8,8 gam chất rắn. Nếu cho dung dịch
A
g
N
O
3
dư vào Y, tạo thành m gam kết tủa. Giá trị của m là A. 51,66 B...
Đọc tiếp
Đốt cháy 5,92 gam hỗn hợp gồm Mg và Fe trong khí O 2 , thu được 8,48 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong 180 mL dung dịch HCl 2M, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, lọc kết tủa và đem nung trong không khí đến khối lượng không đổi, thu được 8,8 gam chất rắn. Nếu cho dung dịch A g N O 3 dư vào Y, tạo thành m gam kết tủa. Giá trị của m là
A. 51,66
B. 53,82
C. 52,74
D. 55,98
Hỗn hợp rắn A gồm Mg, Al và Cu. Đốt cháy m gam rắn A cần dùng 2,24 lít (đktc) hỗn hợp gồm
O
2
và
O
3
có tỉ khối so với He bằng 9,6 thu được hỗn hợp rắn B gồm các oxit. Hòa tan hoàn toàn B cần dùng 200 ml dung dịch HCl 0,6M và
H
2
SO
4
xM. Cô cạn dung dịch sau phản ứng thu được (3m+5,94) gam muối khan. Giá trị của m là A. 6,4 g...
Đọc tiếp
Hỗn hợp rắn A gồm Mg, Al và Cu. Đốt cháy m gam rắn A cần dùng 2,24 lít (đktc) hỗn hợp gồm O 2 và O 3 có tỉ khối so với He bằng 9,6 thu được hỗn hợp rắn B gồm các oxit. Hòa tan hoàn toàn B cần dùng 200 ml dung dịch HCl 0,6M và H 2 SO 4 xM. Cô cạn dung dịch sau phản ứng thu được (3m+5,94) gam muối khan. Giá trị của m là
A. 6,4 gam
B. 7,8 gam
C. 8,6 gam
D. 12,4 gam
Đốt cháy 2,86 gam hỗn hợp Al, Zn, Mg trong bình đựng khí oxi dư, thu được 4,46 gam hỗn hợp rắn X gồm các oxit. Hòa tan toàn bộ X vào 300 ml dung dịch HCl 1M, thu được dung dịch Y. Cho 300ml NaOH 1M vào, thu được m gam kết tủa.Gía trị của m là
Oxi hóa m gam hỗn hợp X gồm Cu và Fe (có tỉ lệ số mol tương ứng là 3 : 2) trong 3,92 lít hỗn hợp khí Y (đktc) gồm O2 và Cl2, thu được hỗn hợp rắn Z gồm các oxit kim loại và muối clorua. Để hòa tan hoàn toàn lượng hỗn hợp Z cần 150 ml dung dịch HCl 2M thu được dung dịch T, thêm tiếp dung dịch AgNO3 dư vào dung dịch T thì thu được 82,55 gam kết tủa. Giá trị của m là. A. 12,16 gam B. 7,6 gam C. 15,2 gam D. 18,24 gam
Đọc tiếp
Oxi hóa m gam hỗn hợp X gồm Cu và Fe (có tỉ lệ số mol tương ứng là 3 : 2) trong 3,92 lít hỗn hợp khí Y (đktc) gồm O2 và Cl2, thu được hỗn hợp rắn Z gồm các oxit kim loại và muối clorua. Để hòa tan hoàn toàn lượng hỗn hợp Z cần 150 ml dung dịch HCl 2M thu được dung dịch T, thêm tiếp dung dịch AgNO3 dư vào dung dịch T thì thu được 82,55 gam kết tủa. Giá trị của m là.
A. 12,16 gam
B. 7,6 gam
C. 15,2 gam
D. 18,24 gam
Đốt cháy 4,16 gam hỗn hợp gồm Mg và Fe trong khí O2, thu được 5,92 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong dung dịch HCl vừa đủ, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 6 gam chất rắn. Mặt khác cho Y tác dụng với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là A. 31,57. B. 32,11. C. 32,65. D. 10,80.
Đọc tiếp
Đốt cháy 4,16 gam hỗn hợp gồm Mg và Fe trong khí O2, thu được 5,92 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong dung dịch HCl vừa đủ, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 6 gam chất rắn. Mặt khác cho Y tác dụng với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là
A. 31,57.
B. 32,11.
C. 32,65.
D. 10,80.
nO/X = (5,92 – 4,16) ÷ 16 = 0,11 mol
[O] + 2HCl → 2Cl + H2O ⇒ nCl– = 2nO = 0,22 mol.
Đặt nMg = x; nFe = y ⇒ 24x + 56y = 4,16(g).
Rắn gồm x mol MgO và 0,5y mol Fe2O3
⇒ 40x + 160.0,5y = 6(g)
⇒ giải hệ có: x = 0,01 mol; y = 0,07 mol.
Bảo toàn electron cả quá trình:
2nMg + 3nFe = 2nO + nAg ⇒ nAg = 2 × 0,01 + 3 × 0,07 - 2 × 0,11 = 0,01 mol.
► Kết tủa gồm 0,01 mol Ag và 0,22 mol AgCl
⇒ m = 0,01 × 108 + 0,22 × 143,5 = 32,65(g).
Đáp án C
Đúng 0
Bình luận (0)
Đốt cháy 4,16 gam hỗn hợp gồm Mg và Fe trong khí O2, thu được 5,92 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong dung dịch HCl vừa đủ, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 6 gam chất rắn. Mặt khác cho Y tác dụng với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là A. 10,80. B. 32,11. C. 32,65. D. 31,57.
Đọc tiếp
Đốt cháy 4,16 gam hỗn hợp gồm Mg và Fe trong khí O2, thu được 5,92 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong dung dịch HCl vừa đủ, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 6 gam chất rắn. Mặt khác cho Y tác dụng với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là
A. 10,80.
B. 32,11.
C. 32,65.
D. 31,57.
Đốt cháy 4,16 gam hỗn hợp gồm Mg và Fe trong khí O2, thu được 5,92 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong dung dịch HCl vừa đủ, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 6 gam chất rắn. Mặt khác cho Y tác dụng với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là A. 31,57. B. 32,11. C. 32,65. D. 10,80.
Đọc tiếp
Đốt cháy 4,16 gam hỗn hợp gồm Mg và Fe trong khí O2, thu được 5,92 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong dung dịch HCl vừa đủ, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 6 gam chất rắn. Mặt khác cho Y tác dụng với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là
A. 31,57.
B. 32,11.
C. 32,65.
D. 10,80.
Chọn đáp án C
nO/X = (5,92 – 4,16) ÷ 16 = 0,11 mol || [O] + 2HCl → 2Cl + H2O ⇒ nCl– = 2nO = 0,22 mol.
Đặt nMg = x; nFe = y ⇒ 24x + 56y = 4,16(g). Rắn gồm x mol MgO và 0,5y mol Fe2O3
⇒ 40x + 160.0,5y = 6(g) ||⇒ giải hệ có: x = 0,01 mol; y = 0,07 mol. Bảo toàn electron cả quá trình:
2nMg + 3nFe = 2nO + nAg ⇒ nAg = 2 × 0,01 + 3 × 0,07 - 2 × 0,11 = 0,01 mol.
► Kết tủa gồm 0,01 mol Ag và 0,22 mol AgCl ⇒ m = 0,01 × 108 + 0,22 × 143,5 = 32,65(g).
Đúng 0
Bình luận (0)
Đốt cháy 16,64 gam hỗn hợp gồm Mg và Fe trong khí O2, thu được 23,68 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong dung dịch HCl vừa đủ, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 24 gam chất rắn. Mặt khác cho Y tác dụng với dungd ịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là A. 126,28 B. 128,44. C. 130,6. D. 43,20.
Đọc tiếp
Đốt cháy 16,64 gam hỗn hợp gồm Mg và Fe trong khí O2, thu được 23,68 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong dung dịch HCl vừa đủ, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 24 gam chất rắn. Mặt khác cho Y tác dụng với dungd ịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là
A. 126,28
B. 128,44.
C. 130,6.
D. 43,20.