Hòa tan hoàn toàn 25,8 gam kim loại kiềm A và oxit của nó vào nước dư thu được dung dịch B Cô cạn dung dịch B thu được 33,6 g chất rắn kha. xác định kim loại kiềm A và khối lượng mỗi chất trong hỗn hợp

Những câu hỏi liên quan
Hòa tan hoàn toàn 25,8 gam kim loại kiềm A và oxit của nó vào nước dư thu được dung dịch B. Cô cạn dung dịch B thu được 33,6 g chất rắn khan. xác định kim loại kiềm A và khối lượng mỗi chất trong hỗn hợp
Gọi kim loại cần tìm là A
Công thức oxit là A2O
Đặt \(\left\{{}\begin{matrix}n_A=x\left(mol\right)\\n_{A_2O}=y\left(mol\right)\end{matrix}\right.\)
=> \(x.M_A+y\left(2.M_A+16\right)=25,8\)
=> \(x.M_A+2y.M_A+16y=25,8\) (1)
PTHH: 2A + 2H2O --> 2AOH + H2
A2O + H2O --> 2AOH
=> \(\left(x+2y\right)\left(M_A+17\right)=33,6\)
=> \(x.M_A+2y.M_A+17x+34y=33,6\) (2)
(2) - (1) = 17x + 18y = 7,8
=> \(x=\dfrac{7,8-18y}{17}\)
Do x > 0 => \(\dfrac{7,8-18y}{17}>0\Rightarrow0< y< \dfrac{13}{30}\) (3)
Thay vào (1) => 7,8.MA + 16y.MA + 272y = 25,8
=> \(M_A=\dfrac{571,2}{7,8+16y}-17\) (4)
(3)(4) => 21,77 < MA < 56,23
=> \(A\left[{}\begin{matrix}Natri\left(Na\right)\\Kali\left(K\right)\end{matrix}\right.\)
- Nếu A là Na:
=> 23x + 62y = 25,8
Và (x + 2y).40 = 33,6
=> x = 0,03; y = 0,405
\(\left\{{}\begin{matrix}m_{Na}=0,03.23=0,69\left(g\right)\\m_{Na_2O}=0,405.62=25,11\left(g\right)\end{matrix}\right.\)
- Nếu A là K
=> 39x + 94y = 25,8
Và (x + 2y).56 = 33,6
=> x = 0,3; y = 0,15
=> \(\left\{{}\begin{matrix}m_K=0,3.39=11,7\left(g\right)\\m_{K_2O}=0,15.94=14,1\left(g\right)\end{matrix}\right.\)
Đúng 6
Bình luận (1)
hòa tan hoàn toàn 8,6 gam hỗn hợp kim loại có hóa trị I và oxit của nó vào nước được dung dịch A. Cô cạn dung dịch A và thu được 11,2 gam hidroxit khan
a) Xác định kim loại hóa trị I
b) Tính khối lượng mỗi chất trong hỗn hợp ban đầu
Hòa tan hoàn toàn 17,2g hỗn hợp kim loại kiềm A và oxit của nó (A2O) vào nước đc dd B. Cô cạn dd B thu đc 22,4g AOH khan. Xác định tên kim loại và khối lượng mỗi chất trong hỗn hợp
Công thức kim loại kiềm là A
--> công thức oxit của nó là AO(0,5)
Cứ 1 mol A, sau khi chuyển thành AOH thì khối lượng tăng lên 17 gam.
Còn cứ 1 mol AO(0,5), sau khi chuyển thành AOH thì khối lượng tăng lên là 9 gam.
Đề bài cho khối lượng AOH nặng hơn khối lượng hỗn hợp là 22,4 - 17,2 = 5,2 gam.
Nếu hỗn hợp trên chỉ là kim loại thì n A = 5,2/17 = 0,3058823 mol và MA = 17,2/0,3058823 = 56,230778.
Nếu hỗn hợp trên chỉ là oxit của A thì n AO(0,5) = 5,2/9 = 0,5777777 --> MAO(0,5) = 22,4/0,5777777 = 38,769235 --> MA = 38,769235 - 8 = 30,769235.
30,769235 < MA < 56,230778 --> A là K với M K = 39
Đúng 1
Bình luận (1)
Hòa tan hoàn toàn m gam hỗn hợp A gồm kim loại kiềm và kiềm thổ vào 400 ml dung dịch HCl 0,25M thu được 400 ml dung dịch B trong suốt có pH 13. Cô cạn dung dịch B thu được 10,07 gam chất rắn. Giá trị của m là A. 6,16 B. 5,84 C. 4,30 D. 6,45
Đọc tiếp
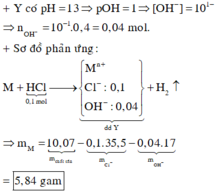
Hòa tan hoàn toàn m gam hỗn hợp A gồm kim loại kiềm và kiềm thổ vào 400 ml dung dịch HCl 0,25M thu được 400 ml dung dịch B trong suốt có pH = 13. Cô cạn dung dịch B thu được 10,07 gam chất rắn. Giá trị của m là
A. 6,16
B. 5,84
C. 4,30
D. 6,45
Đáp án : B
[OH-]B = 0,1 M => nOH(B) = 0,04 mol
=> nOH(A) = nHCl + nOH(B) = 0,14 mol
Vì kim loại chỉ có 1 hóa trị duy nhất => Trong muối clorua thì nOH(trung hòa) = nCl = 0,1 mol
=> chất rắn B gồm : mB = mKL + mOH + mCl
=> mKL = mA = 5,84g
Đúng 1
Bình luận (0)
Cho 6,06 gam hỗn hợp X gồm một kim loại kiềm M và một kim loại R có hóa trị III vào nước, thấy hỗn hợp X tan hoàn toàn tạo ra dung dịch A và 3,808 lít khí (đktc). Chia dung dịch A làm hai phần bằng nhau: – Cô cạn phần thứ nhất thu được 4,48 gam chất rắn khan. – Thêm V lít dung dịch HCl 1M vào phần thứ hai thấy xuất hiện 0,78 gam kết tủa. a. Xác định tên hai kim loại và tính thành phần % khối lượng mỗi kim loại trong X. b. Tính giá trị V.
Đọc tiếp
Cho 6,06 gam hỗn hợp X gồm một kim loại kiềm M và một kim loại R có hóa trị III vào nước, thấy hỗn hợp X tan hoàn toàn tạo ra dung dịch A và 3,808 lít khí (đktc). Chia dung dịch A làm hai phần bằng nhau:
– Cô cạn phần thứ nhất thu được 4,48 gam chất rắn khan.
– Thêm V lít dung dịch HCl 1M vào phần thứ hai thấy xuất hiện 0,78 gam kết tủa.
a. Xác định tên hai kim loại và tính thành phần % khối lượng mỗi kim loại trong X.
b. Tính giá trị V.
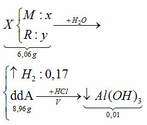
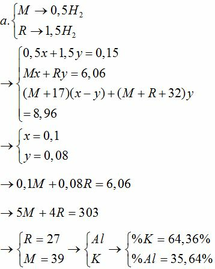
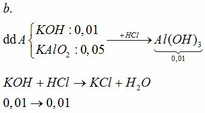
TH1: kết tủa Al(OH)3 chưa bị hòa tan
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,01 ←0,01
→ nHCl = 0,02
→ V = 0,02 (lít) = 20 (ml)
TH2: kết tủa Al(OH)3 bị hòa tan một phần
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,05 → 0,05 0,05
Al(OH)3 + 3HCl → AlCl3 + 3H2O
0,04` → 0,12
→ nHCl = 0,18 → V = 0,18 (l) = 180 (ml)
Vậy có 2 giá trị của V thỏa mãn là: 20 ml và 180 ml
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam hỗn hợp X gồm kim loại kiềm và kiềm thổ vào 400 ml dung dịch HCl 0,25M, thu được 400 ml dung dịch Y trong suốt có pH 13. Cô cạn dung dịch Y thu được 10,07 gam chất rắn. Giá trị của m là A. 6,16. B. 5,84. C. 4,30. D. 6,45.
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp X gồm kim loại kiềm và kiềm thổ vào 400 ml dung dịch HCl 0,25M, thu được 400 ml dung dịch Y trong suốt có pH = 13. Cô cạn dung dịch Y thu được 10,07 gam chất rắn. Giá trị của m là
A. 6,16.
B. 5,84.
C. 4,30.
D. 6,45.
Hoà tan hoàn toàn 17,2g hỗn hợp gồm kim loại A (I) và oxit của nó vào nước dư được dung dịch B. Cô cạn dung dịch B được 22,4g hiđroxit kim loại ( bazơ) khan. a) Tìm kim loại A và oxit tương ứng b) Thành phần % theo khối lượng mỗi chất trong hỗn hợp.
Giả sử hh chỉ có M mà KHÔNG có M2O:
M + H2O --> MOH + 0,5H2
\(\dfrac{17,2}{M}\) = \(\dfrac{22,4}{M+17}\) => M = 56,2
Giả sử hh chỉ có M2O mà không có M:
M2O + H2O ---> 2MOH
\(\dfrac{17,2}{2M+16}\)= \(\dfrac{22,4}{2.\left(M+17\right)}\) => M=21,7
Tu 1 và 2 ==> 21,7 < M < 56,2
==> M có thể là Na (23) và K (39).
TH1: M là Na. Gọi x,y là số mol Na và Na2O:
=> 23x + 62y = 17,2
40(x+2y)=22,4
=> x=0,02 và y=0,27 (nhận)
==> mNa = 0,46g ; mNa2O = 16,74g.
TH2: M là K, goi x,y là số mol K và K2O:
39x + 94y = 17,2
56(x+2y) = 22,4
=> x = 0,2 và y=0,1
==> mK = 7,8g ; mK2O = 9,4g
Vậy M có thể là Na hoặc K
Đúng 2
Bình luận (0)
Hoà tan hoàn toàn 17,2g hỗn hợp gồm kim loại A (I) và oxit của nó vào nước dư được dung dịch B. Cô cạn dung dịch B được 22,4g hiđroxit kim loại ( bazơ) khan. a) Tìm kim loại A và oxit tương ứng b) Thành phần % theo khối lượng mỗi chất trong hỗn hợp.
Gọi \(\left\{{}\begin{matrix}n_X=a\left(mol\right)\\n_{X_2O}=b\left(mol\right)\end{matrix}\right.\)
=> a.MX + 2b.MX + 16b = 17,2 (1)
PTHH: 2X + 2H2O --> 2XOH + H2
a------------------>a
X2O + H2O --> 2XOH
b--------------->2b
=> \(\left(a+2b\right)\left(M_X+17\right)=22,4\) (**)
=> a.MX + 2b.MX + 17a + 34b = 22,4 (2)
(1)(2) => 17a + 18b = 5,2
=> \(a=\dfrac{5,2-18b}{17}\) (*)
Thay (*) vào (**):
\(\left(\dfrac{5,2-18b}{17}+2b\right)\left(M_X+17\right)=22,4\)
=> \(\left(5,2+16b\right)\left(M_X+17\right)=380,8\)
Mà \(18b< 5,2\Rightarrow b< \dfrac{13}{45}\Rightarrow M_X>21,77\)
\(b>0\Rightarrow M_X< 56,23\)
=> 21,77 < MX < 56,23
Mà X là kim loại hóa trị I, tan được trong nước tạo ra dd bazo
=> \(X\left[{}\begin{matrix}Na\\K\end{matrix}\right.\)
- Nếu X là Na => oxit tương ứng là Na2O
- Nếu X là K => oxit tương ứng là K2O
b)
- Nếu X là Na:
\(\left\{{}\begin{matrix}23a+62b=17,2\\a+2b=0,56\end{matrix}\right.\)
=> a = 0,02 (mol); b = 0,27 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Na}=\dfrac{23.0,02}{17,2}.100\%=2,67\%\\\%m_{Na_2O}=\dfrac{0,27.62}{17,2}.100\%=97,33\%\end{matrix}\right.\)
- Nếu X là K
\(\left\{{}\begin{matrix}39a+94b=17,2\\a+2b=0,4\end{matrix}\right.\)
=> a = 0,2 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%m_K=\dfrac{0,2.39}{17,2}.100\%=45,35\%\\\%m_{K_2O}=\dfrac{0,1.94}{17,2}.100\%=54,65\%\end{matrix}\right.\)
Đúng 4
Bình luận (0)
Hòa tan hỗn hợp gồm 2 kim loại kiềm kế tiếp nhau vào nước được dung dịch x và 3,7285 lít khí h2 ở điều kiện chuẩn cho HCl dư vào dung dịch x và cô cạn thu được 2,075 g muối khan a) tìm tên hai kim loại kiềm b) tính khối lượng của mỗi kim loại kiềm trong hỗn hợp ban đầu
a) Sửa đề: `3,7285 -> 3,7185` và `2,075 -> 20,75`
\(n_{H_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
Đặt CT chung của 2 kim loại kiềm là R
\(2R+2H_2O\rightarrow2ROH+H_2\)
0,3<-------------0,3<-----0,15
\(ROH+HCl\rightarrow RCl+H_2O\)
0,3------------->0,3
\(\Rightarrow M_{RCl}=\dfrac{20,75}{0,3}=\dfrac{415}{6}\left(g/mol\right)\\ \Rightarrow M_R=\dfrac{415}{6}-35,5=\dfrac{101}{3}\left(g/mol\right)\)
`=>` 2 kim loại là Na và K
b) Đặt \(\left\{{}\begin{matrix}n_{Na}=a\left(mol\right)\\n_K=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}a+b=0,3\\58,5+74,5=20,75\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Na}=0,1.23=2,3\left(g\right)\\m_K=0,2.39=7,8\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)