Mọi người ơi giúp mik vs, mik cần gấp !!!
Nhiệt phân KMnO4 thu được 1,008 l khí Oxi ở đktc
a) Tìm khối lượng KMnO4 cần dùng .
b) Cho lượng khí Oxi ở trên tác ụng với 4g Canxi. Tính khối lượng sản phẩm thu được.
Cảm ơn mọi người nhé !!!
Nhiệt phân hoàn toàn 79 gam KMnO4, sau PƯ thu đc V lít khí Oxi(đktc)
a) Viết PTHH xảy ra
b) Tính V
c) Dùng lượng oxi thu đc ở trên đốt cháy 3,1 gam photpho. Tính khối lượng sp thu đc
giúp mik vs mik đag cần gấp![]() mik c.ơn trước
mik c.ơn trước
a)
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
b) $n_{KMnO_4} = \dfrac{79}{158} = 0,5(mol)$
Theo PTHH : $n_{O_2} = \dfrac{1}{2}n_{KMnO_4} = 0,25(mol)$
$\Rightarrow V_{O_2} = 0,25.22,4 = 5,6(lít)$
c) $n_P = \dfrac{3,1}{31} = 0,1(mol)$
$4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
Ta thấy : $n_P : 4 < n_{O_2} :5$ nên $O_2$ dư
$n_{P_2O_5} = \dfrac{1}{2}n_P = 0,05(mol)$
$m_{P_2O_5} = 0,05.142 = 7,1(gam)$
Nung nóng KMnO4 thu được K2MnO4+ MnO2+O2. Dùng oxi ở trên oxi hóa sắt ở nhiệt độ cao thu được Fe3O4
a) Tính lượng sắt và oxi cần dùng để điều chế 2,32g Fe3O4
b) Tính khối lượng KMnO4 cần dùng
Mọi người ơi giúp mình nha, nhớ trình bày cụ thể cho mình đó, cảm ơn rất nhiều ạ
2KMnO4 = K2MnO4+MnO2+ O2 (1)
3Fe+ 2O2=(t0)Fe3O4 (2)
nFe3O4=2,32/232=0,01 mol
nO2=2nFe3O4=0,02 mol --> mO2=0,02. 32=0,64 g
nFe= 3nFe3O4=0,03 mol --> mFe=0,03.56=1,68 g
Ta có: nO2(1)=nO2(2)= 0,02 mol --> nKMnO4=2nO2=2. 0,02=0,04 mol => mKMnO4= 0,04. 158=6,32 g
xin lỗi nhé anh nhầm bước cuôi nKMnO4=2NO2=0.04 mol
=> mKMnO4=0.04*158=6.32g
Xin lỗi nhé
a) nFe3O4= 2.32/232=0.01 mol
PTHH : 3Fe + 2O2 ---> Fe3O4
0.03 0.01
mFe=0.03*56=1.68g
Theo bảo toàn khối lượng,ta có : mFe + mO= mFe3O4
<=> 1.68 + mO = 2.32
=> mO= 2.32 - 1.68 = 0.64g
b) nO2= 0.64/32=0.02 mol
PTHH : 2KMnO4 -----> MnO2 + O2 + K2MnO4
0.01 0.02
=>mKMnO4= 0.01*158=1.58g
Chúc em học tốt!!!:))
Trong phòng thí nghiệm cần dùng 28 bình chứa khí oxi để làm thí nghiệm, mỗi bình có dung tích là 100ml. Tính khối lượng thuốc tím (KMnO4) cần dùng để khi nhiệt phân thu đc đủ lượng khí oxi trên, biết khi thu lượng khí oxi bị hao hụt mất 20%
Giúp mik vs ạ mik cám ơn trc :33
\(V_{O_2\left(thu.được\right)}=28=0,1=2,8\left(l\right)\)
=> \(V_{O_2\left(sinh.ra\right)}=\dfrac{2,8.100}{80}=3,5\left(l\right)\)
=> \(n_{O_2\left(sinh.ra\right)}=\dfrac{3,5}{22,4}=0,15625\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,3125<------------------------0,15625
=> mKMnO4 = 0,3125.158 = 49,375 (g)
đốt cháy 16g kim loại đồng trong khí oxi
a) viết phương trình phản ứng
b) tính khối lượng đồng (II) oxit tạo thành
c) tính thể tích oxi cần dùng ( đktc)
d) để có được lượng khí oxi ở trên, cần nhiệt phân bao nhiêu gam KMnO4
PTHH : 2Cu + O2 ---> 2CuO (1)
2KMnO4 ---> K2MnO4 + MnO2 + O2 (2)
Từ gt => nCu =16:64 = 0,25 (mol)
Từ (1) và gt => nCu = nCuO = 2 nO2
=> nCuO = 0,25 mol
nO2 = 0,125 mol
=> mCuO = 0,25 x 80 = 20 (g)
VO2 = 0,125 x 22,4 = 2,8 (l)
Từ (2) => nKMnO4 = 2 nO2
=> nKMnO4 = 0,25
=> mKMnO4 = 0,25 x 158 = 39,5(g)
Bài 6 PT nhiệt phân theo sơ đồ sau: Sample picture a) Tính thể tích khí oxi (đktc) thu được khi nhiệt phân 31,6 g KmnO4. b) Tính khối lượng CuO được tạo thành khi cho lượng khí oxi sinh ra ở trên tác dụng hết với Cu.
Phân hủy KMnO4,thu được K2Mn04;MnO2 và 2,24 lít khí oxi ở đktc. a)Viết phương trình hóa học xảy ra ? b)Tính khối lượng KMnO4 cần đem đi phân hủy? c)Nếu dùng hết lượng oxi trên tác dụng với thể tích của H2 là bao nhiêu lít để tạo ra hỗn hợp nổ mạnh.
nO2 = 2,24/22,4 = 0,1 (mol)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,1 . 2 = 0,2 (mol)
mKMnO4 = 0,2 . 158 = 31,6 (g(
Để tạo hh nổ mạnh nhất thì VH2 : VO2 = 2 : 1
=> VH2 = VO2 . 2 = 2,24 . 2 = 4,48 (l)
Để điều chế khí oxi trong phòng thí nghiệm người ta nhiệt phân KMnO4 ở nhiệt độ cao
a) Để thu được 22,4 lít khí oxi ở đktc thì cần dùng bao nhiêu gam KMnO4
b) Dùng lượng khí oxi trên để đốt than (thành phần chính là cacbon C). Tính lượng CO2 sinh ra ở đktc
"M.n cứu em bài này với ạ không là em sắp thi rồi ạ"
a. \(n_{O_2}=\dfrac{22.4}{22.4}=1\left(mol\right)\)
PTHH : 2KMnO4 ----to----> K2MnO4 + MnO2 + O2
2 1
\(m_{KMnO_4}=2.158=316\left(g\right)\)
b. PTHH : C + O2 ---to--->CO2
1 1 1
\(m_{CO_2}=1.44=44\left(g\right)\)
a. n O 2 = 22.4 22.4 = 1 ( m o l ) PTHH : 2KMnO4 ----to----> K2MnO4 + MnO2 + O2 2 1 m K M n O 4 = 2.158 = 316 ( g ) b. PTHH : C + O2 ---to--->CO2 1 1 1 m C O 2 = 1.44 = 44 ( g )
Nhiệt phân hoàn toàn 31,6g KMnO4 để điều chế khí oxi trong phòng thí nghiệm
a. Tính thể tích khí oxi thu được ở đktc?
b. Đốt cháy 11,2g Fe với lượng khí O2 thu được ở trên. Tính khối lượng Fe từ oxi thu được sau phản ứng
a.\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{31,6}{158}=0,2mol\)
\(PTHH:2KMnO_4\underrightarrow{np}K_2MnO_4+MnO_2+O_2\)
2 1 1 1 ( mol )
0,2 0,1
\(V_{O_2}=n.22,4=0,1.22,4=2,24l\)
b.\(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
3 2 1 ( mol )
0,2 0,1
0,1 0,1 0,05 ( mol )
\(m_{Fe_3O_4}=n.M=0,05.232=11,6g\)
Câu 3: Đốt cháy hoàn toàn 16,8 gam Sắt (Fe) trong không khí
a) Tính khối lượng sản phẩm thu được?
b) Tính thể tích khí oxi, và thể tích không.khí cần dùng ở đktc? (biết rằng oxi chiếm 20% thể tích không khí)
c) Tính khối lượng KMnO4 cần dùng để điều chế đủ oxi cho phản ứng trên? Biết rằng lượng oxi thu được hao hụt 20%
Cho biết: Fe = 56, O = 16, K = 39, Mn = 55
a.b.
\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,3 0,2 0,1 ( mol )
\(m_{Fe_3O_4}=0,1.232=23,2g\)
\(V_{O_2}=0,2.22,4=4,48l\)
\(V_{kk}=4,48.5=22,4l\)
c.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,4 0,2 ( mol )
\(m_{KMnO_4}=\dfrac{0,4.158}{\left(100-20\right)\%}=79g\)
a/ Số mol Fe là : nFe = 16,8: 56 = 0,3 mol
PTPƯ:
3Fe + 2O2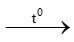 Fe3O4 (1)
Fe3O4 (1)
0,3 mol → 0,2mol → 0,1 mol
Từ (1) ta có số mol Fe3O4 = 0,1mol
→ m Fe3O4 = n.M = 0,1.232 = 23,2gam
b/ Từ (1) ta có số mol O2 đã dùng nO2 = 0,2 mol
Thể tích khí oxi đã dùng ở đktc: VO2 = n.22,4 = 0,2.22,4 = 4,48 lít
Thể tích không khí đã dùng: Vkk = 5. VO2= 5.4,48 = 22,4 lít.
c/ PTPƯ
2 KMnO4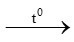 K2MnO4 + MnO2 + O2 (2)
K2MnO4 + MnO2 + O2 (2)
0,4444mol ← 0,222mol
Vì lượng Oxi thu được hao hụt 10% nên số mol O2 cần có là:
nO2 = 0,2mol.100/90 = 0.222 mol
Từ (2) ta có số mol KMnO4 = 0,444mol
Khối lượng KMnO4 bị nhiệt phân
mKMnO4 = n.M = 0,444.158 = 70.152 gam