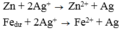number 1 : hh muối X gồm AHCO3 và A2CO#, chia 7,62 g X thành 3 phần bằng nhau :
Phần 1 : tác dụng hoàn toàn với HCl dư thu được 0,672l khí ( dktc )
Phần 2 : tác dụng hoàn toàn với BaCl2 dư thu được 1,97 g tủa
Phần 3 : tác dụng tối đa với 30ml dd NaOH a mol
a) xác định cthh muối
b) tính thành phần % khối lượng mỗi muối trong X
c) a ????
number 2 : cho m (g) hh X gồm 2 kim loại Mg và Fe ở dạng bột vào 50,0 g dd CuSO4 9,6%. Sau pứ thu được 2,48g rắn Y chứa 2 kim loại và dd Z. Thêm NaOH dư vao dd Z rồi lọc tủa, đem nung trong không khí đến khối lượng không đổi thu được 2,0 g rắn (các pứ xảy ra hoàn toàn )
a) tính m và thành phần % khối lượng từng kim loại trong X
b) xác định nồng dộ % các chất tan trong dd Z
number 3 : cho 12g CuO tác dụng vừa đủ dd H2SO4 25% thu được dd A, làm lạnh dd A xuống 20oC ( S = 20,5g) cho đến khi CuSO4.5H2O tách ra hoàn toàn, lọc kĩ đem cân đc m (g) tinh thể. m ????
number 4 : để đánh giá độ nhiễm bẩn H2S trong không khí của 1 nhà máy ng ta tiến hành thí nghiệm : " Lấy 1,4 l không khí ( đktc) rồi dẫn qua dd chì nitrat dư thì thu được 0,239 g tủa
a) tính % thể tích H2S trong 1,4 l không khí đó
b) sự nhiễm bẩn H2S có vượt quá mức cho phép không biết hàm lượng cho phép là 0,01 mg/l
c) một hs phát hiện có thể xử lý luojngwj H2S nhiễm bẩn trong dd bằng cách thổi liên tục khí O2 vào dd đó, nêu hiện tường và viết pthh