Đốt cháy m(g) hiđrocacbon X thu đc 2,688 lít khí CO2(đktc) và 4,32g H2O.
a, tính m?
b, Xác định CTPT của hiđrocacbon X?
Đốt cháy hoàn toàn một lượng hiđrocacbon X thu được 8,4 lít khí CO2 ở đktc và 5,4 gam nước. Xác định CTPT của X là:
![]()
![]()
![]()
![]()
Đốt cháy hoàn toàn một lượng hiđrocacbon X thu được 8,4 lít khí CO 2 ở đktc và 5,4 gam nước. Xác định CTPT của X là:
A. C 4 H 6
B. C 5 H 6
C. C 4 H 8
D. C 5 H 8
Đốt cháy 2,8 lít khí hiđrocacbon X tạo thành 8,4 lít CO2 và 6,75g H2O. Các thể tích khí ở đktc. Tìm CTPT và viết CTCT của hiđrocacbon X
$n_X = \dfrac{2,8}{22,4} = 0,125(mol)$
$n_{CO_2} = \dfrac{8,4}{22,4} = 0,375(mol)$
$n_{H_2O} = \dfrac{6,75}{18} = 0,375(mol)$
Bảo toàn nguyên tố C, H :
$n_C = n_{CO_2} = 0,375(mol) ; n_H = 2n_{H_2O} = 0,75(mol)$
Suy ra :
Số nguyên tử C = $\dfrac{0,375}{0,125} = 3$
Số nguyên tử H = $\dfrac{0,75}{0,125} = 6$
Vậy CTPT là $C_3H_6$
CTCT : $CH_2=CH-CH_3$
Đốt cháy hoàn toàn một hiđrocacbon thu được 6,72 lít co2 (đktc) và 3,6g h2o. Xác định CTPT và viết CTCT
Giúp em với ạ
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
Có: nCO2 > nH2O → Hidrocacbon là ankin.
⇒ n hidrocacbon = nCO2 - nH2O = 0,1 (mol)
Gọi CTPT của hidrocacbon là CnH2n-2
\(\Rightarrow n=\dfrac{0,3}{0,1}=3\)
→ CTPT là C3H4.
CTCT: \(CH\equiv C-CH_3\)
Ta có: \(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)\)
\(n_{H_2O}=\dfrac{14,4}{18}=0,8\left(mol\right)\)
Có: nH2O > nCO2 nên X là ankan.
⇒ nankan = 0,8 - 0,6 = 0,2 (mol)
Giả sử CTPT của X là CnH2n+2 ( n ≥ 1, nguyên).
\(\Rightarrow n=\dfrac{0,6}{0,2}=3\left(tm\right)\)
Vậy: X là C3H8.
BTNT O, có: \(n_{O_2}=\dfrac{0,6.2+0,8}{2}=1\left(mol\right)\)
\(\Rightarrow V_{O_2}=1.22,4=22,4\left(l\right)\)
Bạn tham khảo nhé!
đốt cháy hoàn toàn 2 hiđrocacbon đồng đẳng kế tiếp nhau thu được 3,36 lít khí co2(đktc) và 4,5 gam h20.
a) Xác định CTPT của 2 hidrocacbon
B) Tính thể tích của từng khí trong hỗn hợp ở đktc
n CO2=\(\dfrac{3,36}{22,4}\)=0,15 mol
n H2O=\(\dfrac{4,5}{18}\)=0,25 mol
n ankan=0,25-0,15=0,1 mol
C=\(\dfrac{0,15}{0,1}\)=1,5
=>Công thức là CH4 , C2H6
Thực hiện phản ứng đề hiđro hóa một hiđrocacbon M thuộc dãy đồng đẳng của metan thu được một hỗn hợp gồm H2 và 3 hiđrocacbon N, P, Q. Đốt cháy hoàn toàn 4,48 lít khí N hoặc P hoặc Q nếu thu được 17,92 lít CO2 và 14,4g H2O (thể tích các khí ở đktc). Hãy xác định cấu tạo của M?
A. CH 3 - CH 2 - CH 2 - CH 2 - CH 3
B. CH 3 - CH ( CH 3 ) 2
C. CH 3 - CH 2 - CH ( CH 3 ) 2
D. CH 3 - CH 2 - CH 2 - CH 3
Đáp án D
![]()
Vì ![]() nên N là anken
nên N là anken
Số nguyên tử C trong N là
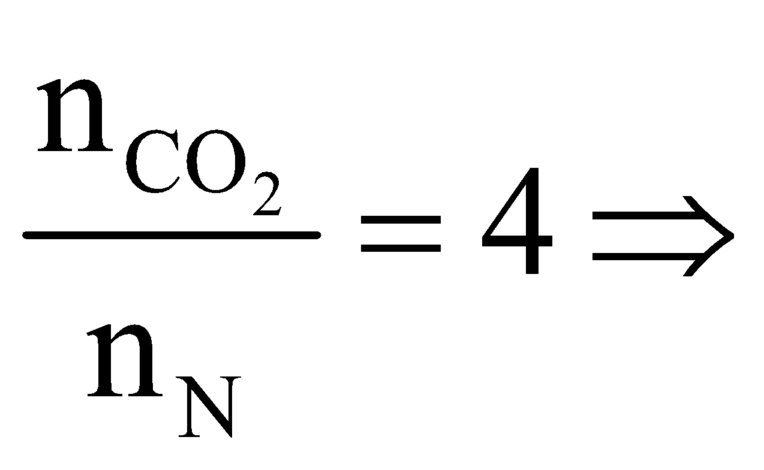 N là C4H8
N là C4H8
Khi đốt cháy N, hoặc P, hay Q đều cho số mol CO2 và H2O như nhau.
Suy ra N, P, Q đều là đồng phân của nhau và có cùng công thức phân tử là C4H8
Ta thấy đáp án A là phù hợp nhất khi tách hiđro tạo thành 3 sản phẩm là đồng phân của nhau
Đốt cháy hoàn toàn m gam một chất X chỉ chứa C và H, thu đc 2,68l CO2(đktc) và 4,32 g H2O. Tính m và xác định ctpt của X
Đốt cháy hoàn toàn 3,2 g bột hiđrocacbon A thu được 4,48l khí CO2 (đktc) và 7,2g H2O. Biết rằng A có khối lượng mol là 16g. Xác định công thức phân tử của hiđrocacbon A.
Gọi CTPT của hiđrocacbon A là \(C_xH_y\)(\(x,y\) nguyên dương)
\(m_H=2\cdot\dfrac{7,2}{18}=0,8\left(g\right)\\ m_C=12\cdot\dfrac{4,48}{22,4}=2,4\left(g\right)\\ \Rightarrow\dfrac{12x}{2,4}=\dfrac{y}{0,8}=\dfrac{16}{3,2}\\ \Rightarrow x=1;y=4\)
Vậy CTPT của hiđrocacbon A là \(CH_4\)