Cho 4,8 g kim loại M ( có hóa trị II trong hợp chất) tác dụng vừa đủ với 4.48 lít khí Clo ( ở đktc ).
a.Xác định kim loại M.
b.Tính m.

Những câu hỏi liên quan
Cho 4,8g kim loại M có hoá trị || trong hợp chất tác dụng vừa đủ với 4,48 khí Clo đktc .sau phản ứng thu được M gam muối. a.Xác định kim loại M b.Tính M nhỏ Giúp mình với,mình cảm ơn
a) \(n_M=\dfrac{4,8}{M_M}\left(mol\right)\)
\(n_{Cl_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: M + Cl2 --to--> MCl2
___\(\dfrac{4,8}{M_M}\)->\(\dfrac{4,8}{M_M}\)
=> \(\dfrac{4,8}{M_M}=0,2=>M_M=24\left(Mg\right)\)
b) \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: Mg + Cl2 --to--> MgCl2
_____0,2--------------->0,2
=> mMgCl2 = 0,2.95 = 19(g)
Đúng 3
Bình luận (0)
cho kim loại m hóa trị 3 tác dụng với clo thu được 4.48 lít khí a. xác định kim loại đã dùng b. tính khối lượng m
Cho 5,56g hỗn hợp A gồm Fe và kim loại M ( hóa trị không đổi) . Chia A thành 2 phần bằng nhau
Phần 1 : Hòa tan hết trong dd HCl được 1,568 lít khí H2(đktc)
Phần 2 : Tác dụng vừa đủ với 2,016 lít khí Cl2 ( đktc) . Xác định kim loại M? Giúp mình vớii
Gọi: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_M=y\left(mol\right)\end{matrix}\right.\) (trong 1 phần) ⇒ 56x + MM.y = 5,56:2 (1)
Giả sử M có hóa trị n không đổi.
- Phần 2: \(n_{Cl_2}=\dfrac{2,016}{22,4}=0,09\left(mol\right)\)
PT: \(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
\(2M+nCl_2\underrightarrow{t^o}2MCl_n\)
Theo PT: \(n_{Cl_2}=\dfrac{3}{2}n_{Fe}+\dfrac{n}{2}n_M=\dfrac{3}{2}x+\dfrac{n}{2}y=0,09\left(2\right)\)
- Phần 1: \(n_{H_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
+ TH1: M có pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2M+2nHCl\rightarrow2MCl_n+nH_2\)
Theo PT: \(n_{H_2}=n_{Fe}+\dfrac{n}{2}n_M=x+\dfrac{n}{2}y=0,07\left(3\right)\)
Từ (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}x=0,04\left(mol\right)\\ny=0,06\end{matrix}\right.\)
Thay vào (1), ta được: \(M_M.y=0,54\) \(\Rightarrow\dfrac{M_M.y}{n.y}=\dfrac{0,54}{0,06}\Rightarrow M_M=9n\)
Với n = 3 thì MM = 27 (g/mol) là thỏa mãn.
→ M là Al.
+ TH2: M không pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(x=n_{Fe}=n_{H_2}=0,07\left(mol\right)\)
Thay vào (1) ta được \(M_M.y=-1,14\) (vô lý vì MM và y đều là số dương)
Vậy: M là Al.
Đúng 2
Bình luận (0)
Cho 1,68 lít khí Cl2 tác dụng vừa đủ với kim loại M hóa trị II thu được 7,125gam muối. xác định M
\(n_{Cl_2}=\dfrac{1.68}{22.4}=0.075\left(mol\right)\)
\(M+Cl_2\underrightarrow{t^0}MCl_2\)
\(....0.075..0.075\)
\(M_{MCl_2}=\dfrac{7.125}{0.075}=95\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow M+71=95\)
\(\Rightarrow M=24\)
\(Mlà:Mg\)
Đúng 1
Bình luận (0)
cho 7,2 gam một kim loại M hóa trị 2 tác dụng vừa đủ với khí clo dư thu được 28,5 gam muối clorua Xác định kim loại
\(n_M=\dfrac{7,2}{M_M}\left(mol\right)\)
PTHH: M + Cl2 --to--> MCl2
\(\dfrac{7,2}{M_M}\)------------>\(\dfrac{7,2}{M_M}\)
=> \(\dfrac{7,2}{M_M}\left(M_M+71\right)=28,5=>M_M=24\left(Mg\right)\)
Đúng 2
Bình luận (0)
Trộn CuO với oxit kim loại M hóa trị II theo tỉ lệ mol tương ứng là 1 :2 được hỗn hợp B. Cho 4,8 gam hỗn hợp B này vào ống sứ, nung nóng rồi dẫn khí CO dư đi qua đến khi phản ứng xảy ra hoàn toàn thu được chất rắn D. Hỗn hợp D tác dụng vừa đủ với 160 ml dung dịch HNO3 1,25M thu được V lít khí NO. Kim loại M A. Zn B. Ca C. Mg D. Ca hoặc Mg
Đọc tiếp
Trộn CuO với oxit kim loại M hóa trị II theo tỉ lệ mol tương ứng là 1 :2 được hỗn hợp B. Cho 4,8 gam hỗn hợp B này vào ống sứ, nung nóng rồi dẫn khí CO dư đi qua đến khi phản ứng xảy ra hoàn toàn thu được chất rắn D. Hỗn hợp D tác dụng vừa đủ với 160 ml dung dịch HNO3 1,25M thu được V lít khí NO. Kim loại M
A. Zn
B. Ca
C. Mg
D. Ca hoặc Mg
Trộn CuO với oxit kim loại M hóa trị II theo tỉ lệ mol tương ứng là 1:2 được hỗn hợp B. Cho 4,8 gam hỗn hợp B này vào ống sứ, nung nóng rồi dẫn khí CO dư đi qua đến khi phản ứng xảy ra hoàn toàn thu được chất rắn D. Hỗn hợp D tác dụng vừa đủ với 160 ml dung dịch HNO3 1,25M thu được V lít khí NO. Kim loại M là A. Zn B. Ca C. Mg D. Ca hoặc Mg
Đọc tiếp
Trộn CuO với oxit kim loại M hóa trị II theo tỉ lệ mol tương ứng là 1:2 được hỗn hợp B. Cho 4,8 gam hỗn hợp B này vào ống sứ, nung nóng rồi dẫn khí CO dư đi qua đến khi phản ứng xảy ra hoàn toàn thu được chất rắn D. Hỗn hợp D tác dụng vừa đủ với 160 ml dung dịch HNO3 1,25M thu được V lít khí NO. Kim loại M là
A. Zn
B. Ca
C. Mg
D. Ca hoặc Mg
Gọi oxit kim loại phải tìm là MO và nCuO = a và nMO =2a
nHNO3 = 0.15 mol
Vì hiđro chỉ khử được những oxit kim loại đứng sau nhôm trong dãy điện hóa nên có 2 trường hợp xảy ra.
∙ Trường hợp 1: M đứng sau nhôm trong dãy điện hóa
CuO + H2 → Cu + H2O
MO + H2 → M + H2O
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
3M + 8HNO3 → 3M(NO3)2 + 2NO + 4H2O
Ta có hệ pt:
{ 80a + (M +16).2a = 3.6
8a/3 + 16a/3 = 0.15 }
a = 0,01875 và M = 40 → M là Ca.
Trường hợp này loại vì CaO không bị khử bởi khí H2.
∙ Trường hợp 2: M đứng trước nhôm trong dãy điện hóa
CuO + H2 → Cu + H2O
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
MO + 2HNO3 → M(NO3)2 + 2H2O
Ta có hệ pt:
{ 80a + (M +16).2a = 3.6
8a/3 + 4a = 0.15 }
a = 0,0225 và M = 24 → M là Mg → Đáp án C
Đúng 0
Bình luận (0)
Trộn CuO với oxit kim loại M hóa trị II theo tỉ lệ mol tương ứng là 1:2 được hỗn hợp B. Cho 4,8 gam hỗn hợp B này vào ống sứ, nung nóng rồi dẫn khí CO dư đi qua đến khi phản ứng xảy ra hoàn toàn thu được chất rắn D. Hỗn hợp D tác dụng vừa đủ với 160 ml dung dịch HNO3 1,25M thu được V lít khí NO. Kim loại M là A. Zn B. Ca C. Mg D. Ca hoặc Mg
Đọc tiếp
Trộn CuO với oxit kim loại M hóa trị II theo tỉ lệ mol tương ứng là 1:2 được hỗn hợp B. Cho 4,8 gam hỗn hợp B này vào ống sứ, nung nóng rồi dẫn khí CO dư đi qua đến khi phản ứng xảy ra hoàn toàn thu được chất rắn D. Hỗn hợp D tác dụng vừa đủ với 160 ml dung dịch HNO3 1,25M thu được V lít khí NO. Kim loại M là
A. Zn
B. Ca
C. Mg
D. Ca hoặc Mg
Đáp án C
Gọi số mol CuO và MO là a,2a(mol)
TH1:CO khử được MO
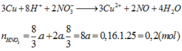
=>a=0,025=>80a+(M+16).2a=4,8
=>M là Ca(loại vì CaO không bị CO khử)
Không có M thỏa mãn lọai
TH2.CO không khử đc MO
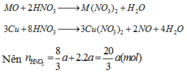
=>a=0,03(mol) =>80a+(M+16).2a=4,8=>M=24
Đúng 0
Bình luận (0)
Cho 3,9 gam kim loại hoá trị I tác dụng với H2O dư, thu được 1,12 lít H2(đktc) a.Xác định M. b.Tính khối lượng bazơ tạo thành.
a, \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: 2M + H2O → 2MOH + H2
Mol: 0,1 0,1 0,05
\(M_M=\dfrac{3,9}{0,1}=39\left(g/mol\right)\)
⇒ M là kali (K)
b, \(m_{KOH}=0,1.56=5,6\left(g\right)\)
Đúng 0
Bình luận (0)

















