để đốt cháy hoàn toàn 0,74g CR A cần 1,12l khong khí chứa 20% O về thể tích. Sản phẩm là CO2, H2O và Na2CO3. trong đó có 2,24ml Co2 và 0,53g Na2CO3. Tìm CT của A ở dạng thực nghiệm

Những câu hỏi liên quan
CÂU 1) Đốt cháy hoàn toàn 0,74g chất rắn X cần 1,12dm3 không khí chứa 20% thể tích O2 . Sản phẩm đốt cháy gồm 224cm3 CO2; 0,53g Na2CO3 và H2O. Biết thể tích các khí đo ở đktc. A có công thức phân tử đơn giản là:A. C2H4O4Na2 B. C3H2O3Na2C. C3H2O4Na2 D. C3H2O2Na2CÂU 2) Nguyên tố hh là :a. yếu tố cơ bản cấu tạo nên nguyên tửb. phần tử cơ bản tạo nên vật chấtc. ngyên tử cùng loạid. phần tử chính cấu tạo nên nguyên tử
Đọc tiếp
CÂU 1) Đốt cháy hoàn toàn 0,74g chất rắn X cần 1,12dm3 không khí chứa 20% thể tích O2 . Sản phẩm đốt cháy gồm 224cm3 CO2; 0,53g Na2CO3 và H2O. Biết thể tích các khí đo ở đktc. A có công thức phân tử đơn giản là:
A. C2H4O4Na2 B. C3H2O3Na2
C. C3H2O4Na2 D. C3H2O2Na2
CÂU 2) Nguyên tố hh là :
a. yếu tố cơ bản cấu tạo nên nguyên tử
b. phần tử cơ bản tạo nên vật chất
c. ngyên tử cùng loại
d. phần tử chính cấu tạo nên nguyên tử
CÂU 2) Nguyên tố hh là :
a. yếu tố cơ bản cấu tạo nên nguyên tử
b. phần tử cơ bản tạo nên vật chất
c. ngyên tử cùng loại
d. phần tử chính cấu tạo nên nguyên tử
Đúng 0
Bình luận (0)
Câu 1 :
\(V_{kk}=1.12\left(l\right)\)
\(\Rightarrow n_{O_2}=\dfrac{1.12}{22.4}\cdot20\%=0.01\left(mol\right)\)
\(n_{CO_2}=\dfrac{0.224}{22.4}=0.01\left(mol\right)\)
\(n_{Na_2CO_3}=\dfrac{0.53}{106}=0.005\left(mol\right)\)
\(BTKL:\)
\(m_{H_2O}=0.74+0.01\cdot32-0.01\cdot44-0.53=0.09\left(g\right)\)
\(n_{H_2O}=\dfrac{0.09}{18}=0.005\left(mol\right)\)
\(m_{O\left(X\right)}=0.74-0.015\cdot12-0.005\cdot2-0.005\cdot2\cdot23=0.32\left(g\right)\)
\(n_O=0.02\left(mol\right)\)
\(CT:C_xH_yO_zNa_t\)
\(x:y:z:t=0.015:0.01:0.02:0.01=3:2:4:2\)
\(CT:C_3H_2O_4Na_2\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 0,74 g chất rắn X cần 1,12 lít không khí chứa 20% thể tích oxi. Sản phẩm đốt cháy gồm 224cm3 CO2, 0,53g Na2CO3 và H2O. Xác định công thức phân tử đơn giản của A biết thể tích các khí đo ở điều kiện tiêu chuẩn.
1,12 dm3= 1,12 lit
224cm3 = 0.224lit
n(kk)= 1,12/ 22,4 =0,05 mol
n (O2)= 0,05x 20%= 0,01 mol
n(CO2)= 0,01 mol
n(Na2CO3) = 0,005 mol
suy ra
m( sản phẩm)= m ( chất phản ứng) = 0,74 + 0,01x 32=1,06 g
m(H2O)= 1,06 – 0,01x 44 – 0,53= 0,09g
n(H2O)=0,005 mol
vì đốt A tạo ra CO2 Na2CO3 và H2O nên trong A có Na, C, H và có thể có O
Ta có:
nO ( có trong sản phẩm) = 0,01x2 + 0,005x3 +0,005= 0,04 mol > nO (O2)= 0,01x2=0,02 mol
trong A có O
nO (A) = 0,04- 0,02 = 0,02 mol
n Na(A) = 0,005x2= 0,01 mol
nH(A)=0,005x2= 0,01 mol
nC (A)= 0,01 + 0,005= 0,015mol
nNa : nH : nC : nO= 0,01: 0,01: 0,015 : 0,02
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 0,74g chất rắn A cần 1,12 dm3 ko khí (đkc) chứa 20% V(O2). Sản phẩm là CO2, H2) và Na2CO3 trong đó có 224cm3 CO2(đkc) và 0,53g Na2CO3. Tìm CT A dạng thực nghiệm
1,12 dm3= 1,12 lit
224cm3 = 0.224lit
n(kk)= 1,12/ 22,4 =0,05 mol
n (O2)= 0,05x 20%= 0,01 mol
n(CO2)= 0,01 mol
n(Na2CO3) = 0,005 mol
suy ra
m( sản phẩm)= m ( chất phản ứng) = 0,74 + 0,01x 32=1,06 g
m(H2O)= 1,06 – 0,01x 44 – 0,53= 0,09g
n(H2O)=0,005 mol
vì đốt A tạo ra CO2 Na2CO3 và H2O nên trong A có Na, C, H và có thể có O
Ta có:
nO ( có trong sản phẩm) = 0,01x2 + 0,005x3 +0,005= 0,04 mol > nO (O2)= 0,01x2=0,02 mol
trong A có O
nO (A) = 0,04- 0,02 = 0,02 mol
n Na(A) = 0,005x2= 0,01 mol
nH(A)=0,005x2= 0,01 mol
nC (A)= 0,01 + 0,005= 0,015mol
nNa : nH : nC : nO= 0,01: 0,01: 0,015 : 0,02
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 0,74 gam chất rắn A cần dùng 1,12 dm3 không khí (đktc) chứa 20% VO2. Sản phẩm là CO2, H2O và Na2CO3 trong đó có 244 cm3 CO2 (đktc) và 0,53 gam Na2CO3. Tìm công thức hiđrocacbon
$n_{O_2} = \dfrac{1,12}{22,4}.20\% = 0,01(mol)$
$n_{CO_2} = \dfrac{244}{1000.22,4} = 0,01(mol)$
$n_{Na_2CO_3} = 0,005(mol)$
Bảo toàn khối lượng : $n_{H_2O} = \dfrac{0,74 + 0,01.32 - 0,01.44 - 0,53}{18} = 0,005(mol)$
Ta có :
$n_C = n_{CO_2} + n_{Na_2CO_3} = 0,015(mol)$
$n_H = 2n_{H_2O} = 0,01(mol)$
$n_O = 0,01.2 + 0,005.3 + 0,005 - 0,01.2 = 0,02(mol)$
$n_{Na} = 2n_{Na_2CO_3} = 0,005.2 = 0,01(mol)$
Ta có:
$n_C : n_H : n_O : n_{Na} = 0,015 : 0,01 : 0,02 : 0,01 = 3 : 2 : 4 : 2$
Vậy A có CTĐGN là $C_3H_2O_4Na_2$
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 11,6 gam chất hữu cơ A thu được 5,3 g Na2CO3 và khí X (gồm có CO2 và H2O) . Dẫn khí X vào bình chứa nước voi trong(dư), kết thúc thí nghiệm thấy khối lượng bình tăng 28,7g và có 55g kết tủa . Hãy xác định CT phần tử của A, biết rằng A chỉ có 1 nguyên tử Oxi
Đốt cháy hoàn toàn 11,6 gam chất hữu cơ A thu được 5,3 g Na2CO3 và khí X (gồm có CO2 và H2O) . Dẫn khí X vào bình chứa nước voi trong(dư), kết thúc thí nghiệm thấy khối lượng bình tăng 28,7g và có 55g kết tủa . Hãy xác định CT phần tử của A, biết rằng A chỉ có 1 nguyên tử Oxi
Để đốt cháy hoàn toàn 4,45 gam hợp chất A cần dùng vừa hết 4,2 lít O2. Sản phẩm cháy gồm có 3,15 gam H2O và 3,92 lít hỗn hợp khí gồm CO2 và N2. Biết thể tích các khi đo ở đktc, trong phân tử của A có 1 nguyên tử nitơ (N). Công thức phân tử của A là: A. C3H7O2N. B. C3H9N. C. C4H9O2N. D. C4H11N.
Đọc tiếp
Để đốt cháy hoàn toàn 4,45 gam hợp chất A cần dùng vừa hết 4,2 lít O2. Sản phẩm cháy gồm có 3,15 gam H2O và 3,92 lít hỗn hợp khí gồm CO2 và N2. Biết thể tích các khi đo ở đktc, trong phân tử của A có 1 nguyên tử nitơ (N). Công thức phân tử của A là:
A. C3H7O2N.
B. C3H9N.
C. C4H9O2N.
D. C4H11N.
Đáp án A
,nO2 = 0,1875 mol
Bảo toàn khối lượng : mA + mO2 = mCO2 + mN2 + mH2O
=> mCO2 + mN2 = 7,3g
Mặt khác : nCO2 + nN2 = 0,175 mol
=> nCO2 = 0,15 ; nN2 = 0,025 mol
Bảo toàn O : nO(A) = 2nCO2 + nH2O – 2nO2 = 0,1 mol
=> nC : nH : nO : nN = 0,15 : 0,0,35 : 0,1 : 0,05 = 3 : 7 : 2 : 1
Vì A chỉ có 1 nguyên tử N nên A có CTPT là : C3H7O2N
Đúng 0
Bình luận (0)
Hỗn hợp X chứa muối natri của 2 axit cacboxylic đơn chức là đồng đẳng kế tiếp. Đốt cháy hoàn toàn hỗn hợp X sản phẩm thu được gồm H2O, Na2CO3 và CO2 trong đó số mol CO2 đúng bằng số mol X phản ứng. Công thức cấu tạo thu gọn của 2 muối trong X là A. CH3COONa và C2H5COONa. B. C2H5COONa và C3H7COONa. C. C2H3COONa và C3H5COONa. D. CH3COONa và HCOONa.
Đọc tiếp
Hỗn hợp X chứa muối natri của 2 axit cacboxylic đơn chức là đồng đẳng kế tiếp. Đốt cháy hoàn toàn hỗn hợp X sản phẩm thu được gồm H2O, Na2CO3 và CO2 trong đó số mol CO2 đúng bằng số mol X phản ứng. Công thức cấu tạo thu gọn của 2 muối trong X là
A. CH3COONa và C2H5COONa.
B. C2H5COONa và C3H7COONa.
C. C2H3COONa và C3H5COONa.
D. CH3COONa và HCOONa.
Đáp án D
gọi n x = a . Vì 2 muối đều có 1 nguyên tử Na trong phân tử nên
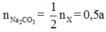
Mặt khác ![]()
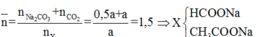
Đúng 0
Bình luận (0)
Để đốt cháy hoàn toàn 4,45 g hợp chất A cần dùng vừa hết 4,20 lít
O
2
. Sản phẩm cháy gồm có 3,15 g
H
2
O
và 3,92 lít hỗn hợp khí gồm
C
O
2
và
N
2
. Các thể tích ở đktc. Xác định công thức đơn giản nhất của chất A.
Đọc tiếp
Để đốt cháy hoàn toàn 4,45 g hợp chất A cần dùng vừa hết 4,20 lít O 2 . Sản phẩm cháy gồm có 3,15 g H 2 O và 3,92 lít hỗn hợp khí gồm C O 2 và N 2 . Các thể tích ở đktc. Xác định công thức đơn giản nhất của chất A.
Theo định luật bảo toàn khối lượng :
![]()
Đặt số mol C O 2 là a, số mol N2 là b, ta có :
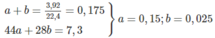
Khối lượng C: 0,150 x 12,0 = 1,80 (g).
Khối lượng H: 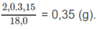
Khối lượng N: 0,0250 x 28,0 = 0,700 (g).
Khối lượng O: 4,48 - 1,80 - 0,35 - 0,700 = 1,60 (g).
Chất A có dạng C x H y N z O t
x : y ; z : t = 0,15 : 0,35 : 0,05 : 0,10 = 3 : 7 : 1 : 2
Công thức đơn giản nhất của A là C 3 H 7 N O 2
Đúng 0
Bình luận (0)














