1. Nung hỗn hợp gồm 3g cacbon và 10g đồng (II) ôxit trong bình kín, sau phản ứng thu được ag đồng và giải phóng 2,75g khí cacbonic.
a) Viết phương trình chữ của phản ứng trên?
b) Tìm giá trị của a.
a) Hãy viết PTHH của các phản ứng giữa khí hidro với hỗn hợp đồng(II) ôxit và sắt (III) ôxit ở nhoẹt dộ thích hợp b) Nếu thu đc 6g hỗn hợp 2kloại trong đó có 2,8g sắt thì thể tích ở đktc khí hidro cần đủ để khử đồng (II) ôxit và sắt (III) ôxit là bao nhiêu?
a, \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, Ta có: \(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
\(m_{Cu}=6-2,8=3,2\left(g\right)\Rightarrow n_{Cu}=\dfrac{3,2}{64}=0,05\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Cu}+\dfrac{3}{2}n_{Fe}=0,125\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,125.22,4=2,8\left(l\right)\)
Trong bình kín không có không khí chứa bột hỗn hợp của 2,8 g Fe và 3,2 g S. Đốt nóng hỗn hợp cho phản ứng xảy ra hoàn toàn, sau phản ứng thu được sắt (II) sunfua (FeS).
a) Viết phương trình hoá học của phản ứng.
b) Tính khối lượng FeS thu được sau phản ứng biết lưu huỳnh dư 1,6 g.
PTHH: \(Fe+S\xrightarrow[]{t^o}FeS\)
Tính theo Fe
Ta có: \(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)=n_{FeS}\) \(\Rightarrow m_{FeS}=0,05\cdot88=4,4\left(g\right)\)
Nung hỗn hợp bột gồm Cu và KClO3 (tỉ lệ mol 1:1) trong bình kín, sau phản ứng kết thúc thu được khí X và chất rắn Y. Dùng khí X để đốt cháy hết hỗn hợp C và S thu được hỗn hợp khí Z gồm 3 khí. Xác định X, Y, Z và viết các phương trình hóa học.
\(X:O_2\\ Y:KCl,CuO,Cu,KClO_4\left(có.thể.có\right)\\ Z:CO,CO_2,SO_2\\ KClO_3-^{^{ }t^{^{ }0}}->KCl+\dfrac{3}{2}O_2\\4 KClO_3-^{^{ }t^{^{ }0}}->KCl+3KClO_4\\ Cu+\dfrac{1}{2}O_2-^{^{ }t^{^{ }0}}->CuO\\ C+O_2-^{t^0}->CO_2\\ C_{dư}+\dfrac{1}{2}O_2-^{t^0}->CO\\ S+O_2-^{t^0}->SO_2\)
Một bình kín chỉ chứa một ít bột niken và hỗn hợp X gồm 0,05 mol điaxetilen (HC≡C-C≡CH), 0,1 mol hiđro. Nung nóng bình một thời gian, thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 22,5. Cho Y phản ứng vừa đủ với 0,04 mol AgNO3 trong NH3, sau phản ứng thu được 5,84 gam kết tủa và 0,672 lít (đktc) hỗn hợp khí Z. Khí Z phản ứng với tối đa a mol Br2 trong dung dịch. Giá trị của a là
A. 0,02
B. 0,04
C. 0,03
D. 0,01.
Một bình kín chỉ chứa một ít bột niken và hỗn hợp X gồm 0,05 mol điaxetilen (HC≡C-C≡CH), 0,1 mol hiđro. Nung nóng bình một thời gian, thu được hỗn hợp khí Y có tỉ khối hơi so với H2 bằng 22,5. Cho Y phản ứng vừa đủ với 0,04 mol AgNO3 trong dung dịch NH3, sau phản ứng thu được 5,84 gam kết tủa và 0,672 lít (đktc) hỗn hợp khí Z. Khí Z phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là:
A. 0,02.
B. 0,03.
C. 0,01.
D. 0,04.
Chọn A
Vì:![]()
![]()
![]()
![]()
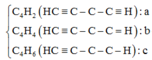
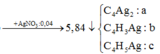
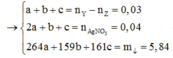
![]()
![]()
→ a = n π L = 0,11 - 0,09 = 0.02
Một bình kín chỉ chứa một ít bột niken và hỗn hợp X gồm 0,05 mol điaxetilen (HC≡C-C≡CH), 0,1 mol hiđro. Nung nóng bình một thời gian, thu được hỗn hợp khí Y có tỉ khối hơi so với H2 bằng 22,5. Cho Y phản ứng vừa đủ với 0,04 mol AgNO3 trong dung dịch NH3, sau phản ứng thu được 5,84 gam kết tủa và 0,672 lít (đktc) hỗn hợp khí Z. Khí Z phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
A. 0,02.
B. 0,03.
C. 0,01.
D. 0,04.
Một bình kín chỉ chứa một ít bột niken và hỗn hợp X gồm 0,05 mol điaxetilen (HC≡C-C≡CH), 0,1 mol hiđro. Nung nóng bình một thời gian, thu được hỗn hợp khí Y có tỉ khối hơi so với H2 bằng 22,5. Cho Y phản ứng vừa đủ với 0,04 mol AgNO3 trong dung dịch NH3, sau phản ứng thu được 5,84 gam kết tủa và 0,672 lít (đktc) hỗn hợp khí Z. Khí Z phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
A. 0,02.
B. 0,03.
C. 0,01.
D. 0,04.
Nung m gam hỗn hợp KClO3 và KMnO4 thu được chất rắn Y và O2, biết KClO3 phản ứng hết, còn KMnO4 còn dư một phần, trong Y có 0,894 gam KCl chiếm 8,132% theo khối lượng, trộn lượng O2 trên với không khí theo tỉ lệ 1:3 trong bình kín ta thu được hỗn hợp khí Z, cho vào bình 0,528 gam Cacbon rồi đốt cháy hết thì thu được hỗn hợp khí T gồm N2, O2, CO2 trong đó CO2 chiếm 22,92% về thể tích. Giá trị của m gần nhất với giá trị nào sau đây?
A. 11,96
B. 12,40
C. 12,53
D. 12,12
Có sự thay đổi số mol hỗn hợp khí xảy ra trong các phản ứng đốt cháy, hoặc đôi khi không thay đổi.
C/S + O2 → CO2/ SO2 (1)
2Al +3/2O2 → Al2O3 (2)
C, S hay A1, chúng là các chất rắn được đem đốt cháy với oxi hoặc một hỗn hợp khí chứa oxi,… và sau phản ứng người ta thu được một khí/hỗn hợp khí mới,…
Trong nhiều trường hợp, ta cần so sánh số mol hỗn hợp khí mới và cũ, như trong tình huống (1), hai giá trị này bằng nhau, tình huống (2) thì khác, khi có oxit tạo thành, tổng số mol khí sẽ giảm.
Với bài tập này, phản ứng của cacbon với oxi xảy ra và số mol hỗn hợp khí không thay đổi, đó chỉ là một sự thay thế như tăng giảm khối lượng vậy, O2 trở thành CO2 theo tỉ lệ 1:1 → nZ = nT
Bảo toàn nguyên tố C: nC/T = nCO2/T = 0,528/12 =0,044
→nT = 0,044/22,92% = 0,192 = nZ → nO2 trộn = 0,192/4 =0,048
→m = mY + mO2 = 0,894/8,132% + 32.0,048 = 12,5296
Chọn đáp án C
a) PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
b) Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\) \(\Rightarrow n_{Al}=0,1mol\)
\(\Rightarrow m_{Al}=0,1\cdot27=2,7\left(g\right)\) \(\Rightarrow m_{Ag}=7,3\left(g\right)\)